2020-12-18 理化学研究所,科学技術振興機
理化学研究所(理研)革新知能統合研究センター分子情報科学チームのアドナン・スリオカ研究員らの国際共同研究チームは、核磁気共鳴(NMR)法[1]に情報・数理科学の手法を適用することで、推定されたタンパク質構造の精度を評価する「Accuracy of NMR Structures Using Random coil index and Rigidity;ANSURR法」を開発しました。
本研究成果は、創薬ターゲットとなるタンパク質の構造決定のプロセスを加速し、疾病の新たな治療法などの開発に貢献すると期待できます。
X線結晶解析法では推定されたタンパク質構造の精度評価法が確立しているのに対し、NMR法では試料を結晶化しなくても細胞内の状況に近い溶液中でタンパク質構造を推定できるという利点がありながら、これまで精度評価の有効な方法がなく、その応用が制限されてきました。
今回、国際共同研究チームは、NMR法によって得られる情報のうち、これまで構造決定には使用されていなかった「化学シフト[2]」から得られるランダムコイル指標と、「数理剛性理論[3]」から得られる指標(構造柔軟性)を比較することで、推定されたタンパク質構造の精度を評価することに成功しました。
本研究は、オンライン科学雑誌『Nature Communications』(12月18日付)に掲載されます。
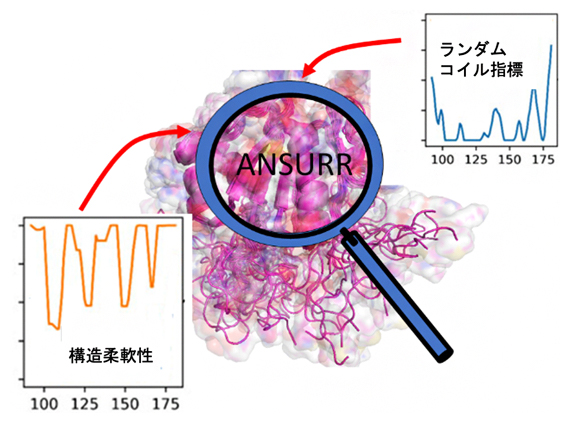
ANSURR法では二つの指標(青とオレンジ)を比較することで精度評価する
背景
核磁気共鳴(NMR)法は、原子核を磁場の中に入れ、核スピンの共鳴現象を観測することで、分子の構造を解析する方法です。論文の共著者でもあるウィリアムソン教授らによって、1985年に初めてタンパク質構造がNMR法によって解かれて以来、多くのタンパク質構造がNMR法によって決定されてきました。
しかし、タンパク質構造データバンク(Protein Data Bank)に登録されている構造の大部分はX線結晶解析法によるものであり、NMR法によるものは10%に過ぎません。このような偏りの一因は、X線結晶解析法には優れた推定精度評価の仕組みがあるのに対し、NMR法には広く受け入れられている推定精度評価法が存在しないため、構造の正確さに関する不安が払拭されない点にあります。
研究手法と成果
今回、国際共同研究チームは、NMR法によって推定されたタンパク質構造の精度を評価する「Accuracy of NMR Structures Using Random coil index and Rigidity;ANSURR)法」を開発しました。ANSURR法では、タンパク質の各アミノ酸残基において定義される局所的剛性に関する2種類の指標を比較することで精度評価を行います。
一つ目は、NMR装置から得られる情報の一つである「化学シフト」から導かれるランダムコイル指標と呼ばれる既存の指標です。
もう一つは、「数理剛性理論」を用いて、NMR法で推定された構造から導き出される指標で、それをランダムコイル指標と比較することで、精度の評価を行います。数理剛性理論とは、棒が関節で接合された枠組みを扱う理論です。分子を扱う場合には、各原子が関節となり、共有結合と水素結合が棒に対応します。数理剛性理論は、主に建築などの分野で耐震性などを計算するために用いられてきましたが、タンパク質構造への応用も近年進んでいます。ANSURR法においては、NMRタンパク質構造に対して、この理論を適用することで、各アミノ残基における局所的剛性指標(構造柔軟性)を導き出します。この指標は化学シフトとは独立な情報から導き出されているため、ランダムコイル指標との相関を計算することで、タンパク質構造の精度を推定できます(図1)。
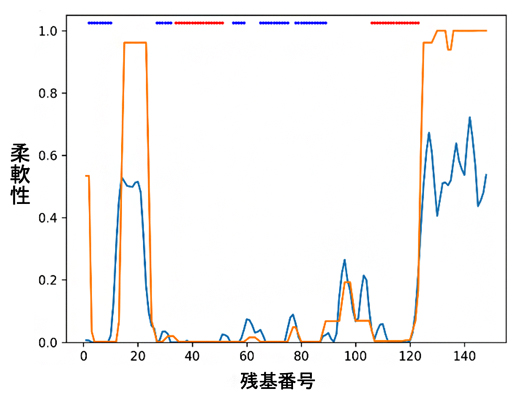
図1 ランダムコイル指標(青)と構造柔軟性(オレンジ)の比較
この場合は2指標間の相関が高いため、NMRタンパク質構造の精度は高いと判断される。
今後の期待
NMR法はタンパク質を結晶化する必要がなく、溶液中のタンパク質の構造を推定できるため、生物学的機能を探る上で非常に有効な方法です。今後、ANSURR法を利用することで、多くの研究者がNMRタンパク質構造の推定精度評価を行えるようにする予定です。これまで、精度保証がないことでNMR構造の使用を躊躇していた創薬研究者も、ANSURR法が完成したことにより、より積極的にNMR構造を利用することが期待できます。
本研究は、数理理論が構造生物学の基礎に対して大きく貢献できることを示す良い例といえます。今後も数理研究を推進することで、自然科学の研究に貢献したいと考えています。
補足説明
1.核磁気共鳴(NMR)法
強い磁場中に置かれた原子核に電磁波を照射すると、核スピンの共鳴現象により、原子核の性質や周囲の環境に応じた周波数(共鳴周波数)の電磁波の吸収や放出が起こるが、その電磁波をNMR信号として捉えることで、物質の分子構造の解析や物性の解析を行う手法。NMRはNuclear Magnetic Resonanceの略。
2.化学シフト
核の周囲の電子の空間的分布の違いにより、試料の共鳴周波数が、基準物質の周波数から変化する現象。本研究では、NMR装置から得られる化学シフトに関する情報から、ランダムコイル指標を計算している。
3.数理剛性理論
例えば、二次元平面において□の形に組まれた枠組みは、力を加えて変形させることができるが、もう一本加えて〼にすると変形できない剛体になる。このような性質を数理的に解析する理論を数理剛性理論という。
国際共同研究チーム
理化学研究所 革新知能統合研究センター 分子情報科学チーム
研究員 アドナン・スリオカ(Adnan Sljoka)
シェフィールド大学
研究員 ニコラス・ファウラー(Nicholas J. Fowler)
教授 マイク・ウィリアムソン(Mike P. Williamson)
研究支援
本研究は、科学技術振興機構(JST)戦略的創造研究推進事業CREST「ビッグデータ時代に向けた革新的アルゴリズム基盤(研究代表者:加藤直樹)」による支援を受けて行われました。
原論文情報
Nicholas J. Fowler, Adnan Sljoka and Mike P. Williamson, “A method for validating the accuracy of NMR protein structures”, Nature Communications, 10.1038/s41467-020-20177-1
発表者
理化学研究所
革新知能統合センター 分子情報科学チーム
研究員 アドナン・スリオカ(Adnan Sljoka)
報道担当
理化学研究所 広報室 報道担当
科学技術振興機構 広報課
JST事業に関すること
科学技術振興機構 戦略研究推進部 ICTグループ
舘澤 博子(たてさわ ひろこ)