2025-01-22 分子科学研究所
【発表のポイント】
- 〇 DNAナノ粒子モーターはナノスケールの輸送システムやデバイスとして注目されている人工分子モーターであるが、天然のモータータンパク質と比べて運動速度が遅く、走行距離が短いという問題があった。
- 〇 運動と化学反応の素過程を解析することでDNAナノ粒子モーターの運動のボトルネック過程を特定した。
- 〇 シミュレーションによる予測と高速高精度1粒子トラッキング実験による検証に基づいて合理的に改造することで、天然のモータータンパク質に匹敵する運動速度と走行距離を実現した。
- 〇 今後、完全な一方向性運動を実現する研究に取り組むことで、生物を超える人工分子システムや新たな検査技術への応用が期待される。
【概要】
分子科学研究所/総合研究大学院大学の原島崇徳助教、大友章裕助教(当時、現京都大学大学院理学研究科助教)、飯野亮太教授らの研究グループは、人工分子モーターの一種であるDNAナノ粒子モーターの運動素過程と化学反応素過程の解析に基づき、合理的に運動性能を向上させることに成功しました。この成果により、30 nm/s(秒速30ナノメートル、ナノメートルは1メートルの10億分の1の大きさ)の運動速度と3 μm(マイクロメートル、= 1000ナノメートル)の走行距離を同時に達成し、天然に存在するモータータンパク質の運動性能に匹敵する人工分子モーターを初めて実現しました。本研究成果は国際学術誌「Nature Communications」に2025年1月16日付でオンライン掲載されました。
1. 研究の背景
キネシンやミオシンに代表される天然のモータータンパク質(*1)は、ATP分子(*2)をエネルギー源として自律的かつ10-1000 nm/sの速度で高速に運動することにより、細胞内での物質輸送や筋肉の収縮など、生命活動において重要な役割を担っています。モータータンパク質に触発され、人工的に分子モーターを設計しナノスケールの輸送システムやデバイスとして利用する研究が盛んに行われています。特に、DNA分子(*3)を利用した人工分子モーターは、塩基配列や構造の設計自由度の高さから注目されています。しかし、DNA人工分子モーターは運動速度が約0.1 nm/sと非常に遅いことが課題でした。運動速度を改善した人工分子モーターとして最近、DNAを金ナノ粒子に修飾したDNAナノ粒子モーターが開発されました。DNAナノ粒子モーターの運動速度は1 nm/s程度とナノサイズの人工分子モーターの中では最速ですが、依然として天然のモータータンパク質には及んでいません。本研究グループは、DNAナノ粒子モーターの運動のボトルネック過程(*4)を特定・改善することにより運動速度のさらなる向上に取り組みました。
2. 研究の成果
本研究ではまず、DNAナノ粒子モーターの運動速度を制限する要因を明らかにするため、暗視野顕微鏡を用いた高速高精度1粒子トラッキング(*5)を実施しました(図1左)。DNAナノ粒子モーターは、DNA修飾金ナノ粒子、RNA修飾基板、RNA分解酵素RNase Hにより構成され、DNA修飾金ナノ粒子がモーター、RNA修飾基板がレールに相当します。金ナノ粒子上のDNAは、基板上のRNAと二重鎖を形成することにより、ナノ粒子が基板に結合します。次に、RNase HはDNA/RNAによる二重鎖上のRNAを選択的に分解するため、RNaseH によりレールが一部破壊され、モーターは先ほどまでいた位置に戻ることが出来なくなります。このDNA/RNA二重鎖形成とRNA分解の過程を繰り返すことで、熱ゆらぎによるブラウン運動(ランダムな動き)が整流され前進するという仕組みです。この仕組みは、レールを分解して退路を断って前進するBurnt Bridge型ブラウンラチェット(*6)として知られています。
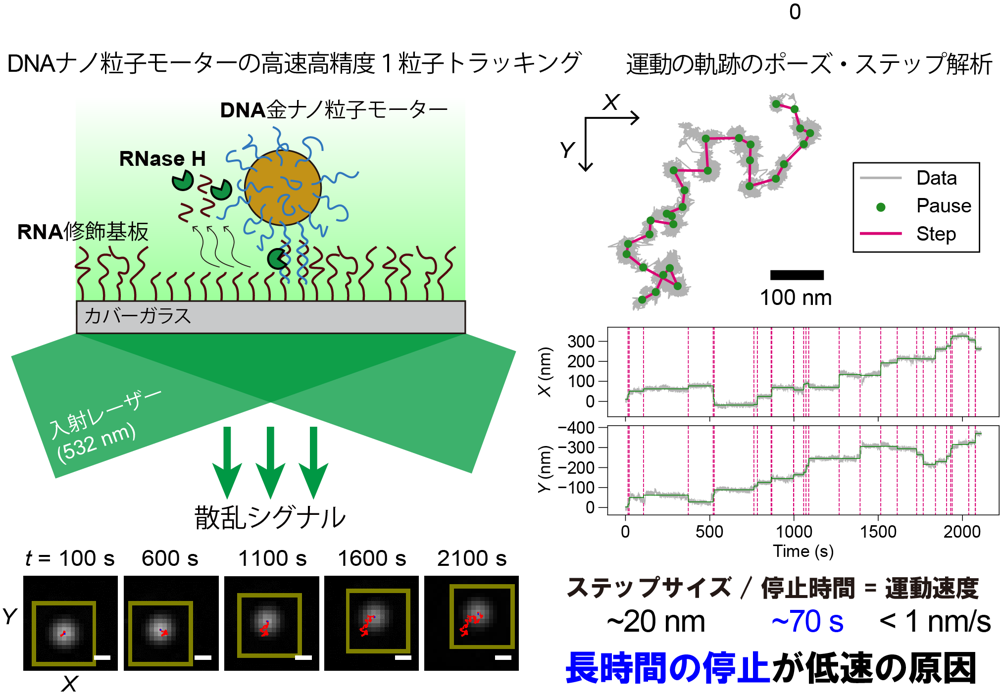
図1 高速高精度1粒子トラッキング実験により、長時間の停止が低速の原因であることを解明
高速高精度1粒子トラッキングの結果、DNAナノ粒子モーターは一定速度で連続的に運動するのではなく、モータータンパク質と同様に、停止(ポーズ)と瞬間的な移動(ステップ)を繰り返しながら運動するポーズ・ステップ運動を行うことが明らかとなりました(図1右)。また、運動速度が遅いのは、停止の時間が約70秒と、モータータンパク質に比べて非常に長いためであることも明らかとなりました。
運動の停止中はDNA/RNA二重鎖の形成、RNase Hの結合、RNAの分解といった化学反応素過程が進行し(図2左下、速度論モデル)、その中でもRNase Hの結合がボトルネック過程であると特定されました。そこで、RNase Hの結合過程を迅速化するため、RNase H濃度を増加させた実験を行ったところ、停止の時間が約0.2秒まで短縮し、運動速度はモータータンパク質に匹敵する約100 nm/sまで高速化しました。しかしながら、RNase Hが高濃度の条件では、運動速度が向上する一方で走行距離が短くなってしまうというトレードオフが生じることが明らかとなりました。
次に、このトレードオフが生じる原因を解明するため、運動を再現するシミュレーションを開発しました(図2左)。このシミュレーションは、化学反応素過程とナノ粒子の幾何学モデルを組み合わせたもので、DNAナノ粒子モーターのポーズ・ステップ運動や運動速度のRNaseH濃度依存性を定量的に再現することができました。また、RNase Hが高濃度の条件では、運動のボトルネック過程がRNase Hの結合からDNA/RNAの二重鎖形成に切り替わることが明らかとなりました。さらに、ボトルネック過程の切り替わりにより、モーターが基板から脱離しやすくなって走行距離が短くなることが明らかとなりました。
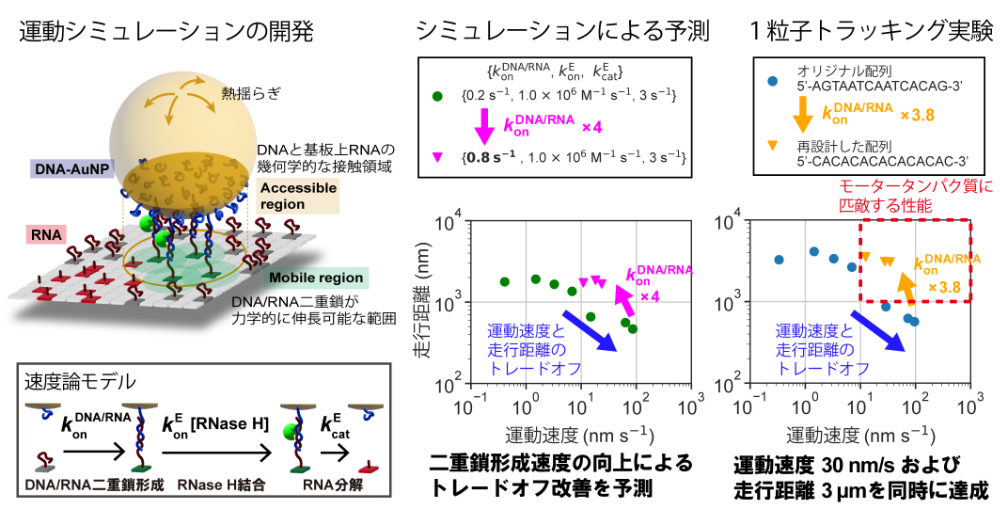
図2 シミュレーションによる予測に基づきDNA塩基配列を再設計し、性能向上に成功
そこで、シミュレーションの化学反応素過程の速度パラメーターを変化させ、運動速度と走行距離が両立する条件の探索を行いました。その結果、DNA/RNAの二重鎖形成の速度を4倍に増加させるとトレードオフが発生せず、高い運動速度と長い走行距離が両立可能と予測されました(図2中央▼)。この予測を基に、DNA/RNAの二重鎖形成速度を高める新しいDNA/RNA配列を設計しました。新たに設計した配列では、GC含有量(*3)の増加と反復配列の導入により、二重鎖形成速度が3.8倍向上しました。このDNA/RNA配列を用いてモーターを作製し、高速高精度1粒子トラッキング実験を行ったところ、シミュレーションの予測と一致する結果が得られ、30 nm/sの運動速度と3 μmの走行距離が同時に実現されました(図2右▼)。この性能は天然のモータータンパク質に匹敵し、ナノサイズの人工分子モーターとしては過去最高となります。
3. 今後の展開・この研究の社会的意義
等方的な球状の金ナノ粒子を構成部品とするDNAナノ粒子モーターは、動きの方向制御に原理的な限界があり、完全な一方向運動の実現が困難という欠点を持ちます。そこで現在は、異方的な形状を持つ金ナノロッドで構成されるDNAナノロッドモーターにより、高い運動速度と長い走行距離に加え、完全な一方向運動を実現する研究に取り組んでいます。
人工分子モーターは、使用できる部品の種類が多く設計の自由度が高い、熱安定性が高い、水以外の有機溶媒中でも働けるといった、モータータンパク質が持たない多くの利点を有します。モータータンパク質に匹敵する性能を持つ人工分子モーターの開発は、生体機能を模倣し凌駕する人工分子システムの実現に寄与し、ナノテクノロジーの発展に貢献する成果です。高い運動速度、長い走行距離、高い一方向性を両立する人工分子モーターを実現することで例えば、人工分子モーターの動きで演算を行う分子コンピューターや、感染・疾患分子を人工分子モーターの動きで高感度に検出する検査システムの実現が期待されます。
4. 用語解説
*1)モータータンパク質:タンパク質により構成される分子モーター。ATP分子の分解に伴う化学エネルギーを運動エネルギーに変換し、一方向運動を実現する。
*2)ATP(アデノシン三リン酸)分子:分解されることで、生命活動に必要な化学エネルギーを生み出す、生体内エネルギー通貨とも呼ばれる分子。
*3)DNA(デオキシリボ核酸)分子:アデニン(A)、チミン(T)、シトシン(C)、グアニン(G)の塩基、糖、リン酸から構成され、塩基配列(A、T、G、Cの並び方)に生体内の遺伝情報が内包される生体分子。塩基間の相補的な水素結合により、二重らせん構造を形成する。
*4)ボトルネック過程:ある反応において最も時間のかかる過程。律速段階とも呼ばれる。
*5)1粒子トラッキング:顕微鏡を用いて一つの粒子を直接イメージングし、その運動の軌跡を追跡する手法。
*6)Burnt Bridge型ブラウンラチェット:レール分子を燃料として分解することにより、退路を断ちながら熱運動で前進する分子モーター。退路を断つことにより後退運動を抑制し、本来方向性を持たない熱ゆらぎによるブラウン運動を前進方向に整流する。
5. 論文情報
掲載誌:Nature Communications
論文タイトル:”Rational engineering of DNA-nanoparticle motor with high speed and processivity comparable to motor proteins”(生体分子に匹敵する高速・高プロセシビティのDNAナノ粒子モーターの合理的性能向上)
著者:Takanori Harashima, Akihiro Otomo, Ryota Iino
掲載日:2025年1月16日(オンライン公開)
DOI:10.1038/s41467-025-56036-0
6. 研究グループ
分子科学研究所
7. 研究サポート
本研究は、MEXT 科学研究費助成事業 新学術領域研究(研究領域提案型)「発動分子科学」(18H05424)、JSPS 科学研究費助成事業 学術変革領域研究(A)(公募研究)「分子サイバネティクス」(23H04434)、「メゾヒエラルキーの物質科学」(24H01732)、科学技術振興機構(JST)ACT-X「生命と情報」(JPMJAX24LE)、JSPS 科学研究費助成事業 若手研究(23K13645)、公益財団法人 津川モーター研究財団 2023年度研究助成の支援の下で実施されました。
8. 研究に関するお問い合わせ先
原島崇徳(はらしま たかのり)
分子科学研究所/総合研究大学院大学 助教
飯野亮太(いいの りょうた)
分子科学研究所/総合研究大学院大学 教授
9. 報道担当
自然科学研究機構 分子科学研究所 研究力強化戦略室 広報担当
総合研究大学院大学 総合企画課 広報社会連携係