インスリンの働きを高める脳から骨格筋までの経路を解明し、肥満・糖尿病の予防と治療に期待
2017-12-15 生理学研究所
内容
| レプチンは脂肪細胞から分泌されるホルモンであり、視床下部腹内側核に作用して骨格筋での糖の取込みを促進し、糖尿病を防ぎます。しかし、レプチンが、視床下部腹内側核に作用した後、骨格筋において糖の取込みを促進する機構は不明でした。今回、自然科学研究機構生理学研究所の箕越靖彦教授、徳島大学大学院医歯薬学研究部の志内哲也准教授、昭和女子大学江崎治教授、静岡大学三浦進司教授らの共同研究グループは、レプチンが視床下部腹内側核に作用した後、交感神経とβ2アドレナリン受容体を活性化し、インスリン作用を増強することによって、骨格筋への糖の取込みを促進することを明らかにしました。 本研究結果は、2017年11月9日にScientific Reports誌に掲載されました。 |
今回の発見
- 脂肪細胞から分泌されるホルモン・レプチンが、視床下部腹内側核に作用して骨格筋に投射する交感神経を活性化し、β2アドレナリン受容体を活性化することによって、骨格筋においてインスリンの働きを増強し、結果、糖の取り込みを促進することが分かりました。
- 交感神経は、血圧や心拍数を調節することが知られています。本研究は、それだけでなく、骨格筋において糖の取込みを促進することが分かりました。
概要
私達の体には、レプチンと呼ばれるホルモンがあり、脂肪細胞で産生されて血中に分泌され、脳に作用を及ぼします。レプチンは、主に視床下部の神経細胞(ニューロン)に作用を及ぼして、食欲を抑えるとともに、末梢組織において脂肪酸酸化や糖の利用を高めることで、熱産生を促進します。また、骨格筋などの末梢組織においてインスリンの作用を高め、その結果、糖の取込みを促進し、血糖値の上昇を防ぎます。レプチンによる抗糖尿病作用がヒトにおいても重要であることは、レプチンの産生場所である脂肪細胞が消失する病気「脂肪萎縮症」において、血中レプチン濃度が低下してインスリンの働きが低下し、その結果、重症の糖尿病を発症することからも明らかです。脂肪萎縮症では、膵臓からインスリンはたくさん分泌されるのですが、骨格筋においてインスリンの働きが低下するため、インスリンによる治療もほとんど効果がありません。ところがレプチンを投与すると、この病気の糖尿病が著しく改善することが明らかとなり、現在では、この疾患の治療薬として世界中で利用されようになりました。
箕越教授の研究グループは、これまで、レプチンが視床下部腹内側核の神経細胞に直接働き、骨格筋、心臓、そして熱産生組織として知られる褐色脂肪組織においてインスリンの働きを高め、糖の利用を促進すること、加えて骨格筋ではAMP-kinase(AMPK)を活性化することによって脂肪酸酸化を促進することを報告してきました(Diabetes 1999, 1999, 2009, 2013, 2017; Nature 2002)。しかし、レプチンが視床下部腹内側核に作用した後、どのようにして上記の組織において糖の取込みを促進するかは、不明でした。このメカニズムを解明することは、新しい糖尿病治療の開発にもつながる可能性があります。とりわけ、骨格筋は個体に占める割合が大きいため、骨格筋でのメカニズムを明かにすることが重要でした。
本研究グループは、視床下部腹内側核神経細胞にレプチンが作用すると、交感神経が活性化することから、交感神経から分泌されるノルアドレナリンの受容体、特に骨格筋に多く発現するβ2アドレナリン受容体に着目しました。研究グループは、まず、βアドレナリン受容体を全て欠損したマウス(β-lessマウス)を準備して、そのマウスの視床下部腹内側核にレプチンを投与し、骨格筋を含む末梢組織での糖の取込みを調べました。その結果、レプチンを視床下部腹内側核に投与すると、対照群のマウスでは、骨格筋、心臓、褐色脂肪組織において糖の取込みが促進しましたが、β-lessマウスでは糖の取込みが増加しませんでした。肥満の原因となる白色脂肪組織では、糖の取込みは対照群、β-lessマウス共に変化しませんでした。また、レプチンを視床下部腹内側核に投与すると、骨格筋に投射する交感神経の活動が高まることも分かりました。
次に、骨格筋のβ2アドレナリン受容体が、糖の取込みに直接関与しているか否かを調べるため、電気穿孔法(エレクトロポレーション法)を用いて、β-lessマウスの片足の一部の骨格筋にβ2アドレナリン受容体を強制的に発現させ、レプチンによる糖の取込みを調べました。その結果、β2アドレナリン受容体を発現させた骨格筋においてのみ、レプチンによる糖の取込みが回復しました。
以上の実験結果から、レプチンが視床下部腹内側核に作用すると、骨格筋に投射する交感神経の活動が高まり、交感神経末端からノルアドレナリンが分泌されて、骨格筋内に存在するβ2アドレナリン受容体を活性化し、糖の取り込みを促進すると考えられます。この作用は白筋よりも、姿勢の維持など関わる赤筋で強く、これは、レプチンが赤筋に投射する交感神経の活動をより強く促進するためによると考えられます。また、β2アドレナリン受容体を強制的に発現させた骨格筋では、糖の取込みが促進すると同時に、骨格筋内のインスリンシグナルが増強していました。このことから、交感神経から分泌されたノルアドレナリンが、β2アドレナリン受容体を介して骨格筋におけるインスリン作用を増強し、これによって糖の取込みを促進することが示唆されます。褐色脂肪組織と心臓への糖の取込み促進作用も同様の機構によって糖の取込みが促進する可能性があります。
交感神経は、血圧や心拍数を調節することが知られています。本研究は、これらの作用に加えて、骨格筋のインスリン作用を増強し、糖の取込みを増加させることが分かりました。今回の発見は、肥満や糖尿病の病因解明、新しい治療法の確立に繋がることが期待されます。
本研究は、日本学術振興会 科学研究費補助金基盤研究B(代表研究者:箕越靖彦教授)、若手研究B(代表研究者:志内哲也)、および科学技術振興機構の戦略的創造研究推進事業(JST-PRESTO)「生体における動的恒常性維持・変容機構の解明と制御」における研究課題「中枢・末梢・時間を統合した代謝生理学的ネットワーク機能の解明」(研究代表者:志内哲也)の支援を受けて行われました。
用語解説
- レプチン
脂肪細胞から分泌されるホルモン。レプチンは、視床下部に作用することによって、摂食を抑制するとともに、エネルギー消費を促進する。また、同時に糖や脂肪酸の利用を促進することによって、抗糖尿病作用を起こす。 - 視床下部腹内側核
視床下部に存在する神経核の一つ。電気刺激すると摂食抑制が引き起こされることから、満腹中枢とも呼ばれる。視床下部腹内側核神経細胞にはレプチン受容体が発現しており、レプチンは、視床下部腹内側核神経細胞を介して骨格筋など末梢組織での糖の取込みを促進する。 - β-lessマウス
βアドレナリン受容体には、β1、β2、β3受容体の3つのサブタイプがある。β-lessマウスは、これら3種のβアドレナリン受容体を全身ですべて欠損したマウスである。
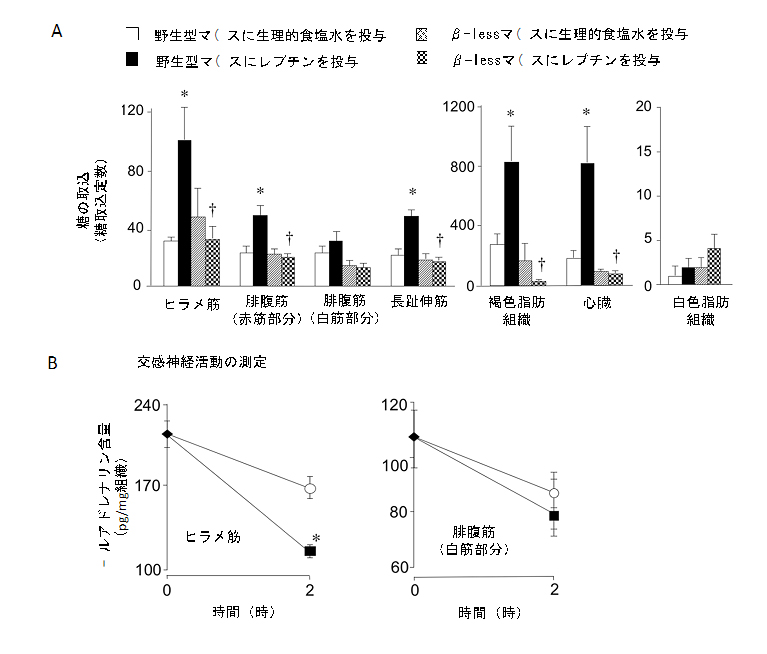
図1 レプチンを視床下部腹内側核に投与すると、骨格筋など末梢組織において糖の取込みが増加するが、βアドレナリン受容体欠損マウスでは増加しない。
解説
A レプチンをマウス視床下部腹内側核に投与した時の、末梢組織における糖取込みの変化。対照群では、骨格筋(赤筋)[ヒラメ筋(赤筋)、腓腹筋(赤筋部分)、長趾伸筋(混合筋)]、褐色脂肪組織、心臓において糖の取込みが促進した。しかし、β-lessマウスでは促進しなかった。白色脂肪組織では糖の取込みはレプチンによって変化しなかった。
B ノルアドレナリン含量の減少速度に基づく交感神経活動の測定。ノルアドレナリン含量の減少が早いほど、その組織において交感神経の活動が活発であることを示す。レプチンをマウス視床下部腹内側核に投与すると、ヒラメ筋に投射する交感神経の活動が亢進した。しかし、腓腹筋の白筋部分では変化しなかった(糖の取込みと相関する)。
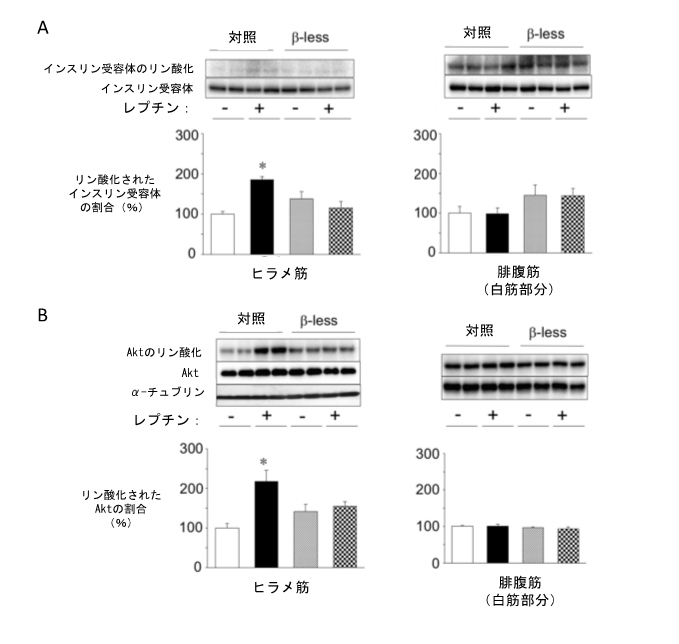
図2 レプチンを視床下部腹内側核に投与すると、インスリン受容体とインスリンシグナル分子Aktが活性化するが、βアドレナリン受容体欠損マウスでは増加しない。
解説
レプチンをマウス視床下部腹内側核に投与した時の、ヒラメ筋(赤筋)と腓腹筋(白筋部分)におけるインスリン受容体(A)とインスリンシグナル分子Akt(B)の活性の変化。写真の黒いバンドは、(A)リン酸化されたインスリン受容体、インスリン受容体、(B)リン酸化されたAkt、Aktのタンパク質量を示す。また、リン酸化はこれらの分子が活性化していることを示す。
レプチンを視床下部腹内側核に投与すると、対照群では、インスリン受容体とAktがヒラメ筋(赤筋)において活性化した。しかし、腓腹筋(白筋部分)では活性化しなかった。β-lessマウスでは、ヒラメ筋においてもインスリン受容体とAktは活性化しなかった。
図3 β2アドレナリン受容体をβアドレナリン受容体欠損マウスの骨格筋に強制発現させると、レプチンによる糖の取込み、インスリンシグナル分子の活性化が回復する。
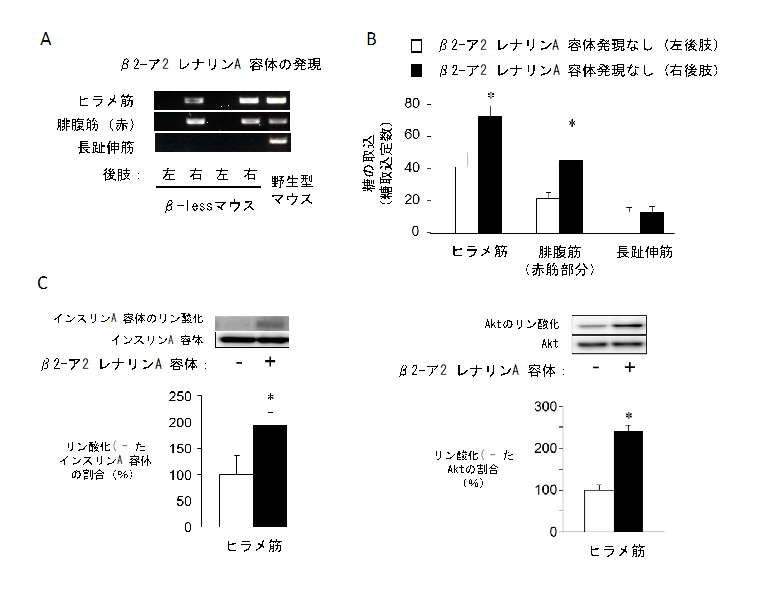
解説
A β-lessマウスの右後肢の一部骨格筋にβ2アドレナリン受容体を強制的に発現させた。ヒラメ筋と腓腹筋(赤筋部分)にβ2アドレナリン受容体を発現させ、同じ右後肢の長趾伸筋には発現させなかった。
B β2アドレナリン受容体を強制発現させると、レプチンによる糖取込み促進作用が回復した。しかし、β2アドレナリン受容体を発現させなかった長趾伸筋では回復しなかった。
C β2アドレナリン受容体を強制発現させると、レプチンによるインスリン受容体(左図)とAkt(右図)のリン酸化亢進作用が回復した。
この研究の社会的意義
交感神経は、血圧や心拍数を調節することが知られています。本研究は、これらの作用に加えて、骨格筋のインスリン作用を増強し、糖の取込みを増加させることが分かりました。今回の発見は、2型糖尿病の原因と言われるインスリン抵抗性の発症メカニズム、またその治療法の開発に貢献すると考えられます。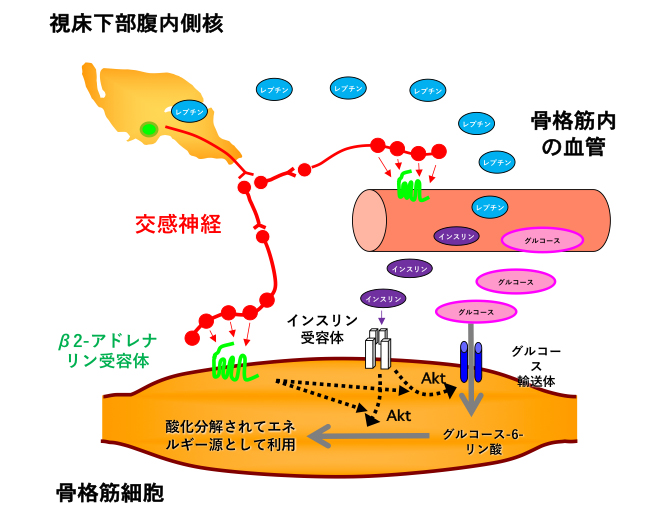
解説
脂肪細胞から血中に分泌されたレプチンは、視床下部腹内側神経細胞に作用し、交感神経を活性化する。活性化した交感神経はノルアドレナリンを分泌して、骨格筋細胞及び血管のβ2-アドレナリン受容体を活性化する。β2-アドレナリン受容体は、インスリンによるインスリン受容体とその細胞内シグナル分子であるAktをリン酸化して活性化する。活性化したインスリンシグナルは、骨格筋細胞への糖(グルコース)の取込みを促進する。骨格筋細胞に取り込まれたグルコースは酸化分解され、運動や熱産生のエネルギー源として利用される。
論文情報
Induction of glucose uptake in skeletal muscle by central leptin is mediated by muscle β2-adrenergic receptor but not by AMPK
Shiuchi T, Toda C, Okamoto S, Coutinho EA, Saito K, Miura S, Ezaki O, Minokoshi Y. Scientific Reports. 2017年 11月9日掲載
お問い合わせ
<研究について>
自然科学研究機構 生理学研究所 生体機能調節研究領域
生殖・内分泌系発達機構研究部門 教授 箕越 靖彦 (ミノコシ ヤスヒコ)
<広報に関すること>
自然科学研究機構 生理学研究所 研究力強化戦略室
リリース元
自然科学研究機構 生理学研究所
関連部門
生殖・内分泌系発達機構研究部門
関連研究者
教授 箕越 靖彦 MINOKOSHI, Yasuhiko