関節リウマチに対する再生医療開発の可能性
2022-03-31 東京医科歯科大学,日本医療研究開発機構
ポイント
- 関節リウマチにおいて炎症性サイトカインを産生しているCD34+THY1+滑膜線維芽細胞サブセット※1が、骨芽細胞や軟骨細胞への高い分化能を有することを突き止めました。
- サブセット表面マーカーの1つであるTHY1が滑膜線維芽細胞の骨芽細胞分化能を促進していることを明らかにしました。
- CD34+THY1+滑膜線維芽細胞サブセットやそのTHY1シグナルを治療標的とした、抗炎症のみならず関節組織再生を目指した関節リウマチの新しい再生医療への応用が期待できます。
概要
東京医科歯科大学大学院医歯学総合研究科膠原病・リウマチ学分野の保田晋助教授、故・溝口史高元講師、野田聖二特任助教の研究グループは、日本医療研究開発機構(AMED)免疫アレルギー疾患実用化研究事業の委託を受け(2020—22年度:関節リウマチ関連線維芽細胞サブセットを標的とした新規治療戦略の開発)、本学再生医療研究センター、本学運動器外科学分野グループ、日本鋼管福山病院、苑田会人工関節センター病院との共同研究で、関節リウマチや変形性関節症における滑膜線維芽細胞の3つのサブセットのうち、CD34+THY1+滑膜線維芽細胞が高い骨芽細胞・軟骨細胞分化能を有することを突き止めました。その研究成果は、国際科学誌Arthritis Research & Therapyに、2022年2月15日にオンライン版で発表されました。
研究の背景
関節リウマチは、免疫の異常により全身の関節に腫れや痛みを生じ(炎症)、骨や軟骨といった関節組織の破壊により変形をきたす疾患です。関節を形成する滑膜とよばれる組織が炎症の首座であり、病理的には滑膜組織にリンパ球などの免疫細胞が浸潤し、滑膜線維芽細胞が増生しています。近年、関節リウマチの治療法は大きく進歩し、免疫細胞やそれらが産生するサイトカインを標的とした分子標的薬が多数開発され、臨床で用いられています。一方、これらの分子標的薬を用いても関節炎を完全には抑えられない患者様がいること、過度な免疫抑制による感染症が問題となっています。また、一度破壊された関節組織は修復できず、外科手術などなしでは変形が永続的に残ってしまうことも問題となっています。以上から、関節リウマチ治療におけるアンメットニーズは従来の抗リウマチ薬で効果不十分な患者さんに過度な免疫抑制をきたすことなく有効であり、破壊された関節組織を修復できるような新しい治療法の開発です。
東京医科歯科大学大学院医歯学総合研究科膠原病・リウマチ内科学分野の研究グループは、現在の関節リウマチ治療の限界を打破するべく、AMED免疫アレルギー疾患実用化研究事業の委託のもとに滑膜線維芽細胞を標的とした治療戦略の開発を目指しています(2020—22年度:関節リウマチ関連線維芽細胞サブセットを標的とした新規治療戦略の開発)。患者由来滑膜線維芽細胞のシングルセルRNAシークエンシング解析により、滑膜線維芽細胞は表面マーカーであるCD34およびTHY1の発現パターンから、増殖能、浸潤能、炎症性サイトカイン産生能などの機能の異なる3つの主要なサブセット(CD34–THY1–、CD34–THY1+、CD34+THY1+)に分かれることが最近明らかとなりました(図1、Mizoguchi F. et al. Nat commun 2018)。CD34–THY1+サブセットは変形性関節症に比べ関節リウマチで増加しており、関節破壊に関わる浸潤能が高く、CD34+THY1+サブセットは炎症性サイトカインを高産生することから、どちらも関節リウマチの病態への関与が想定されていました。一方、以前から滑膜線維芽細胞には間葉系幹細胞※2様の多分化能が存在することが報告されており、関節リウマチの再生医療への応用が期待されていました。
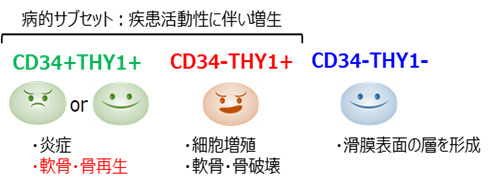
図1 関節リウマチ滑膜線維芽細胞サブセット
そこで本研究グループは、新たに同定された滑膜線維芽細胞サブセットの骨芽細胞や軟骨細胞への間葉系幹細胞様の分化能を比較検討し、骨・軟骨分化能に重要なシグナル分子を同定することを試みました。
研究成果の概要
本学及び協力医療機関で行われた70名(関節リウマチ患者:18名、変形性関節症患者:52名)の膝人工関節置換術の際に、患者様の同意を得た上で提供された滑膜組織を使用して研究を行いました。滑膜組織から酵素処理をして滑膜線維芽細胞を単離し、セルソーターを用いてCD34、THY1の発現に応じて3つの滑膜線維芽細胞サブセットに分離しました。分離した3つのサブセットにおける間葉系幹細胞に特徴的な表面分子の発現をフローサイトメトリーで調べました。また、分離した各滑膜線維芽細胞サブセットを骨芽細胞、軟骨細胞および脂肪細胞へ分化させるための専用培地で3週間培養し、それぞれの細胞への分化について組織染色や定量的PCRで評価しました。
間葉系幹細胞の表面マーカーの発現について評価したところ、骨芽細胞分化に優れた間葉系幹細胞において発現している分子(THY1、CD73)は、CD34+THY1+サブセットにおいて強く発現しており、その傾向は、RAとOAいずれにおいても同様であることが判明しました(図2※3)。次に、骨芽細胞への分化能に関して骨芽細胞分化による石灰化の形成を赤く染める染色法(アリザリンレッド染色)や骨芽細胞を青く染める染色法(Alkaline phosphatase、ALP染色) にて評価したところ、CD34+THY1+サブセットがRAとOA由来いずれでも、3つのサブセットの中で優れていることがわかりました(図3)。組織学的な評価に加えて、骨芽細胞分化を促進する転写因子であるRUNX2や骨芽細胞が分泌するALPのmRNA発現も同サブセットで高値でした。また、軟骨細胞分化能に関しても、各サブセットから形成された軟骨ペレットの大きさと軟骨基質を赤く染める染色法(サフラニンO染色)によって評価したところ、CD34+THY1+サブセットが最も優れていることがわかりました(図3)。また、軟骨基質であるアグリカンのmRNA発現も同サブセットで高値でした。なお、脂肪細胞への分化能に関しては、各サブセットとも同様に低値でした。
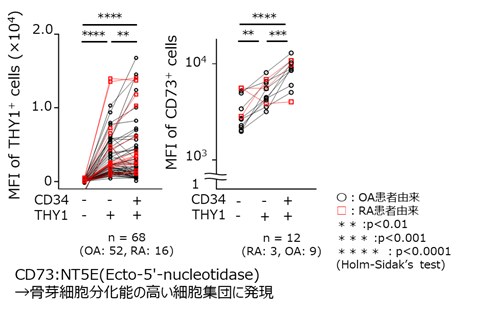
図2 CD34+THY1+サブセットは骨芽細胞分化に促進的な表面分子を高発現していた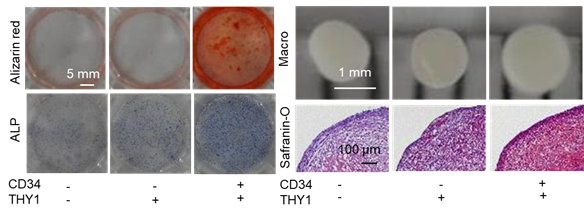
図3 CD34+THY1+サブセットは高い骨芽細胞・軟骨細胞分化能を呈した
滑膜線維芽細胞サブセットの表面マーカーとして用いたTHY1は、細胞質膜に存在するグリコシルホスファチジルイノシトール(GPI)アンカータンパク質の1つであり、間葉系幹細胞の骨芽細胞分化におけるシグナル分子としても報告されています。THY1の発現はCD34+THY1+サブセットで最も高かったことから(図1)、CD34+THY1+サブセットにおける高い骨芽細胞・軟骨細胞分化能にTHY1が関与している可能性が考えられました。このため、滑膜線維芽細胞におけるTHY1をsiRNAによりノックダウンしたところ、骨芽細胞への分化が抑制されることが、組織学的(アリザリンレッド染色、ALP染色)およびRUNX2とALPのmRNA発現の評価によって示されました(図4)。
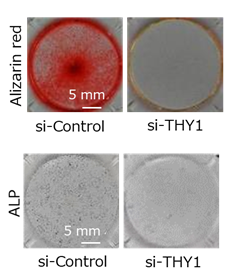
図4 THY1発現抑制は骨芽細胞分化を抑制した
研究成果の意義
本研究によって、最近新たに同定された関節リウマチの滑膜線維芽細胞サブセットのうち、炎症性サイトカインを高産生することから悪玉と考えられていたCD34+THY1+サブセットが、骨・軟骨の修復・再生に関与する善玉サブセットとしても機能しうることが明らかとなりました。また、CD34+THY1+サブセットに高発現するTHY1が、この高い骨・軟骨分化能に関与することもわかりました。本研究は、CD34+THY1+サブセットの高サイトカイン産生能を抑制し、骨・軟骨分化能を高めるような治療薬が、従来の抗炎症のみならず関節再生にも働く新しい抗リウマチ薬となる可能性を示しています。また、CD34+THY1+サブセットにおけるTHY1の発現や機能を制御する薬がこのような治療薬として期待されます。
用語解説
- ※1 サブセット
- 機能的に分類した細胞集団のことである。
- ※2 間葉系幹細胞
- 自己増殖能や間葉系組織(骨、軟骨、脂肪組織)への分化能を有する幹細胞である。変形性関節症では、膝滑膜組織から間葉系幹細胞を単離、培養し再度膝関節に投与することで軟骨再生を試みる治療が行われている。
- ※3 MFI
- Mean fluorescence intensityの略であり、各細胞における、特定の発色パターンで色づけした表面分子の発光強度の平均値である。
論文情報
- 掲載誌
- Arthritis Research & Therapy
- 論文タイトル
- CD34+THY1+ synovial fibroblast subset in arthritic joints has high osteoblastic and chondrogenic potentials in vitro
お問い合わせ先
研究に関すること
東京医科歯科大学大学院医歯学総合研究科
膠原病・リウマチ内科学分野 保田 晋助(ヤスダ シンスケ)
報道に関すること
東京医科歯科大学 総務部総務秘書課広報係
AMED事業に関すること
日本医療研究開発機構(AMED)
疾患基礎研究事業部 疾患基礎研究課

