2024-04-16 理化学研究所,京都大学iPS細胞研究所
理化学研究所(理研)バイオリソース研究センター(BRC)iPS創薬基盤開発チーム 野中 秀樹 客員研究員、近藤 孝之 客員研究員(京都大学iPS細胞研究所 特定拠点講師)、井上 治久 チームリーダー(京都大学iPS細胞研究所 教授)らの共同研究グループは、ヒト人工多能性幹細胞(iPS細胞)[1]からアストロサイト[2]へ分化誘導する方法の改良と、ハイスループットスクリーニング[3]に適合するiPS細胞由来アストロサイトの表現型解析法の開発に成功しました。
本研究成果は、小児神経疾患・神経変性疾患・脳血管障害など多様なアストロサイト関連疾患のモデル構築や治療法開発に貢献すると期待されます。
今回、共同研究グループは、理研BRCに寄託されたヒトiPS細胞から改良した分化誘導法を用いて、均質なアストロサイト集団を作製しました。このアストロサイトをハイスループットスクリーニングに適合する多検体処理が可能な培養プレートに播種(はしゅ)したのち、サイトカイン[4]放出能、遊走[5]機能、オートファジー[6]応答機能、カルシウムシグナル[7]応答といったアストロサイト機能表現型解析を行うためのプラットフォームを開発しました。さらに、この機能表現型解析法を患者さん由来iPS細胞に適用することで、病態表現型の探索にも応用可能であることを示しました。今回開発したヒトiPS細胞由来アストロサイトと解析プラットフォームは、疾患モデルと病態解明研究および治療法開発につながる成果です。
本研究は、科学雑誌『Journal of Cellular and Molecular Medicine』オンライン版(3月20日付)に掲載されました。
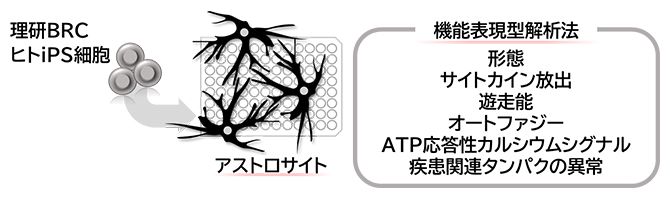
iPS細胞由来アストロサイトを用いた機能表現型解析法
背景
中枢神経は、神経細胞とグリア細胞で構成されています。脳での情報は神経細胞を介して伝達されますが、グリア細胞は神経細胞を補佐する役割を果たしています。グリア細胞の一種であるアストロサイトは、グリア細胞の中でも最も多く存在する細胞種で、サイトカイン分泌、神経成熟、脳内代謝恒常性の維持などさまざまな役割を担っており、脳内環境を維持しています。
そのためアストロサイトの異常は、脳卒中、神経炎症性疾患、神経変性疾患、神経系の発達に関わる疾患などの病気の原因となるため、それらの疾患形成の複雑さを理解し、治療法を開発するためは、アストロサイトの多様な特性を評価することが必要です。
iPS細胞作製技術の導入後、患者さん由来iPS細胞から人体を構成するいろいろな種類の細胞を作製して研究に用いることができるようになり、国内外の研究グループが、ヒトiPS細胞からアストロサイトを分化誘導する方法を開発してきました。しかし、均質なアストロサイトの細胞集団の高純度作製には課題があり、また、安定的かつ多検体処理に適合するスケールで行えるアストロサイトの機能評価系がないため、ヒトiPS細胞から作製したアストロサイトのハイスループットスクリーニングへの適用は困難で、治療法開発への応用は限定的でした。
研究手法と成果
共同研究グループは、アストロサイトに起因する病態の理解や創薬研究につなげるため、ヒトiPS細胞由来のアストロサイトに対して多検体処理に適合するスケールでの機能表現型解析法の構築に挑みました。
理研BRCに寄託されたヒトiPS細胞から、神経系細胞への分化途中の培地組成検討と細胞播種密度の最適化により改良した分化誘導法を用いて均質なアストロサイト集団を作製しました。このアストロサイト集団をハイスループットスクリーニングに適合する多検体処理が可能な培養プレートに播種し、アストロサイトのマーカーであるGFAPやS100βタンパク質を発現していることを確認しました(図1)。
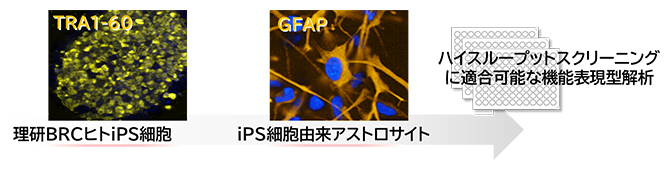
図1 iPS細胞由来アストロサイトの機能表現型解析
理研BRCに寄託されたiPS細胞(左、未分化マーカーであるTRA1-60陽性)からアストロサイト(中央、アストロサイトのマーカーであるGFAP陽性)へ分化誘導をした後に、病態解析や治療法開発において重要となるハイスループットスクリーニングに適合可能な機能表現型解析を開発。
作製したアストロサイト集団は、サイトカインの一種であるインターロイキン(IL)-1βあるいは腫瘍壊死因子(TNF)-αの培地中の添加刺激に応じて、多様なサイトカインを分泌しました。また、播種されたアストロサイト領域の一部に傷をつけて細胞を剝がすことにより、アストロサイトの遊走能を評価することもできました。このように、アストロサイトの機能特性を構築した評価系における数値変化を表現型として比較することで、生体内における神経炎症応答をモデル化して解析することができます。
次に、脳の恒常性維持を担うアストロサイトの機能の評価として、刺激応答性カルシウムシグナルを用いた興奮性評価および飢餓やストレスに対するオートファジー応答評価をハイスループットで行うことのできる実験系を構築しました。
さらに、アストロサイト病態を引き起こすアレキサンダー病[8]患者さん由来iPS細胞を含む複数のiPS細胞株でも、これらの機能が同様に評価可能であることが確認されました。これは、今回開発した機能表現型解析法が疾患iPS細胞にも適用可能であり、病態表現型の探索に用いることができることを意味しています。
今後の期待
ヒトiPS細胞から数カ月の培養期間を経て作製されるアストロサイトは、一様な細胞集団を得ることが困難であり、病態解析や化合物スクリーニングへの適用は限定的でした。本研究で開発したヒトiPS細胞由来アストロサイトと解析プラットフォームは、ハイスループットスクリーニングの実験系に適合し、疾患モデルと病態解明研究および治療法開発に貢献することが期待されます。
補足説明
1.人工多能性幹細胞(iPS細胞)
多様な種類の体細胞へ分化する能力を多能性という。多能性を持ち、培養皿内で無限に増やすことができる細胞を多能性幹細胞という。iPS細胞は、成人の血液や皮膚の細胞にOct3、Sox2、Klf4遺伝子などの初期化因子を導入して人工的に作製した多能性を持つ幹細胞である。多能性を維持した未分化状態のマーカーのTRA1-60などが陽性となる。
2.アストロサイト
脳に存在する細胞のうち、血管や神経細胞以外の細胞であるグリア細胞の一種で、脳の環境維持や神経機能調節などさまざまな機能を持つことが明らかになりつつある。グリア線維性酸性タンパク質(GFAP: Glial fibrillary acidic protein)などがマーカーとなる。
3.ハイスループットスクリーニング
スクリーニングとは、目的の活性を持つ化合物を選別すること。ハイスループットスクリーニングとは、ロボットなどを用いて膨大な数の化合物から有用なものを迅速かつ高効率で選別するスクリーニングのこと。多数検体あるいは多数条件の培養細胞を解析できるため、創薬やバイオマーカー研究などで使用されるが、細胞品質の均質性を保って実験のばらつきを最小限に抑えることや、多検体処理に適合した解析手法が必要となる。
4.サイトカイン
細胞同士の情報伝達に関わる、さまざまな生理活性を持つ可溶性タンパク質の総称。免疫関連細胞間の情報伝達の手段として細胞から放出され、免疫システムに関与する。アストロサイトから放出されるサイトカインも、神経機能の維持や神経炎症を介した病態形成に重要な役割を持つ。
5.遊走
細胞などが生体内のある場所から別の場所に移動すること。アストロサイトは、歴史的には生体内で移動することの少ない比較的静的な細胞であると考えられていたが、発達期・神経損傷応答など特定の状況下で遊走することが分かってきた。アストロサイトの遊走とさまざまな病態との関連性が推測されている。
6.オートファジー
細胞が自らの細胞内成分を分解する主要なメカニズム。細胞内のオルガネラ(細胞小器官)やタンパク質などの細胞質成分をオートファゴソーム(小胞)へ取り込み、リソソームで分解する。ストレス時の細胞の生存にも関わり、細胞の恒常性を維持するために不可欠な機能である。アストロサイトのオートファジーの応答性はいろいろな神経疾患と関連することが明らかになりつつある。
7.カルシウムシグナル
細胞質内のカルシウムイオン(Ca2+)の濃度(カルシウム濃度)は約10-7M(mol/L)であり、細胞外液の約10-3Mに対して極端に低く抑えられている。刺激に応じて誘導される細胞質内の急激なカルシウム濃度上昇は、脳神経活動を含む多くの生命現象でシグナル(カルシウムシグナル)として利用される。アストロサイトは、通常低濃度に維持されている細胞内カルシウム濃度を、何らかの刺激やシグナル伝達の結果により急激に上昇させて、細胞内タンパクとの結合変化などを通じて細胞機能を調節する。
8.アレキサンダー病
小児あるいは成人期に、てんかん・進行性の白質脳症・精神運動障害を呈する、難治性神経変性疾患の一つで、現時点で根本治療法はない。アストロサイトの細胞骨格を構成するグリア線維性酸性タンパク質をコードするGFAP遺伝子が、原因遺伝子として同定されている。神経病理学的指標として、ローゼンタール線維が知られており、アストロサイト内のGFAP陽性細胞質内構造物、あるいは電子顕微鏡でグリア細線維に囲まれた高電子密度小体として観察される。
共同研究グループ
理化学研究所 バイオリソース研究センター iPS創薬基盤開発チーム
客員研究員 野中 秀樹(ノナカ・ヒデキ)
(田辺三菱製薬株式会社 創薬本部 ニューロサイエンスユニット 研究員)
客員研究員 近藤 孝之(コンドウ・タカユキ)
(京都大学iPS細胞研究所 特定拠点講師)
チームリーダー 井上 治久(イノウエ・ハルヒサ)
(京都大学iPS細胞研究所 教授)
田辺三菱製薬株式会社 創薬本部 ニューロサイエンスユニット
グループ長 大関 洋光(オオゼキ・ヒロミツ)
研究支援
本研究は、日本医療研究開発機構(AMED)再生・細胞医療・遺伝子治療プロジェクト「次世代医療を目指した再生・細胞医療・遺伝子治療研究開発拠点(研究代表者:髙橋淳、JP23bm1323001)」「レジストリ連携による神経変性疾患iPS細胞コホートの構築と整備(研究代表者:井上治久、JP22bm0804034)」「機能性オルガノイドを用いた運動ニューロン疾患遺伝子治療薬スクリーニング系の確立(研究代表者:井上治久、JP23bm1423014)」「脳細胞ヒト化による神経病態と免疫応答解析の基盤技術開発(研究代表者:井上治久、JP23bm1423012)」、上原記念生命科学財団、日本学術振興会(JSPS)科学研究費助成事業基盤研究(B)「点鼻タウワクチンによる脳内免疫応答の解明とナノ粒子のベクター利用(研究代表者:井上治久、21H02807)」、同基盤研究(C)「患者アストロサイトとハイブリッドマウスによるアルツハイマー病病態の解明(研究代表者:近藤孝之、23K06927)」の助成を受けて行われました。
原論文情報
Hideki Nonaka, Takayuki Kondo, Mika Suga, Ryu Yamanaka, Yukako Sagara, Kayoko Tsukita, Naoko Mitsutomi, Kengo Homma, Ryuta Saito, Fumihiko Miyoshi, Hiromitsu Ohzeki, Masahiro Okuyama, Haruhisa Inoue, “Induced Pluripotent Stem Cells based Assays Recapture Multiple Properties of Human Astrocytes”, Journal of Cellular and Molecular Medicine, 10.1111/jcmm.18214
発表者
理化学研究所
バイオリソース研究センター iPS創薬基盤開発チーム
チームリーダー 井上 治久(イノウエ・ハルヒサ)
(京都大学iPS細胞研究所 教授)
客員研究員 野中 秀樹(ノナカ・ヒデキ)
客員研究員 近藤 孝之(コンドウ・タカユキ)
(京都大学iPS細胞研究所 特定拠点講師)
報道担当
理化学研究所 広報室 報道担当
京都大学iPS細胞研究所(CiRA)国際広報室