2025-02-20 名古屋大学
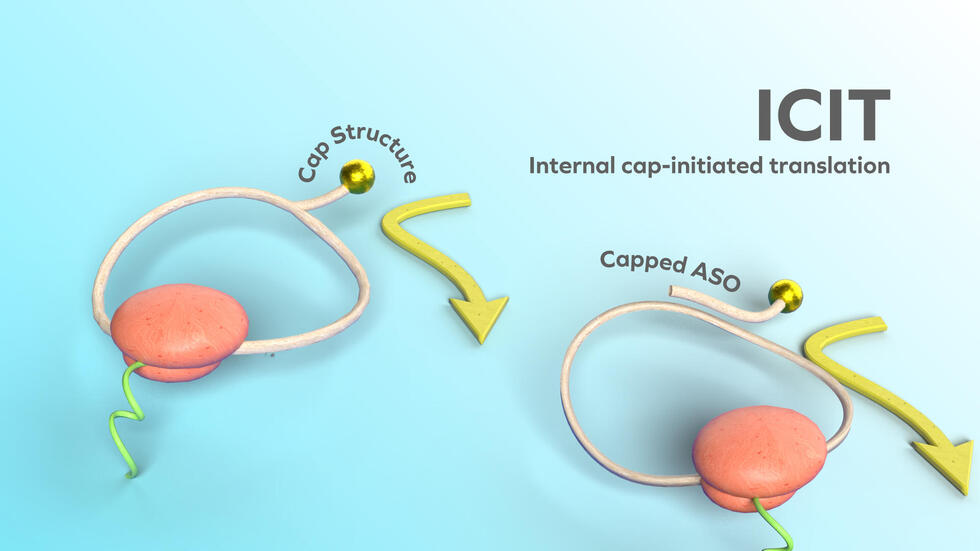
名古屋大学大学院理学研究科の阿部 洋 教授、福地 康佑 博士後期課程学生、中嶋 裕子 研究員、阿部 奈保子 特任准教授の研究グループは、理化学研究所開拓研究本部の岩崎 信太郎 主任研究員、七野 悠一 研究員、東京科学大学 内田 智士 教授との共同研究で、キャップ構造を環状mRNAに結合させることで翻訳を開始できることを見出し、新しい翻訳機構としてinternal cap-initiated translation (ICIT)と命名しました。ICIT機構を用いることで、環状mRNAからの高効率な翻訳や、疾患特異的な翻訳制御が可能になりました。
環状mRNAは直鎖mRNAと比較し、安定性が高く、炎症作用が低いことから、次世代の分子設計として期待されていました。しかしながら、これまでの環状mRNAの設計では、タンパク質合成量が少ないため実用化が困難でした。
今回発見したICIT機構を用いることで、環状mRNAからの高効率なタンパク質合成が可能になりました。さらにICIT機構を利用し、がんをはじめとした病気の細胞や目的組織でのみタンパク質合成が起こるような翻訳反応スイッチを開発し、mRNAの副作用を下げるために有用な技術を開発しました。ICITは生体内で翻訳反応を制御する機構として使われる可能性があり、重要な課題として研究が進むことが期待されます。
本研究成果は、2025年2月19日19時(日本時間)付Nature誌が発行する雑誌『Nature Biotechnology』に掲載されます。
【ポイント】
・鎖の内部にキャップ構造注1)をもつ環状mRNAを設計・合成した。
・独自の分子構造が高い安定性と高い翻訳注2)能を兼ね備えることを証明。
・キャップ構造を持つRNA鎖と環状mRNA注3)が相互作用することで、環状mRNAの翻訳反応を促進する、新たな翻訳促進メカニズムを発見。
・がん細胞などの病気の細胞でのみ翻訳を起こすことができる翻訳スイッチを開発。
◆詳細(プレスリリース本文)はこちら
【用語説明】
注1)キャップ構造
mRNAの5’末端に存在する修飾構造であり、mRNAの翻訳促進や安定性向上など、必要不可欠な構造。
注2)翻訳
mRNAからタンパク質が合成される過程。翻訳能を向上させることがmRNA医薬の発展に重要。
注3)環状mRNA
末端構造を持たない輪っかのような形を持つmRNAである。核酸分解酵素や免疫受容体に認識されにくいといった特徴を持つため、その医薬応用が期待されている。
【論文情報】
雑誌名: Nature Biotechnology
論文タイトル: Internal cap-initiated translation for efficient protein production from circular mRNA
著者: 福地康佑(名古屋大学)、中嶋裕子(名古屋大学)、阿部奈保子(名古屋大学)、木村誠悟(名古屋大学)、橋谷文貴(名古屋大学)、七野悠一(理化学研究所)、Yiwei LIU(名古屋大学)、荻巣亮子(名古屋大学)、杉山里美(名古屋大学)、川口大輔(名古屋大学)、稲垣雅仁(名古屋大学)、Zheyu MENG(名古屋大学)、梶原司琉(名古屋大学)、多田瑞紀(名古屋大学)、内田智士(東京科学大学)、Ting-Ting LI(名古屋大学)、Ramkrishna MAITY(名古屋大学)、河崎泰林(名古屋大学)、木村康明(名古屋大学)、岩崎信太郎(理化学研究所)、阿部洋*(名古屋大学) (*は責任著者)
DOI:10.1038/s41587-025-02561-8
URL:https://www.nature.com/articles/s41587-025-02561-8
【研究代表者】
大学院理学研究科 阿部 洋 教授