2025-11-18 東京農工大学,横浜国立大学,科学技術振興機構
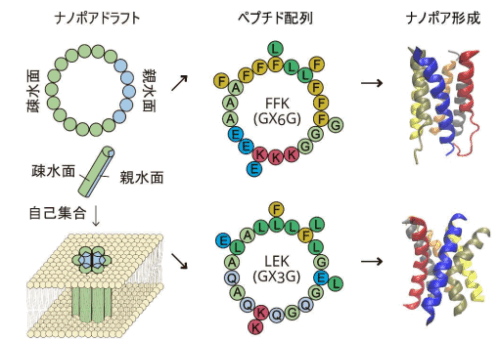
図1:設計したペプチドの配列と構造。天然タンパク質に多く見られる「GAS モチーフ」と呼ばれる特徴的なアミノ酸配列に着目し、それを基にFFKおよびLEKという二種類の人工ペプチドを設計した(。左)脂質から成る膜においては、疎水面が膜に接する外側へ親水面が内側へと自己集合する。(中)FFK と LEK それぞれを構成するアミノ酸。(右)αヘリックスが密に寄り添って、安定した構造を作っている。(Peng et al., ACS Nano 2025 を基に作成)
<関連情報>
- https://www.jst.go.jp/pr/announce/20251118-2/index.html
- https://www.jst.go.jp/pr/announce/20251118-2/pdf/20251118-2.pdf
- https://pubs.acs.org/doi/10.1021/acsnano.5c15080
ヘリックスパッキングモチーフを用いた単一分子検出のためのαヘリカルペプチドナノポアの新規設計 De Novo Design of α-helical Peptide Nanopores for Single-molecule Detection using Helix Packing Motifs
Zugui Peng,Masataka Usami,Ayaka Nakada,Yusuke Sekiya,Shoko Fujita,Batsaikhan Mijiddorj,Izuru Kawamura,and Ryuji Kawano
ACS Nano Published: December 1, 2025
DOI:https://doi.org/10.1021/acsnano.5c15080
Abstract
Nanopore sensing using transmembrane proteins holds great potential for single-molecule detection. The creation of pore-forming proteins is an emerging research direction, and one promising strategy is the bottom-up de novo design of nanopores. However, de novo α-helical nanopores with sufficiently large dimensions to accommodate single-molecule sensing have not been previously reported. Here, we designed and constructed α-helical nanopores based on two helix-packing motifs, GX6G and GX3G, which we named FFK and LEK. Electrical recordings revealed that both FFK and LEK form nanopores in lipid membranes with high conductance. FFK exhibited multiple conductance states, whereas LEK formed more monodisperse pores. Although both nanopores assembled via a stepwise monomer-joining mechanism, the assembly and disassembly dynamics of FFK were significantly faster than those of LEK. We further demonstrated the single-molecule sensing capabilities of both pores, showing that they can detect cyclodextrin derivatives, while LEK could additionally sense poly-l-lysine. Overall, these results demonstrate the feasibility of designing functional α-helical nanopores for nanopore sensing technologies.