2026-03-06 ジョージア工科大学
<関連情報>
- https://research.gatech.edu/feature/nanohydrogels
- https://www.nature.com/articles/s41467-025-66788-4
動的ナノハイドロゲルを用いた腫瘍非依存型薬物送達 Tumor agnostic drug delivery with dynamic nanohydrogels
Stephen N. Housley,Alisyn R. Bourque,Lilya V. Matyunina,Isabel A. Panicker,Elisa Schrader Echeverri,Marrissa Izykowicz,Olivia A. Herrmann,Sebinne Lee,Johana C. Arboleda,Vida Jamali,John F. McDonald,James E. Dahlman & M. G. Finn
Nature Communications Published:07 January 2026
DOI:https://doi.org/10.1038/s41467-025-66788-4
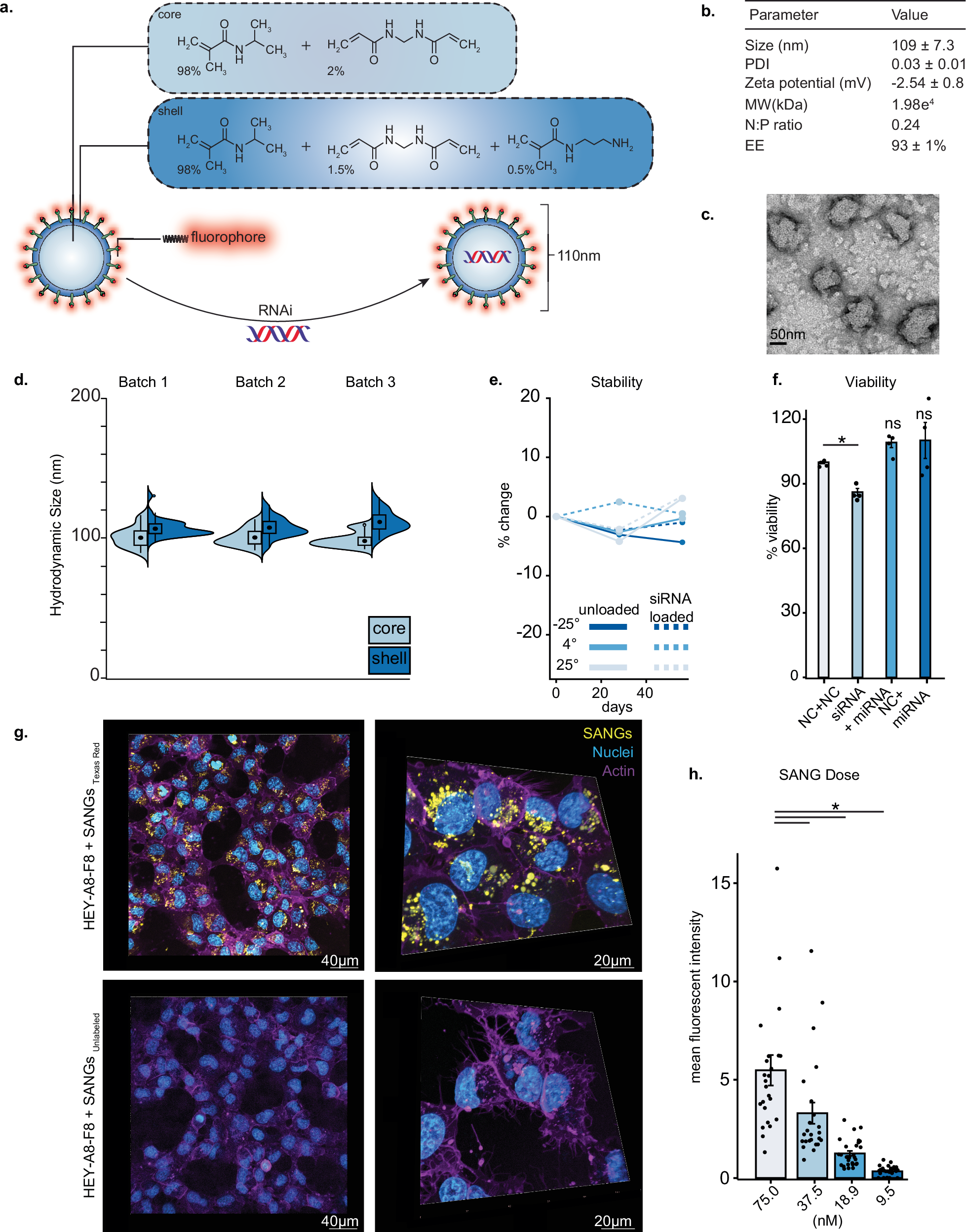
Abstract
RNA interference (RNAi) holds unique potential as a clinically viable modality to pharmacologically regulate oncogenes in sequence-specific manner. However, systemic delivery of RNAi to tumors encounters myriad obstructions, and strategies to overcome such barriers have largely consisted of academic demonstrations with few approaches reaching patients. Here we report the development of a self-agglomerating nanohydrogel (SANGs) platform that selectively localizes to tumor tissue, is efficiently internalized by cancer cells, is agnostic to RNAi payload, and achieves functional suppression of multiple oncogene targets. After intravenous injection, SANGs preferentially accumulate and are retained in primary and metastatic loci in four aggressive cancer models in rodents. SANGs deliver multiple RNAi payloads that significantly suppress oncogene expression and sensitize previously resistant tumors while being safe and well tolerated in simulated clinical applications across three species. We propose, and provide the first direct evidence in support of, a mechanism featuring emergent material properties by which SANGs achieve durable solid-tumor delivery without attachment of cell- or tumor-targeting ligands. Overall, the SANGs platform is an enabling technology for RNAi-based cancer therapeutics and is poised for advanced pharmaceutical development with multiple solid-tumor indications.


