破骨細胞の過剰な活性化を介して多発性骨髄炎が発生する可能性を発見
2021-06-25 広島大学,日本医療研究開発機構
本研究成果のポイント
- メンデル遺伝型マイコバクテリア易感染症(MSMD)で頻繁に認める多発性骨髄炎の発症メカニズムを調査しました。
- MSMD患者の骨髄炎の病巣では骨融解が生じており、破骨細胞が増加していることを発見しました。その原因として、患者では遺伝的な要因でIFN-γの作用が減弱しており、IFN-γによる破骨細胞の抑制が不十分であることを新規に見いだしました。
- 本研究から、破骨細胞の過剰な活性化が、骨髄炎の発症に関与する可能性が示唆されました。将来的に、破骨細胞を標的とした骨髄炎の治療開発に繋がることが期待されます。
概要
メンデル遺伝型マイコバクテリア易感染症(MSMD)(*1)は、細胞内寄生菌(BCG、非結核性抗酸菌、サルモネラ菌など)による感染症を繰り返す非常に稀な遺伝性の免疫の病気です。細胞内寄生菌は通常、IFN-γ(*2)により活性化された食細胞(マクロファージなど)により排除されます。そのため、IFN-γの産生や作用が障害された患者は、MSMDを発症します。これまでにMSMDの原因として、主にIFN-γの産生や作用に関連した11種類の遺伝子における変異が報告されています。そのなかで、IFN-γの刺激を受け取るIFN-γ受容体1(IFN-γR1)や、IFN-γの刺激を伝達するSTAT1の異常により発症するMSMD患者は、多発性骨髄炎(*3)を頻発することが知られていました。しかし、どうして多発性骨髄炎がこれらの患者で頻発するのかは、長い間謎でした。
岡田賢(広島大学大学院医系科学研究科小児科学教授)、小林正夫(同名誉教授)、津村弥来(同研究員)、三木瑞香(広島赤十字・原爆病院小児科)の研究グループは、MSMD患者におけるIFN-γの作用障害が、骨吸収を担う『破骨細胞』(*4)の活性化を介して、多発性骨髄炎を引き起こす可能性を新規に見いだしました(図1)。
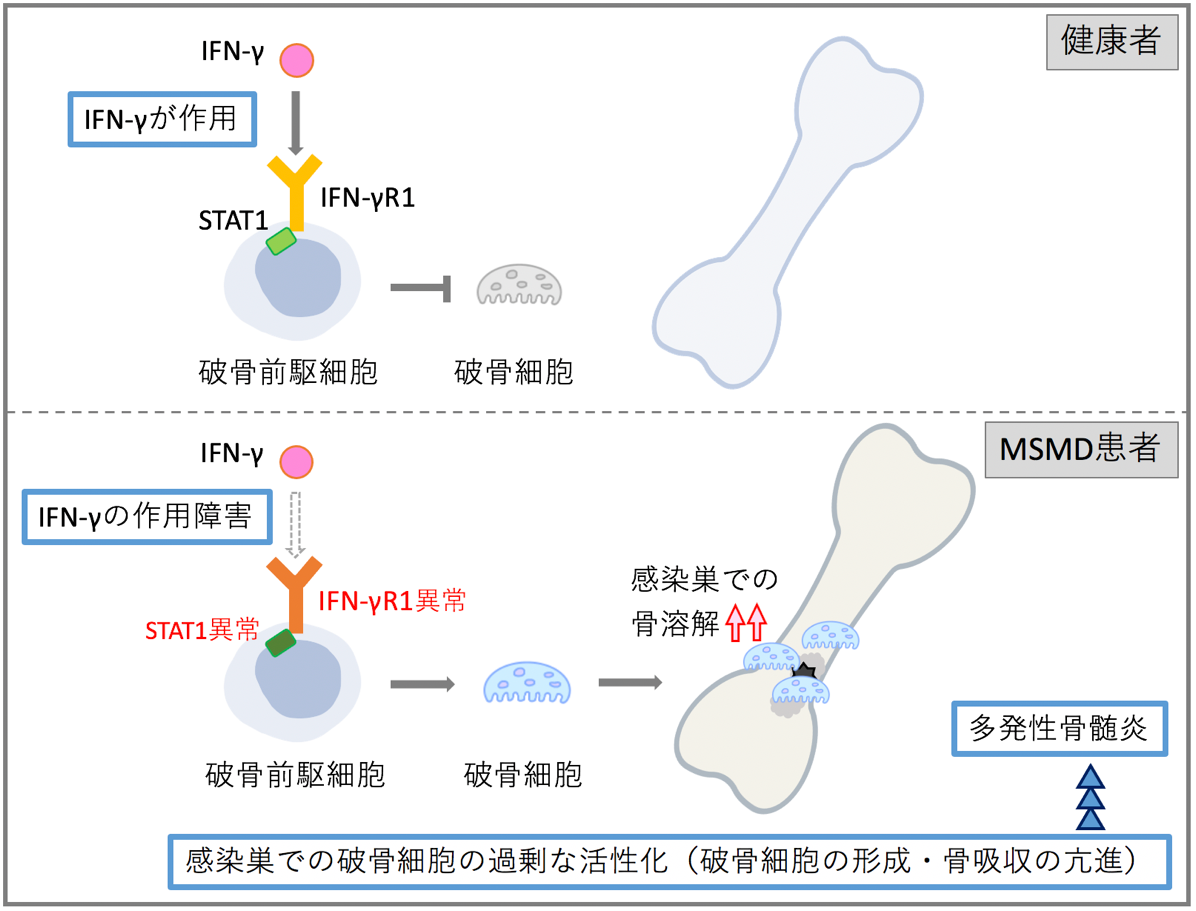 図1 本研究の概要図
図1 本研究の概要図
本研究は、国立研究開発法人日本医療研究開発機構(AMED)難治性疾患実用化研究事業のサポートを受けて実施いたしました。
本研究成果は、2021年6月24日(木)午後8時(日本時間)に「Journal of Allergy and Clinical Immunology」で公開されました。
発表論文
- 論文タイトル
- Enhanced osteoclastogenesis in patients with MSMD due to impaired response to IFN-γ
- 著者
- 津村弥来,三木瑞香,溝口洋子,平田修,西村志帆,玉浦萌,香川礼子,早川誠一,小林正夫,岡田賢*
*Corresponding Author(責任著者) - 掲載雑誌
- Journal of Allergy and Clinical Immunology
- DOI番号
- 10.1016/j.jaci.2021.05.018
背景
メンデル遺伝型マイコバクテリア易感染症(MSMD)は、細胞内寄生菌(BCG、非結核性抗酸菌、サルモネラ菌など)による感染症を繰り返す非常に稀な遺伝性の免疫の病気です。細胞内寄生菌の排除に際して、マクロファージなどの食細胞が重要な役割を果たします。細胞内寄生菌は通常、IFN-γにより活性化された食細胞により排除されます。細胞内寄生菌を取り込んだ食細胞は、IL-12を産生します。IL-12はIL-12受容体β1(IL-12Rβ1)を発現したT細胞、NK細胞に作用し、IFN-γの産生を促します。IFN-γは、IFN-γ受容体1(IFN-γR1)を発現した食細胞を活性化させ、取り込んだ細胞内寄生菌の排除を促します。このように細胞内寄生菌の排除には、IL-12とIFN-γの共同作業が重要であり、IL-12のシグナルに障害がある(IFN-γの産生障害がある)、もしくは食細胞におけるIFN-γの作用障害があることでMSMDを発症します。
IFN-γの作用障害を示すIFN-γR1異常症(*5)あるいはSTAT1異常症(*6)の患者では、多発性骨髄炎を頻発することが知られています。一方、IL-12の作用が障害されたIL-12Rβ1異常症(*7)(二次的にIFN-γの産生が障害される)では、多発性骨髄炎の報告は多くありません(表1)。そこで本研究グループは、多発性骨髄炎とIFN-γの作用障害との関連性に着目して研究に取り組みました(図1)。
表1 MSMD患者における多発性骨髄炎の頻度
| 病気 | 遺伝形式 | 患者 | 頻度 |
|---|---|---|---|
| IFN-γR1異常症 | 常染色体優性 | 59/83 | 71.1% |
| STAT1異常症 | 常染色体優性 | 15/25 | 60.0% |
| IL-12Rβ1異常症 | 常染色体劣性 | 8/136 | 5.9% |
研究成果の内容
IFN-γR1異常症あるいはSTAT1異常症の患者の多発性骨髄炎は、溶骨性変化を示唆するレントゲン所見を示します(図2上)。そこで、多発性骨髄炎の病巣部から得られた組織を詳しく調査したところ、破骨細胞の特異的マーカーであるTRAP(*8)で染色される多核細胞の増加を検出しました(図2下)。TRAP陽性細胞は破骨細胞を反映することから、多発性骨髄炎の病変部には破骨細胞が多数存在しており、破骨細胞による骨を溶かす作用(骨吸収)が亢進していると推測しました。
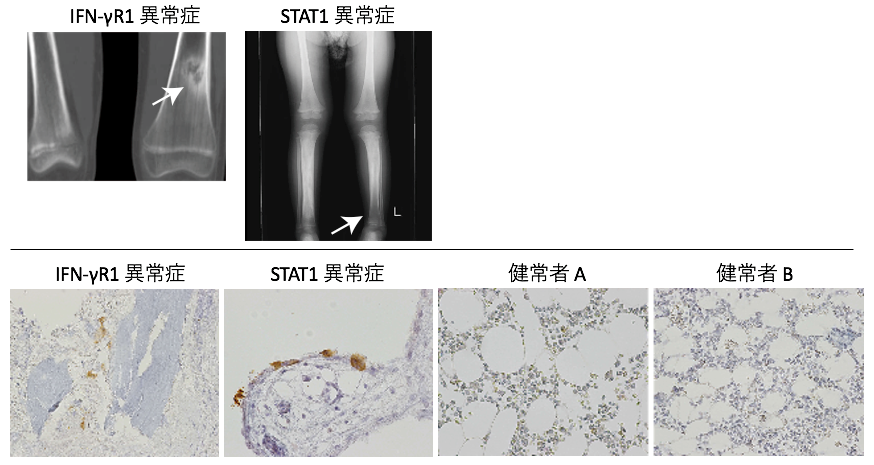 図2 IFN-γシグナル伝達異常症でみられる骨髄炎と破骨細胞の過形成(上)患者の骨髄炎部位で、骨溶解像(矢印で示す部分)を認めました。
図2 IFN-γシグナル伝達異常症でみられる骨髄炎と破骨細胞の過形成(上)患者の骨髄炎部位で、骨溶解像(矢印で示す部分)を認めました。
(下)患者の骨髄炎部位で、TRAP陽性(茶色)の破骨細胞が検出されました。一方で健常者の骨髄では、破骨細胞の存在は確認できませんでした。
破骨細胞は、細胞内寄生菌の排除を担うマクロファージと同じ系統に属する細胞です。過去の研究で、IFN-γが破骨細胞の形成や、その機能(骨吸収)を強力に阻害することが知られていました。そのため本研究グループは、IFN-γの作用が障害されたIFN-γR1異常症やSTAT1異常症では、IFN-γによる破骨細胞の抑制が上手く働かず、感染局所で破骨細胞の増生と、それによる骨吸収が過剰に起こると考えました。その仮説を証明するため、患者、健常者の骨髄細胞から破骨細胞を分化誘導し、それに対するIFN-γの影響を調査しました。
まず、患者、健常者の骨髄細胞は、一定の条件下で破骨細胞に分化することを確認しました。次に、IFN-γにより破骨細胞の分化抑制を試みたところ、健常者では低濃度のIFN-γで抑制されたのに対して、患者では高濃度のIFN-γが抑制に必要でした(図3)。このことから、患者においてIFN-γによる破骨細胞の分化抑制が障害されていることが判明しました。さらに本研究グループは、IFN-γによる破骨細胞の機能抑制(骨吸収の抑制)を調査しました。健常者では、低濃度のIFN-γにより骨吸収の抑制が可能でした。しかし患者では、骨吸収の抑制に多量のIFN-γが必要でした。このことから、患者においてIFN-γによる破骨細胞の骨吸収の抑制が障害されていることが判明しました(図4)。
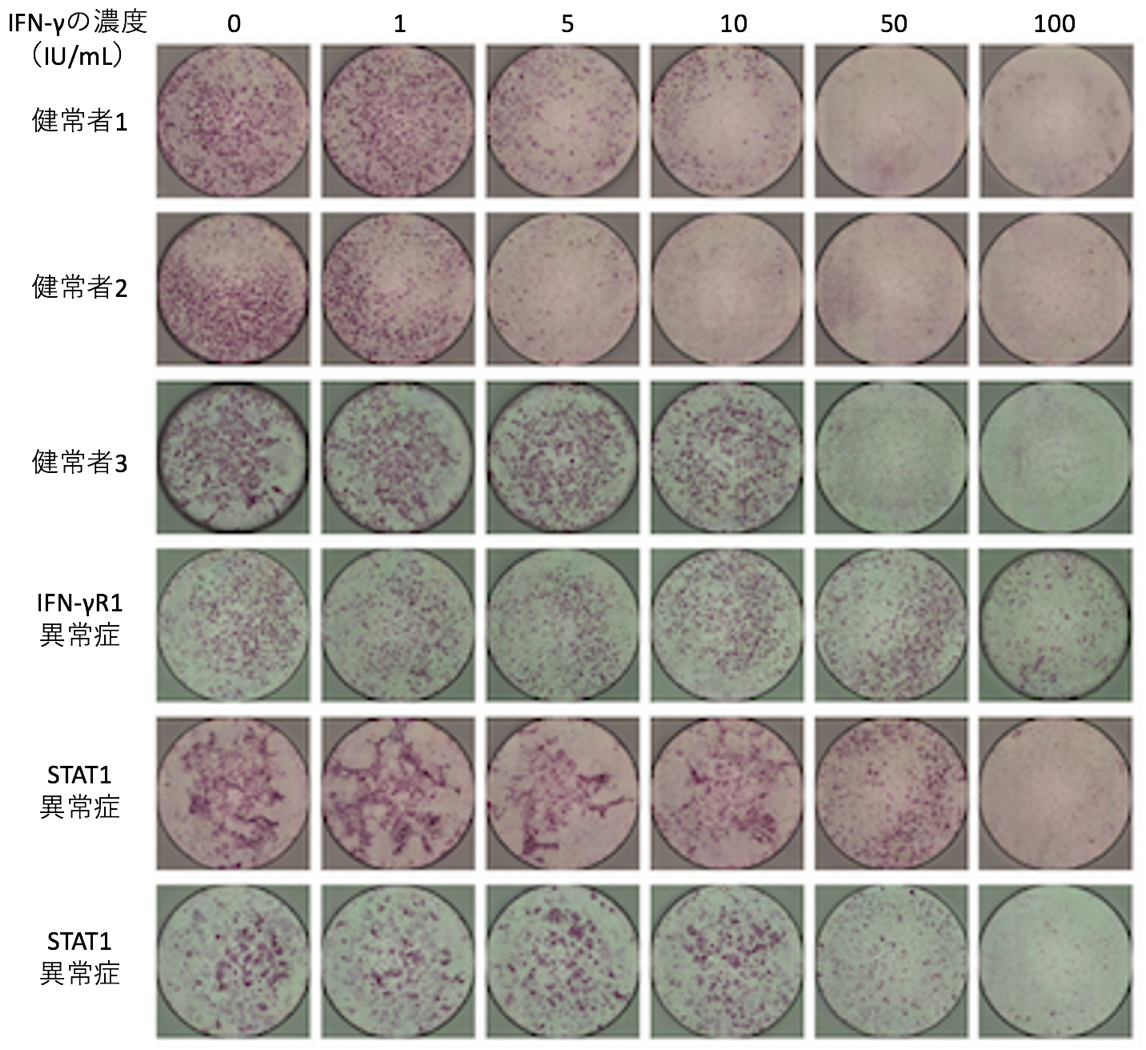 図3 IFN-γによる破骨細胞形成の阻害効果破骨前駆細胞にRANKLとM-CSFを加えて破骨細胞を形成させました(破骨細胞:図中の赤紫)。同時に様々な濃度のIFN-γを加え、IFN-γによる破骨細胞形成への阻害効果を検討しました。IFN-γの濃度が増えるに従って破骨細胞の形成が阻害される様子がわかります。健常者では50 IU/mLのIFN-γの濃度で破骨細胞形成が阻害されていました。一方、IFN-γR1異常症では100 IU/mLのIFN-γを加えても破骨細胞の阻害が不十分でした。STAT1異常症では100 IU/mLのIFN-γで形成が阻害されました。
図3 IFN-γによる破骨細胞形成の阻害効果破骨前駆細胞にRANKLとM-CSFを加えて破骨細胞を形成させました(破骨細胞:図中の赤紫)。同時に様々な濃度のIFN-γを加え、IFN-γによる破骨細胞形成への阻害効果を検討しました。IFN-γの濃度が増えるに従って破骨細胞の形成が阻害される様子がわかります。健常者では50 IU/mLのIFN-γの濃度で破骨細胞形成が阻害されていました。一方、IFN-γR1異常症では100 IU/mLのIFN-γを加えても破骨細胞の阻害が不十分でした。STAT1異常症では100 IU/mLのIFN-γで形成が阻害されました。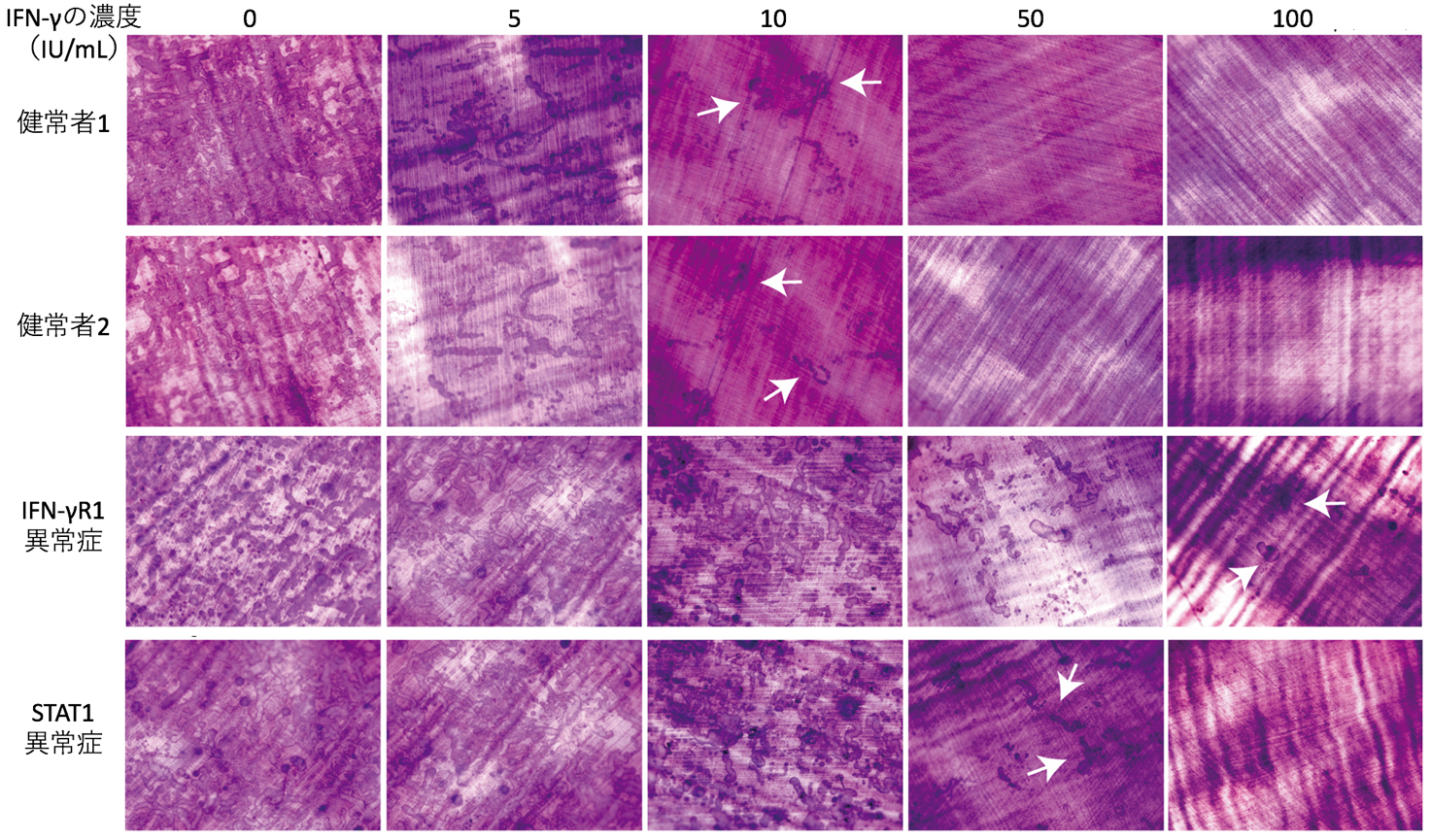 図4 IFN-γによる破骨細胞の骨吸収能に対する阻害効果象牙骨切片の上で破骨細胞を形成させると、破骨細胞は骨切片の上を移動しながら骨を吸収します。そのため骨吸収は、くぼみとして検出されます。IFN-γの濃度が増えるに従って骨吸収が阻害されており、白の矢印で示す濃度まで骨吸収の形跡を認めました。健常者では、50 IU/mLのIFN-γで骨吸収の形跡がみられなくなります。一方、IFN-γR1異常症やSTAT1異常症では、50 IU/mLのIFN-γでも骨吸収の形跡を認めました。
図4 IFN-γによる破骨細胞の骨吸収能に対する阻害効果象牙骨切片の上で破骨細胞を形成させると、破骨細胞は骨切片の上を移動しながら骨を吸収します。そのため骨吸収は、くぼみとして検出されます。IFN-γの濃度が増えるに従って骨吸収が阻害されており、白の矢印で示す濃度まで骨吸収の形跡を認めました。健常者では、50 IU/mLのIFN-γで骨吸収の形跡がみられなくなります。一方、IFN-γR1異常症やSTAT1異常症では、50 IU/mLのIFN-γでも骨吸収の形跡を認めました。
一連の結果から、IFN-γR1異常症やSTAT1異常症では、『IFN-γによる破骨細胞の形成や、骨吸収の抑制』が障害されており、それにより多発性骨髄炎が頻発する可能性が考えられました。
今後の展開
本研究で、IFN-γR1異常症やSTAT1異常症では、IFN-γによる破骨細胞の形成や骨吸収の阻害が不十分であり、そのことが頻回な多発性骨髄炎の原因となる可能性が示唆されました。多発性骨髄炎は、MSMDのみならず自己炎症性疾患などの他の病気でも時に認める病態です。今回の研究をさらに発展させることで、様々な疾患でみられる多発性骨髄炎の病態をあきらかとするとともに、病態に基づく治療法の開発に繋がることが期待されます。
注釈
- (*1)MSMD
-
メンデル遺伝型マイコバクテリア易感染症。細胞内寄生菌(BCG、非定型抗酸菌、サルモネラ菌など)による感染症を頻発する非常に稀な先天性の病気です。細胞内寄生菌は、主に活性化されたマクロファージにより除菌されます。マクロファージの活性化には、IL-12/IFN-γの共同作業が必要で、IFN-γの作用が障害される、あるいはIFN-γの産生が障害されることでMSMDが発症します。これまでに図の黒で示す11種類の遺伝子の障害によりMSMDが発症することが報告されています。
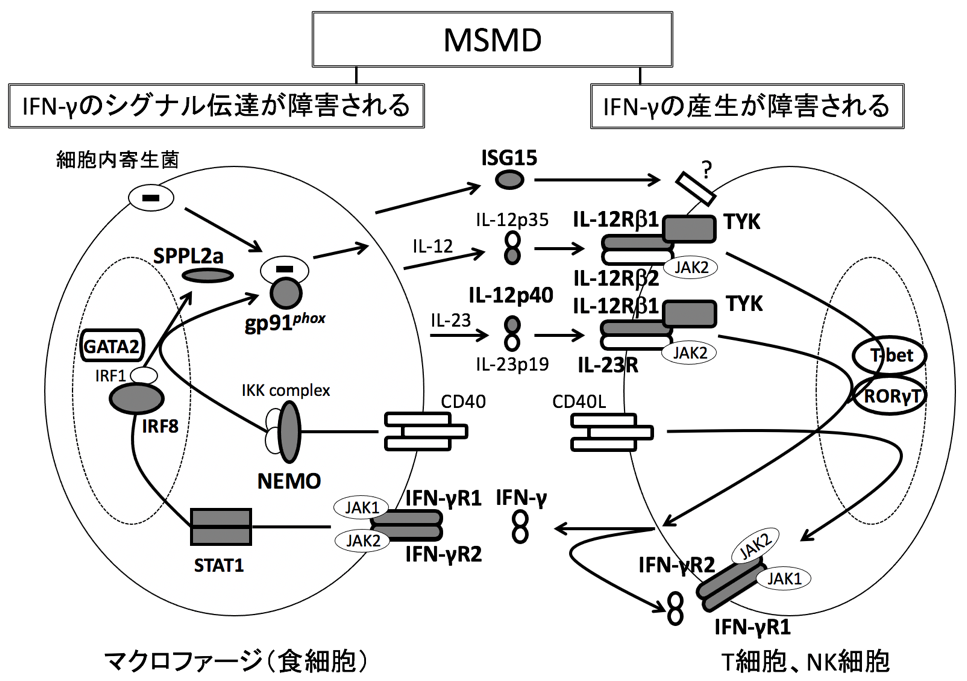 図
図 - (*2)IFN-γ
- T細胞やNK細胞から作られるサイトカイン(細胞に影響を与える物質のこと)で、白血球による炎症を強化する働きを持ちます。また、マクロファージなどの食細胞を活性化させ、その貪食力(細菌などを取り込む能力)や除菌力を強化することで、細胞内寄生菌を排除します。
- (*3)多発性骨髄炎
- 多発性に起こる骨の感染症で、通常は細菌、抗酸菌、真菌などによって起こります。
- (*4)破骨細胞
- 多数の核を持つ巨大な細胞で、骨を吸収する働きがあります。骨髄内に存在し、様々な免疫細胞の元となる『造血幹細胞』から作られるマクロファージ系の破骨前駆細胞にサイトカイン(RANKLとM-CSF)を加えると、破骨前駆細胞同士が融合して破骨細胞が形成されます。
- (*5)IFN-γR1異常症
- IFN-γの刺激を感知する受容体の1つ。本症では、IFN-γの作用が障害されることでMSMDを発症します。
- (*6)STAT1異常症
- STAT1は、シグナル伝達兼転写活性化因子(STAT:signal transduction and activator of transcription)ファミリーに属する分子で、IFN-α/β, IFN-γなどからの刺激を伝達し、遺伝子発現を誘導する役割を持ちます。本症では、IFN-γの作用が障害されることでMSMDを発症します。
- (*7)IL-12Rβ1異常症
- IL-12の刺激を感知する受容体です。本症では、IL-12の作用が障害され(二次的にIFN-γの産生が障害され)MSMDを発症します。
- (*8)TRAP
- 酒石酸抵抗性酸性ホスファターゼ(Tartrate-Resistant Acid Phosphatase)は、破骨細胞のマーカーとして使われます。
お問い合わせ先
研究に関すること
広島大学 大学院医系科学研究科 小児科学 教授 岡田 賢
報道(広報)に関すること
広島大学 広報部広報グループ
AMED事業に関すること
日本医療研究開発機構(AMED)
ゲノム・データ基盤事業部医療技術研究開発課
難治性疾患実用化研究事業