2023-01-10 生命創成探究センター
本研究成果のポイント
- 免疫応答を記述する数理モデルを開発
- 免疫系が適切な応答を起こすための学習過程を機械学習の概念を用いて記述
- 抗原の特徴に応じて異なる強さの応答が誘導されることを示し、アレルギーの発症やその治療効果を再現
概要
広島大学大学院統合生命科学研究科データ駆動生物学研究室の本田直樹教授(兼任:京都大学生命科学研究科特命教授、自然科学研究機構生命創成探究センター客員教授)、吉戸香奈さん(京都大学生命科学研究科大学院生)らからなる研究グループは、免疫系が体内への様々な侵入者(抗原)に対して有害か無害かを判断し、適切な免疫応答を起こす仕組みを提案する数理モデルを開発しました。
免疫系は自己(体内にある物質)と非自己(ウイルスなどの外からの侵入者)を判別できることは良く知られています。しかし、非自己の抗原には、有害なウイルスや細菌だけでなく、無害な花粉や食べ物なども含まれていますが、どのように免疫系がそれらを識別し、適切な強さの応答を誘導しているのかは免疫学における大きな謎でした。本研究では、「予測符号化」という機械学習の概念に基づき、「免疫系が抗原のリスクを予測し、その予測と実際の観測との誤差に基づいて免疫記憶がアップデートされる」という新しい仮説を提唱しました。この仮説に基づく数理モデルにより、抗原の量やそれが入ってくる速度に応じて免疫応答の強さが決まることを示しました。また、花粉症などのアレルギーの発症や、アレルゲン免疫療法(舌下免疫療法など)の効果を再現し、本モデルの妥当性を示しました。本研究で提唱されたモデルは、「抗原に応じた免疫応答の誘導メカニズム」という免疫学における根本的な謎の解明に貢献することが期待されます。また、アレルギーや腸炎などの免疫系の誤作動によって引き起こされる疾患の、数理モデルを用いた統一的理解に発展することが期待されます。
本研究成果は、iScience誌に2022年12月7日に掲載されました。
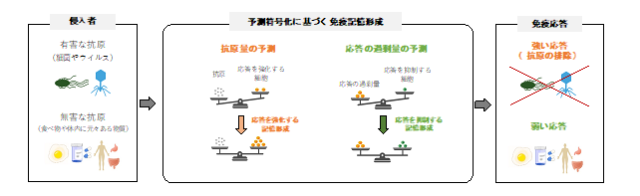
図1 予測符号化に基づく免疫記憶形成(模式図)
背景
私たちの体を細菌やウイルスから守る役割を果たしているのが免疫系です。免疫系は、私たちにとって有害な侵入者(有害な抗原)に対しては強い免疫応答を起こすことでそれらを排除します。一方で、食べ物や体内にもともと存在する物質などの無害な抗原に対しては強い免疫応答を起こしません。これらの無害な抗原に強い免疫応答が誘導されると、アレルギーや自己免疫疾患などの様々な疾患が引き起こされてしまいます。このように免疫系は抗原の危険性に応じてその応答の強さを変化させているのですが、そのメカニズムは未だに明らかとなっていませんでした。
さらに、ワクチンの効果などとして知られるように、免疫系は一度経験した抗原の情報を「免疫記憶」として体内に保存します。この免疫記憶によって、同じ抗原に対する免疫応答が経時的に変化するのですが、その詳細なメカニズムは明らかとなっていません。本研究では、特に、花粉などのアレルゲンに対して突然強い免疫応答を起こしてしまうアレルギーの発症と、そのアレルゲンの成分を少量、長期間投与することでアレルギー症状を緩和させる舌下免疫療法などのアレルゲン免疫療法に着目しました。アレルギーの発症と治療についても、そのメカニズムはよくわかっていません。
研究成果の内容
本研究では、さまざまな種類の免疫細胞(T細胞)の相互作用を記述する数理モデルを提案しました。さらに、免疫系は一度経験した抗原について学習できるシステムであると捉えられることから、機械学習で用いられる「予測符号化」という概念をモデルに導入しました(図1)。具体的には、免疫応答を強化する細胞は、抗原を効率的に排除するために「抗原の量」を予測します。一方で、免疫応答を抑える細胞は、過剰な応答を効率的に抑えるために「どのくらい免疫応答が過剰であるか」を予測します。これらの予測による情報は免疫記憶を担う「メモリーT細胞」の生成に反映されると仮定しました。
この予測符号化による免疫記憶形成を導入した数理モデルの数値シミュレーションにより、免疫系が抗原の量や抗原の入ってくるスピードに応じてその応答の強さを変化させることを示しました。つまり、大量かつ急激に入力される抗原に対しては強い応答を起こす一方で、少量または大量でもゆっくり入力される抗原に対しては強い応答を起こさないという結果が得られました。これは、ウイルスや細菌は体内で自己増殖することで急激にその量が増加するために強い免疫応答が起こる(免疫系によって排除される)一方で、食べ物などは体内でその量が急激に増えることがないために強い応答が起きない(排除されない)と解釈することができます。
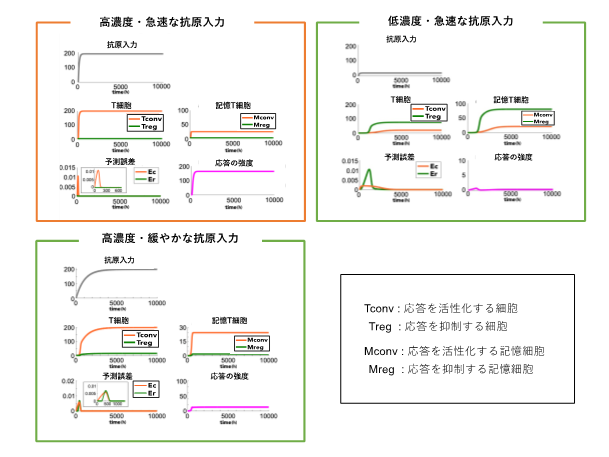
図2 異なる抗原の量や入力速度に対する免疫応答のシミュレーション
また、アレルギーの発症とその治療のシミュレーションも行いました。大量の抗原にさらされると上述のとおり強い免疫応答が誘導されます。しかし、その後に少量の抗原を投与すると、免疫系を抑制するタイプのメモリーT細胞が蓄積しました。その結果、再び大量の抗原を投与しても、その応答が弱まることが示されました。つまり、我々の提案した数理モデルによって、花粉などのアレルゲンに大量にさらされることにより引き起こされるアレルギーの発症、さらには、アレルゲンの成分を少量、長期間投与することによって、再びアレルゲンに曝露されてもアレルギーが発症しないというアレルゲン免疫療法(舌下免疫療法など)の効果を再現することができました。
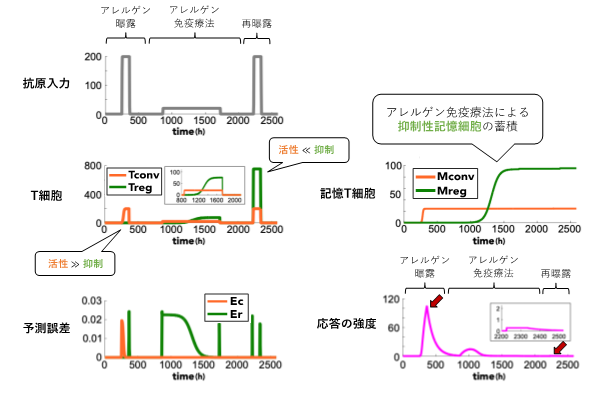
図3 アレルギーの発症およびその治療のシミュレーション
今後の展開
本研究は、免疫応答を記述する数理モデルを開発し、予測符号化という概念を用いて免疫系が抗原の危険性を予測しつつ、適応的に学習している可能性を提唱しました。これまで、実験免疫学では、「この抗原に対してはこのような応答が起こる」というように各抗原に対する応答が詳細に解明されてきました。しかしながら、そもそも「なぜ抗原によって異なる応答を誘導できるのか?」という根本的な謎が残ったままでした。本研究のように数理モデルを用いることで、実験のみでは解明が難しい「統一的なメカニズム」を提案することが可能になります。今後、実験的アプローチによって数理モデルから提案されたメカニズムを検証していくことで、複雑な免疫系の統一的理解が発展していくと考えられます。
掲載論文
著者: Kana Yoshido & Honda Naoki,
タイトル: Adaptive discrimination between harmful and harmless antigens in the immune system by predictive coding
掲載誌: iScience, 2023
DOI: https://doi.org/10.1016/j.isci.2022.105754
プロジェクトについて
本研究は、JST【ムーンショット型研究開発事業目標2050年までに、超早期に疾患の予測・予防をすることができる社会を実現】【JPMJMS2024-9】、自然科学研究機構生命創成探究センターExCELLS連携研究、学術変革研究領域(B)(No. 21H05170、計画班代表:本田直樹)、日本学術振興会(JSPS)科学研究費助成事業の基盤研究(B)(No.21H03541、代表:本田直樹)、特別研究員奨励費(No. 21J23680、代表:吉戸香奈)の支援を受けたものです。
お問い合わせ先
研究に関すること
広島大学大学院統合生命科学研究科 数理生命科学プログラム データ駆動生物学研究室
教授 本田直樹
広報に関すること
広島大学 広報室
京都大学 総務部広報課国際広報室
自然科学研究機構 生命創成探究センター 研究戦略室