ハッキングシステムで遺伝子ドライブを分割してフルドライブに変換、新たな実験の柔軟性を提供…一方でフルドライブシステムの驚くべきフィットネスコストも明らかに Hacking system converts split gene drives into full drives, offering new experimentation flexibility… but also reveals surprising fitness costs of full drive systems
2023-01-12 カリフォルニア大学サンディエゴ校(UCSD)
蚊のために設計された遺伝子ドライブは、毎年何十万人もの死者を出しているマラリア感染の拡大を抑制する可能性があるが、このようなドライブは急速に広がって集団全体を支配してしまうので、安全性の問題が指摘されている。研究者らは、蚊のような標的集団における遺伝子ドライブ要素の拡散を支配する原理を、ドライブ装置を構成するさまざまな部品の組み合わせを試すことで解明してきた。しかし、研究チームは、まだ解明すべきことがあり、重要な疑問が残っていることを明らかにした。
Nature Communications誌において、カリフォルニア大学サンディエゴ校の研究者は、元博士研究員のGerard Terradas、博士研究員のZhiqian Li、Ethan Bier、カリフォルニア大学バークレー校大学院生のJared Bennett、准教授のJohn Marshallと密接に協力し、実験室で遺伝子ドライブを試験・開発する新しいシステムの開発と、それを実際の応用に向けて安全にツールに転換することについて記述しています。
生物科学部、細胞発生生物学教室の教員であるBierは、「これらの研究は、遺伝子ドライブシステムの新たな工学的機能を強化すると同時に、最も重要な可動部分間の重要な相互作用を評価・分析する方法に関する重要な情報を提供しています」と述べています。
<関連情報>
- https://today.ucsd.edu/story/researchers-create-new-system-for-safer-gene-drive-testing-and-development
- https://www.nature.com/articles/s41467-022-35044-4
分割駆動素子からフル駆動素子への遺伝的変換 Genetic conversion of a split-drive into a full-drive element
Gerard Terradas,Jared B. Bennett,Zhiqian Li,John M. Marshall & Ethan Bier
Nature Communications Published:12 January 2023
DOI:https://doi.org/10.1038/s41467-022-35044-4
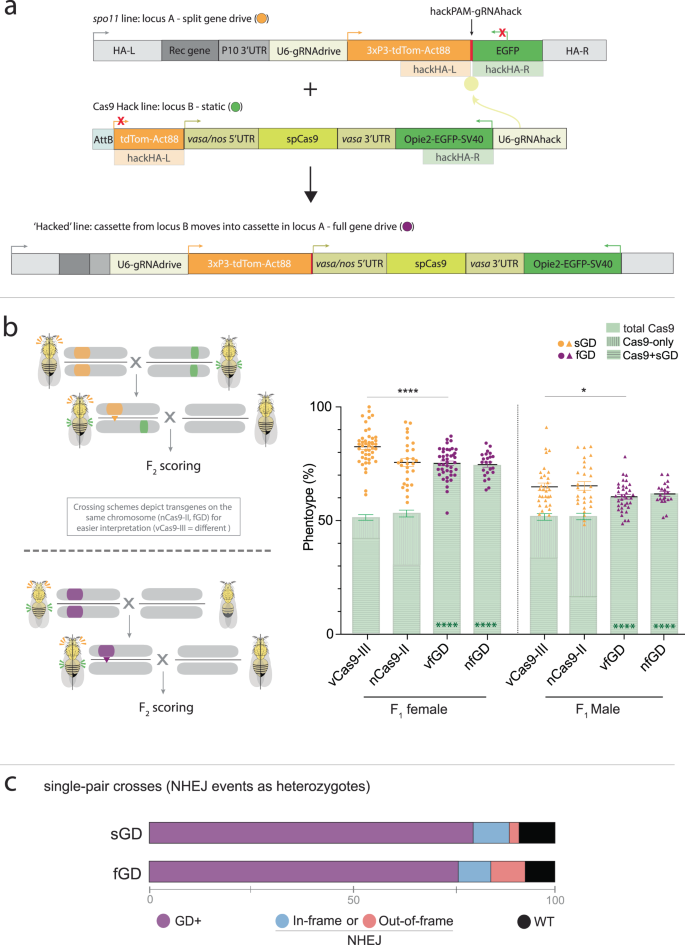
Abstract
The core components of CRISPR-based gene drives, Cas9 and guide RNA (gRNA), either can be linked within a self-contained single cassette (full gene-drive, fGD) or be provided in two separate elements (split gene-drive, sGD), the latter offering greater control options. We previously engineered split systems that could be converted genetically into autonomous full drives. Here, we examine such dual systems inserted at the spo11 locus that are recoded to restore gene function and thus organismic fertility. Despite minimal differences in transmission efficiency of the sGD or fGD drive elements in single generation crosses, the reconstituted spo11 fGD cassette surprisingly exhibits slower initial drive kinetics than the unlinked sGD element in multigenerational cage studies, but then eventually catches up to achieve a similar level of final introduction. These unexpected kinetic behaviors most likely reflect differing transient fitness costs associated with individuals co-inheriting Cas9 and gRNA transgenes during the drive process.