2023-03-28 量子科学技術研究開発機構
発表概要
- 致死性心室不整脈に対する世界初の炭素イオン線(重粒子線)による不整脈放射線治療をQST病院において実施しました。
- 痛みは伴わず、治療時間は準備を含め1時間以内(照射時間8分)と低侵襲です。
- 難治性心室頻拍に対する体外放射線照射はX線が使用されていますが、治療対象領域(ターゲット)周辺の健常組織を完全に回避することが難しいという問題があります。そのため、心臓を栄養する冠動脈とターゲットが近接している症例は治療困難な現状がありました。炭素イオン線はその物理特性を生かし、冠動脈を回避することに成功しました。
- これまで炭素イオン線治療は主にがん治療を対象としていましたが、難治性不整脈に苦しむ患者さんの新たな選択肢としての可能性を広げます。
発表概要
東海大学医学部付属病院(所在地:神奈川県伊勢原市下糟屋143、病院長:渡辺雅彦)循環器内科教授の吉岡公一郎および量子科学技術研究開発機構(所在地:千葉県千葉市稲毛区穴川4-9-1、理事長:平野俊夫) QST病院(病院長:山田滋)治療診断部部長の若月優らの研究グループは、難治性致死性心室不整脈(心室頻拍)〔i〕に対する重粒子線〔ii〕を用いた体外放射線治療 (特定臨床研究, 厚労省認定番号 jRCTs032190041, https://jrct.niph.go.jp/re)を2023年2月に実施しました。
致死性心室不整脈は、治療に緊急を要する極めて重篤な不整脈を指します。心室頻拍では、心臓が1分間に120回以上不規則に痙攣し、ときに心室細動へ移行するため、心臓突然死の原因となります。心室頻拍を引き起こす可能性のある代表的な器質的心臓病としては、心筋梗塞、拡張型心筋症、肥大型心筋症、催不整脈性右室心筋症、心サルコイドーシスなどがあります。日本では年間 6~8 万人が心臓突然死で亡くなっており、高齢社会においてさらに増加することが予想されています。心室頻拍の治療は現在のところ薬剤、カテーテルアブレーション〔iii〕、植込み型除細動器〔iv〕の3つが主体ですが、これらを組み合わせて治療を行っても難渋することのある重篤な疾患です。いくつかの理由でこうした治療を全て受けられないことも少なくありません。
体外放射線治療は、心室頻拍に対する第4の選択肢として期待されています。現時点では心筋梗塞ないし心筋症に合併する心室頻拍が良い適応です。治療のために麻酔の必要がなく、また照射時間が極めて短時間であることから、患者さんにとって侵襲性が低いことがメリットです。これまでの放射線治療の適応は、ほぼ腫瘍疾患に限られていましたが、不整脈という全く異なる疾患領域への治療応用は極めて革新的です。一方で本治療はいまだ発展途上にあり、幾つかの限界もあります。使用する放射線には世界的にX線が選択されていますが、心臓を栄養する冠動脈と治療対象領域(ターゲット)が近接している場合は治療が困難となります。そこでわれわれは放出エネルギーの調整が可能な物理特性を有する炭素イオン線に着目しました。X線のリスクが高い症例に対して新たなオプションを追加できたことは、不整脈放射線治療領域における大きな前進であると言えます。
特定臨床研究の背景
がん治療では、体幹部定位放射線治療(SBRT)〔v〕などの放射線治療技術の進歩により、標的組織に隣接する正常臓器への障害を最小限に抑えつつ、標的に対して高線量の放射線を正確に照射することが可能となりました。この技法を応用し、2017年より「難治性致死性心室不整脈(心室頻拍)」に対する体外放射線治療が実施され、優れた治療成績を収めています(Cuculich PS, et al. NEJM, 2017)。東海大学の吉岡らの研究グループは、2019 年日本国内の医療機関において初めて本治療を実施し、その成果を報告しました(Heart Rhythm Case Rep. 2021;7:306-311. )。ターゲットの設定には独自に心臓核医学(99mTc-TF, I123MIBG, F18FDG-PETなど)〔vi〕による機能評価手法を取り入れて、綿密な治療計画を作成しています(Circ Rep. 2023;5:69-79 )。それと同時に健常組織への被ばくを最小限にとどめるためにより有効な手段は何かを検討してきました。炭素イオン線による臨床実施計画です。
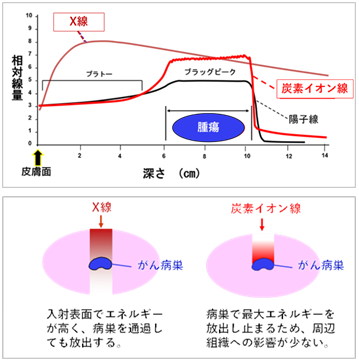
X線と炭素イオン線の線量分布を比較してみます。右図の如く仮に体表面から8cmの深さに腫瘍があった場合、X線は体内へ入射する際に皮膚の表面近くで放射線のエネルギーが最大になり、体の奥へ進むほど線量が減少します。
炭素イオン線では、病巣直前で放出エネルギーを増大させ、その後急激に減衰するように設定可能です。そのため放射線量を集中させ、正常組織への影響を少なくすることが可能です。この特徴を心臓に応用することで、ターゲット周辺の微細構造(冠動脈、大動脈弁、房室結節など)や心臓後方臓器(気管、食道、大血管など)への影響を減少させることが出来ると考えています。
炭素イオン線(重粒子線)による治療の実施
炭素イオン線をもちいた重粒子線治療は放射線医学総合研究所(現 量子科学技術研究開発機構:QST)において1994年6月から開始され、現在までに約1万5千人のがん患者さんに実施されています。治療用の加速機器は、世界に15施設、日本に7施設配備され、わが国は世界有数の炭素イオン線治療大国です。新世代の放射線治療として、今まで一貫してがんや肉腫などの悪性腫瘍性疾患を対象に使用されてきましたが、今回のような非腫瘍性疾患に対する適応は初めての試みでした。患者さんは治療室へ独歩で入室し、麻酔等の使用はなし、治療時間は準備を含め1時間、照射時間は8分です。治療中の植込み型除細動器の誤作動や故障はなく、バイタルサインは安定していました。治療後の急性心膜炎や心不全などの合併症はなく、4日後無事に退院しました。まもなく治療1か月となりますが、有害事象なく経過しています。放射線による抗不整脈効果は一般的に3か月の観察期間を経て評価されますが、晩期放射線合併症とあわせて十分に留意して外来で慎重に経過を見ていく予定です。X線を用いたSBRTでも、炭素イオン線による放射線治療であっても、いずれも高精度放射線療法であり、心臓ターゲットの位置や患者さんの病態特性によって、両者を使い分けられるになることが今後の我々の目標です。
今後の展開
放射線が不整脈を抑制する基礎的メカニズムは徐々に明らかになってきています。カテーテルアブレーションによる不整脈治療は、心室頻拍の原因となる異常な電気回路を物理的に遮断することが目標です。高周波による熱焼灼あるいはガス冷却による凍傷によって、不整脈の原因となる心筋組織の線維化を獲得することが治療効果となります。いっぽう放射線治療では、線維化が確立する3~6か月を待たずして照射早期(翌日~1か月)より不整脈の抑制作用が認められることが多く報告されました。すなわち、早期の抗不整脈効果は必ずしも線維化に起因しないことが類推されています。
本研究グループは世界に先駆けて1997年より炭素イオン線(重粒子線)が心臓に及ぼす電気生理学的機序について基礎研究を重ねてきました。2000年の米国心臓協会学術集会において「放射線が有する抗不整脈効果について」はじめて明らかにました。その主要なメカニズムとして、炭素イオン線が梗塞心における心臓ギャップ結合蛋白コネキシン43(Cx43)〔vii〕の発現を促す事実を発見し、その結果として興奮伝導の回復が促されることで心室不整脈が抑制されることを報告しています(Cardiovasc Res. 2006, Am J Physiol Heart Circ Physio. 2010, Pacing Clin Electrophysiol. 2017, Int J Part Ther. 2018)。近年では、炭素イオン線が心室不整脈のみならず心房細動〔viii〕の誘発性をも低下させることを明らかにしました (Circ J. 2022)。加齢うさぎを用いた心房細動モデルにおけるコネキシン40/43(Cx40/43)の回復以外に、過剰に増生した幼若交感神経を抑制することがひとつの機序と類推しています。
コネキシン蛋白は細胞間コミュニケーションを司る重要な役割を担っていますが、不全心で著しく減少することが不整脈発生の要因として知られてきました。不全心では心臓の収縮力の低下を補うために交感神経系およびレニン-アンジオテンシン系が活性化します。交感神経の亢進は不整脈発生の修飾因子として作用するため、β遮断薬などを用いた抑制を行うことが一般的です。炭素イオン線は細胞間コミュニケーションの改善と交感神経過増生の抑制に一役を担うことから、心不全の治療法としても発展する可能性を秘めています。
付記
本研究は以下の支援により実施されています。
日本学術振興会 科学研究費助成事業 基盤研究C 「致死性心室不整脈患者に対する放射線体外照射による新規不整脈治療」(研究代表者 吉岡公一郎、2020-2023)、 日本学術振興会 科学研究費助成事業 基盤研究C「病態ウサギにおける重粒子線の心房細動抑制作用と電気生理学機序の解明」(研究代表者 網野真理, 2019-2022)、東海大学医学部医学科研究助成金重点的研究「ウサギ心房細動モデルにおける炭素線照射による抗不整脈効果のメカニズム解析」(研究代表者 網野真理, 2020-2021)、公益財団法人 放射線影響協会 研究奨励助成金「放射線体外照射による致死性心室不整脈抑制作用における交感神経除神経効果を明らかにする」(研究代表者 網野真理, 2020-2021)、QST 戦略的理事長ファンド(研究分担者 網野真理、 2020-2023)、QST創成研究理事長ファンド(研究責任者 網野真理、 2021-2023)
【研究代表者】
吉岡公一郎(東海大学医学部付属病院循環器内科 教授、量子科学技術研究開発機構 共同利用研究員)
【研究分担者】
若月優(量子科学技術研究開発機構 量子生命・医学部門 QST病院 治療診断部 部長)
網野真理(東海大学医学部付属病院 循環器内科 准教授、量子科学技術研究開発機構 量子生命・医学部門 量子医科学研究所 重粒子線治療研究部 主幹研究員)
森慎一郎(量子科学技術研究開発機構 量子生命・医学部門 量子医科学研究所 物理工学部治療システム開発グループ グループリーダー)
下川卓志(量子科学技術研究開発機構 量子生命・医学部門 量子医科学研究所 物理工学部粒子線照射効果研究グループ グループリーダー)
森康晶(量子科学技術研究開発機構 量子生命・医学部門 QST病院 治療診断部治療課 医師)
石川仁(量子科学技術研究開発機構 量子生命・医学部門 QST病院 副病院長)
株木重人(東海大学医学部付属病院 放射線治療科 講師)
国枝悦夫(東海大学医学部付属病院 放射線治療科 客員教授、総合東京病院放射線治療センター長)
橋本順 (東海大学医学部付属病院 画像診断科 教授)
伊苅裕二(東海大学医学部付属病院 循環器内科 教授)
菅原章友(東海大学医学部付属病院 放射線治療科 教授)
柳下敦彦(東海大学医学部付属病院 循環器内科 准教授)
坂間晋(東海大学医学部付属病院 放射線治療科 講師)
福澤毅(東海大学医学部付属病院 放射線治療科 助教)
黒木俊寿(東海大学医学部付属病院 放射線治療科 助教)
【コーディネーター】
鈴木和子(量子科学技術研究開発機構QST病院 経営戦略部 臨床研究支援室 臨床研究コーディネーター)
露木匡子(量子科学技術研究開発機構QST病院 経営戦略部 臨床研究支援室 臨床研究コーディネーター)
藤原由希子(東海大学医学部付属病院 治験・臨床研究センター Ns CRC)
用語解説
〔i〕難治性致死性心室不整脈
死亡してしまう危険性の高い不整脈を「致死性不整脈」と呼び、極めて重症度が高い病態です。頻脈性(脈が速い)と徐脈性(脈が遅い)に大別され、前者では心室細動および持続性心室頻拍、後者では洞停止および完全房室ブロックが代表的な疾患です。心室頻拍の治療においては、従来治療(薬剤、カテーテルアブレーション、植込み型除細動器など)に抵抗性の場合を難治性と定義します。薬剤副作用で投薬を中断せざるを得ない場合や、解剖学的理由などでアブレーション治療を施せない場合も含まれます。
〔ii〕 炭素イオン線(重粒子線)
重粒子とはヘリウム(He)より重い原子番号をもつ原子の原子核(重イオン)ビームを指します。日本では重粒子線の一つである炭素イオン線が代表的で、20年近くにわたり“がん治療”に用いられていることから、「重粒子線」イコール「炭素イオン線」と考えても良いでしょう。陽子の12倍の重さをもつ炭素の原子核を光速の約70%まで加速して照射するため、高い線量集中性と生物効果を持ち合わせ、がん治療に適した性質と言えます。
量子科学技術研究開発機構(量研/QST)は、炭素イオン線などによるがんの治療、放射線の人体への影響や医学利用、放射線防護や被ばく医療などの研究、量子論や量子技術に基づく生命現象の解明と医学への展開を目指す量子生命科学研究、量子ビームによる物質・材料科学、生命科学等の先端研究開発、高強度レーザーなどを利用した光量子科学研究、国際協定に基づくITER計画及び幅広いアプローチ(BA)活動を中心とした人類究極のエネルギー源である核融合の研究などを実施し、炭素イオン線研究のトップランナーとして先導的な役割を果たしています(https://www.qst.go.jp/site/about-qst/). そのなかでもQST病院は炭素イオン線を用いた臨床治療を世界で最も早く開始し、その実績は他国の追随を許しません(https://hospital.qst.go.jp/)。
〔iii〕 心室不整脈のカテーテルアブレーション
カテーテルと呼ばれる直径2mm程度の細い管を鼠径部の大腿静脈から心臓に挿入し、カテーテルの先端から高周波電流を流し、心室不整脈の原因となる異常な電気回路を焼灼します。組織の線維化による瘢痕がおこると不整脈の起源ないし異常伝導路が遮断され、発作が起きにくくなる治療法です。外科的な心臓手術と違って、胸部を切開する必要はありません。カテーテルアブレーションで心室不整脈以外に上室不整脈や心房細動を治療することができますが、不整脈の種類や患者さんの状態によって根治率や再発率は異なり、複数回の治療が必要な場合もあります。手技時間は2-5時間、術後は6-8時間の安静が必要です。
〔iv〕 植込み型除細動器
植込み型除細動器は、致死性頻脈性心室不整脈(心室頻拍、心室細動など)の発生を検知するために、心臓を常時監視し、発作時には電気ショックを作動させて突然死を予防します。しかし不整脈が起こらないよう予防する機器ではないため、根治治療にはなり得ません。薬物やカテーテルアブレーション治療などと併用することが効果的と言われています。一般的にICD(Implantable Cardioverter Defibrillator)と呼ばれています。電池の寿命は作動状況によって異なりますが、大体4~5年程度で電池交換手術が必要となります。
〔v〕 体幹部定位放射線治療(SBRT)
放射線技術の開発によって三次元高精度照射が可能となり、胸部や腹部の病巣に対して放射線を6~8方向から1点に高い精度で照射する治療法です。集中性に優れていることから「ピンポイント照射」とも呼ばれています。1回線量を高く設定することが出来るため、患者さんは短期間で治療を終えることが可能です。
〔vi〕 心臓核医学検査
99m-Tc-TF (99m-technetium tetrofosmin): 心臓における可逆的な虚血および梗塞組織の領域を特定するために使用されます。安静および負荷検査の2種類があり、安静シンチグラフィーでは残存心筋の領域や心機能の評価が可能です。後者の負荷心筋シンチグラフィーでは、心臓に薬剤ないし運動負担をかけた状態と安静の状態の二回検査を行うことで、冠動脈の狭窄に起因する狭心症の診断が可能となります。
I-123-MIBG (123I- metaiodobenzylguanidine scintigraphy):不整脈の発生は心臓交感神経の影響を強く受けることから、MIBGを用いて心筋局所における交感神経機能を評価します。MIBGはノルアドレナリンと構造が類似していることから、心筋内でノルアドレナリンと同様の挙動を示します。交感神経末端において心筋に取り込まれ、貯蔵顆粒に保存されます。正常心筋ではMIBGの高い集積がみられますが、いっぽう障害心筋では交感神経機能の障害をきたしていることから、除神経領域ではMIBGが集積しないという現象が画像で確認できます。
F-18-FDG-PET (Fluorodeoxyglucose F18 Positron Emission Tomography):PET検査は一般的に“がん疾患”で多用されることが多い検査です。循環器領域では、虚血性心筋症による心不全患者を対象に、心筋血流SPECTでは生存心筋の判定が困難な場合にPET検査を施行します。PETはSPECTに比べて、ガンマ線の吸収による減衰が少なく、鮮明な画像が得られることが特徴です。心筋の血液かん流が、僅かながら温存されている部位を同定することが可能です。
〔vii〕 コネキシン
心筋細胞を相互に連結しているミクロの構造に、ギャップジャンクション(gap junction)、デスモゾーム(desmosome)、接着結合(fascia adherens)の3種類があります。後者2つは、それぞれ細胞骨格と収縮タンパクの付着部位であり、細胞どうしの機械的な連結部位であることから興奮伝導には関与しませんが gap junctionは細胞の電気的かつ代謝的連結を司る中心的なたんぱく質です。軽度ストレス時には隣接細胞へ障害を伝達し、一部の細胞に掛かる致命的なダメージを希釈します。高度ストレス時にはギャップジャンクションを閉鎖し、障害をうけた細胞のアポトーシス(能動的な細胞死)を実施すると考えられてきました。
ほ乳類の心筋細胞に発現しているコネキシンは, Cx40, Cx43, Cx45の 3種類で、それらの分布は心臓内の部位によって異なります。心房や心室の作業筋には Cx43が最も多く、心房筋では Cx40も存在します。心室内刺激伝導系(His束,脚,プルキンエ線維)では Cx40が豊富に発現し、洞房結節や房室結節では Cx45が主体となります。虚血、心肥大、炎症などの病態にともなってコネキシンの発現量や発現部位やリン酸化状 態などが変化し、正常な興奮伝導が妨げられて不整脈発生基質を形成します。
〔viii〕 心房細動
心房細動は, 1分間に400~600回の速さで心房が振動し、血液のうっ滞により血栓が形成されます。この血栓が脳の血管に詰まって脳梗塞を引き起こすと、重症化しやすく死亡することもあります。幸いにも救命されたとしても、言語障害や運動麻痺などの重い後遺症が残ることが少なくありません。高齢者では心房細動を発症する方が多く、脳梗塞予防のために血液をさらさらにする抗凝固薬が必要になります。抗凝固薬は出血性副作用の危険性を高め、長期的な内服が難しい場合があります。心房細動は検診で診断される患者数だけでもおよそ80万人、実際には100万人を超すと推定されており、高齢社会で増加の一途をたどっています。心房細動に対するカテーテルアブレーションは心室不整脈に比べて成功率が高く、70%程度の症例で根治を期待でいます。焼灼の手法は、高周波、冷凍凝固、レーザーなどが一般的ですが、近年ではマーシャル静脈に対するエタノール注入法やパルスフィールドアブレーションといった最新の治療法が開発されています。