2023-04-24 京都大学iPS細胞研究所
ポイント
- 免疫不全デュシェンヌ型筋ジストロフィー(DMD)モデルラットを作製した。
- 従来のDMDモデルマウスよりDMD患者さんに近い重篤な症状を示す。
- ヒト不死化筋芽細胞株をDMDモデルラットの前脛骨筋に移植すると生着する。
1. 要旨
佐藤優江 特定研究員(京都大学CiRA臨床応用研究部門)、櫻井英俊准教授(京都大学CiRA同部門)らの研究グループは、免疫不全ラット(ヌードラット注1)とデュシェンヌ型筋ジストロフィー(DMD)モデルラット注2を交配させ、免疫不全DMDモデルラットを作製しDMD患者さんと同様に重篤な症状を示すことを明らかとしました。さらに、この免疫不全DMDモデルラットにヒト不死化骨格筋芽細胞を前脛骨筋に移植し生着することを世界で初めて報告しました。
本研究で報告されたDMDモデルラットは従来の細胞製剤の評価試験で一般的に用いられてきたDMDマウスモデルと比較してDMD患者さんと酷似したきわめて重篤な臨床症状を示しました。DMDモデルラットは、細胞製剤の前臨床試験での評価試験に使用することが可能であり、より正確に病態改善効果などを運動機能や生化学的検査により測定することが可能になると考えられます。これらの成果により、DMD治療に有効な細胞製剤の早期実用化、細胞移植治療の実現に貢献できると期待されます。
この研究成果は2023年4月10日にスイス科学誌「Frontiers in Physiology」でオンライン公開されました。
2. 研究の背景
デュシェンヌ型筋ジストロフィー(DMD)は、筋肉にあるジストロフィンというタンパク質が欠損することによって筋肉が変性や壊死する進行性の重篤な筋疾患で、根本的な治療法は開発されていません。また、DMDでは、病状の進行に伴い呼吸機能と心機能が低下し、呼吸不全および心不全となり致死的な病態となります。
本研究グループは、これまでに、ヒトiPS細胞から高い再生能を持つ骨格筋幹細胞の誘導に成功しています(CiRAプレスリリース:2020年7月3日「筋ジストロフィーマウスにおけるヒトiPS細胞由来骨格筋幹細胞の移植効果を確認」)。DMDの細胞移植治療を行うためには、移植する細胞の評価を行うモデル動物が必要です。ヒト細胞を移植することが可能となる免疫不全のDMDモデルラットを作製し、病理学的評価、生化学的評価、運動機能評価を実施しました。
3. 研究結果
1)免疫不全DMDモデルラットはDMD患者さんの病態を再現している
まず本研究グループは、免疫不全ラットにDMDモデルラットを交配させ免疫不全DMDモデルラットを作製しました(図1)。また、免疫不全DMDモデルラット(DMD nude)は68週齢で死亡することが明らかとなり、極めて症状が重篤であることが示唆されました(図2)。
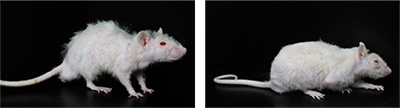
図1 免疫不全ラット(左)と免疫不全DMDモデルラット(右)
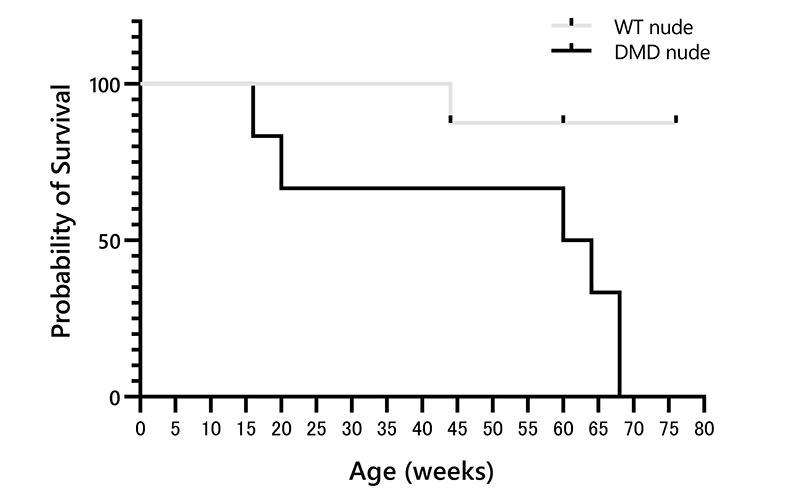
図2 免疫不全DMDモデルラットの生存曲線
2)免疫不全DMDモデルラットでは筋破壊と運動機能低下が生じている
筋破壊の指標である尿中タイチンを測定したところ、免疫不全DMDモデルラット(DMD nude)では野生型ラット(WT nude)と比較して有意に上昇していました(図3、左)。また運動機能評価として前肢の握力を測定するGripテストを実施したところ、免疫不全DMDモデルラットでは野生型ラットに比べ有意に低下していました(図3、右)。さらに12か月齢の免疫不全ラットと免疫不全DMDモデルラットの各筋重量を比較したところ、近位筋である大腿四頭筋で骨格筋重量が低下し、心筋では重量の増大が認められました(図4)。これらの所見はDMD患者さんにおいて認められる病態と類似しており、患者さんの病態を模倣していることが示唆されます。
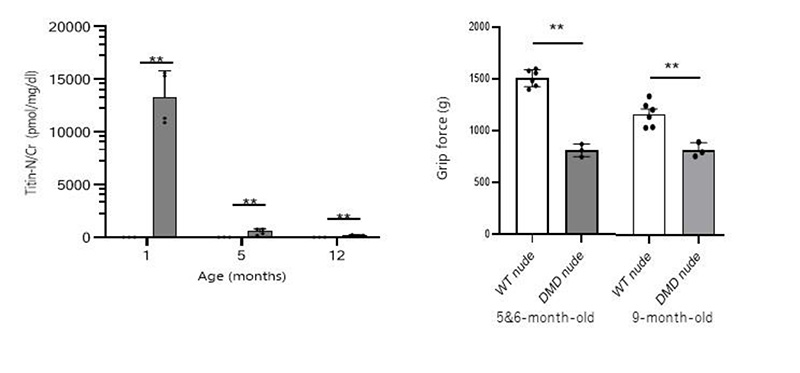
図3 免疫不全DMDモデルラットの生化学的検査と運動機能評価
1、5、12か月齢の尿中タイチンの測定結果(左)と、5~6か月齢と12か月齢でのGripテストの結果(右) **p<0.01
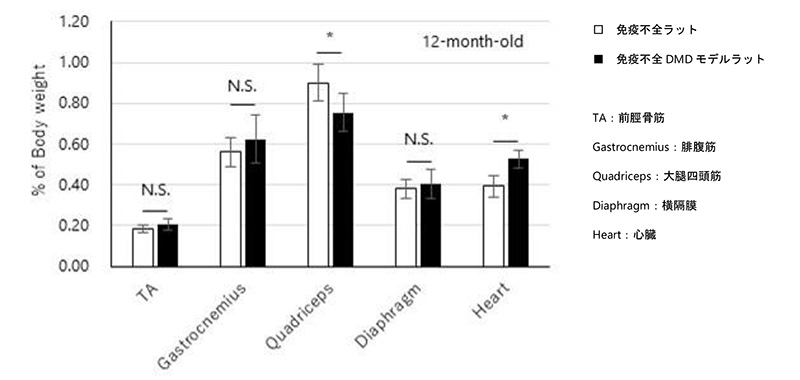
図4 免疫不全DMDモデルラットの各筋重量/体重比較結果
12か月齢の各筋重量を体重で平均した結果 *p<0.05
3)免疫不全DMDモデルラットでは横隔膜と心臓は月齢とともに繊維化が進行する
DMD患者さんでは重篤な呼吸筋障害と心不全を示すことから、今回作製した免疫不全DMDモデルラットについて横隔膜と心臓の繊維化をシリウスレッド染色にて確認しました。免疫不全DMDモデルラットでは横隔膜、心臓について月齢を経るごとに繊維化が進行していることが分かりました。進行性に繊維化が進行していく過程は、DMD患者さんの病態と相関しており、免疫不全DMDモデルマウスでは認められない病態であるので、この免疫不全DMDモデルラットが、より患者さんの病態に近い重篤な病態を示すことが病理組織的解析により確認されました。
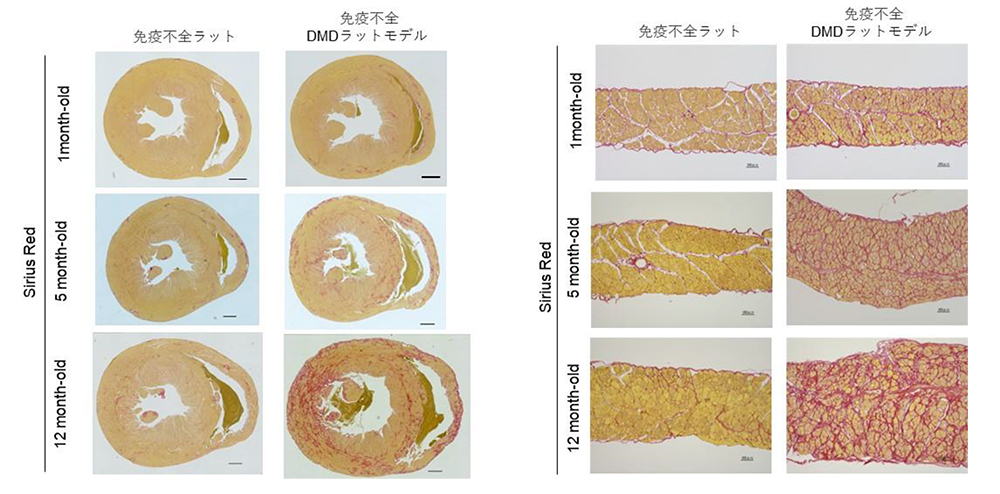
図5 免疫不全ラットと免疫不全DMDモデルラットの心臓と横隔膜のシリウスレット染色結果
1、5、12か月齢での代表的なシリウスレット染色結果。繊維化が進行している領域が赤く染色される。
4)DMDモデルラットの前脛骨筋(TA)へヒト不死化筋芽細胞株(Hu5)を移植し生着を確認した
(1)~(3)の結果より、今回作成した免疫不全DMDモデルラットが免疫不全DMDモデルマウスより重症度が高く、DMDモデル動物として適していることが分かりました。さらに、今回作成した免疫不全DMDモデルラットにヒト不死化筋芽細胞であるHu5/KD3細胞が生着するか確認するため筋肉内への移植実験を行い、3週間後にもヒト不死化細胞が生着し、ヒトスペクトリン陽性かつジストロフィン陽性筋線維を再生していることが分かりました。
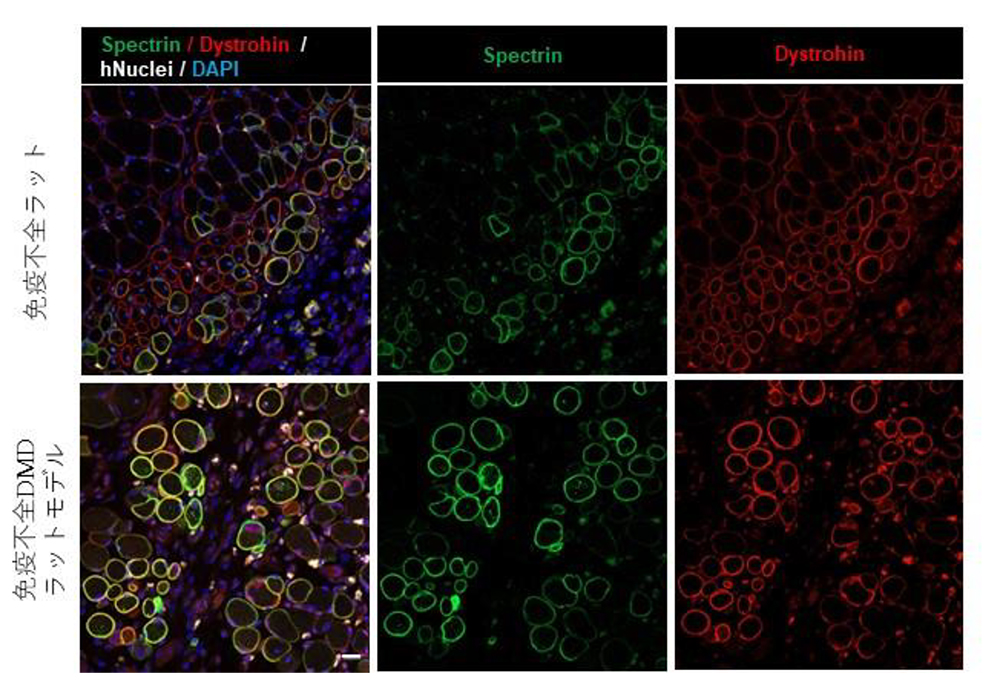
図6 ヒト不死化筋芽細胞株(Hu5)を前脛骨筋(TA)へ移植し3週間後の筋組織の免疫染色像
ヒトスペクトリン陽性筋線維はヒト細胞が筋線維を再生させていることをあらわす。免疫不全DMDモデルラットではもともとジストロフィンが欠損しているが、スペクトリン陽性となった筋線維にはジストロフィンも発現しており、移植細胞による筋再生によりジストロフィン陽性筋線維が再生されたことが分かる。
4. まとめと展望
本研究では、免疫不全DMDモデルラットを作製しヒト不死化筋芽細胞が生着可能であることを示しました。また、現在前臨床試験に使用されているDMDモデルマウスより症状が重篤であり、よりヒトDMD患者さんに近い病態を示していることを明らかとしました。
櫻井准教授らの研究でグループでは、DMD患者さんへの細胞移植治療を目指して、ヒトiPS細胞から高い再生能を持つ骨格筋幹細胞の誘導に成功しています。今回、細胞製剤の機能評価に利用可能な免疫不全DMDモデルラットを確立したことにより、DMD患者さんのための細胞移植治療研究を加速させることが期待されます。
5. 論文名と著者
- 論文名
A new immunodeficient Duchenne muscular dystrophy rat model to evaluate engraftment after human cell transplantation - ジャーナル名
Frontiers in Physiology - 著者
Masae Sato1, Megumi Goto1, Keitaro Yamanouchi2, Hidetoshi Sakurai1,*
*責任著者 - 著者の所属機関
- 京都大学iPS細胞研究所 臨床応用研究部門
- 東京大学大学院農学生命科学研究科 獣医学専攻
6. 本研究への支援
本研究は、下記機関より支援を受けて実施されました。
- 国立研究開発法人日本医療研究開発機構(AMED)
- 医療分野研究成果展開事業 産学連携医療イノベーション創出プログラム「ACT-MS」
- 再生医療実現拠点ネットワークプログラム「iPS細胞研究中核拠点」
7. 用語説明
注1)ヌードラット
解剖学的に無胸腺・外見的に無毛で免疫学的にT細胞機能が欠如しており重度免疫不全であることから異種細胞移植実験に使用される。組織学的には毛包が認められ、生後6週齢頃には被毛を持つ個体が多い。
注2)DMDモデルラット
共著者である山内 啓太郎 博士(東京大学大学院農学生命科学研究科 獣医学専攻 准教授)らによりCRISPR/Cas9法をもちいて作製されたジストロフィン遺伝子変異ラット。
DOI番号:10.1038/srep05635

