2024-03-25 産業技術総合研究所
近畿大学生物理工学部(和歌山県紀の川市)生命情報工学科教授 財津桂(研究実施当時、名古屋大学)、愛知県警察本部科学捜査研究所(愛知県名古屋市)主任研究員 久恒一晃、国立研究開発法人 産業技術総合研究所(茨城県つくば市)主任研究員 井口亮、名古屋市衛生研究所(愛知県名古屋市)研究員 谷口賢、金城学院大学生活環境学部(愛知県名古屋市)講師 浅野友美らの研究グループは、尿から薬物を迅速に分析できる新手法「RaDPi-U(ラドパイ-ユー)」を開発しました。この手法は、煩雑な試料調製や専門性の高い装置の操作などが一切不要で、たった3分で尿試料から直接40種類の薬物を分析できます。従来法と比べて、非常に迅速かつ簡便でありながら、信頼性の高い分析結果が得られるため、今後、薬物犯罪捜査や急性薬物中毒の薬物分析などに大きく貢献できます。
本研究成果は令和6年(2024年)3月25日(月)AM9:00(日本時間)に、分析科学に関する国際的な学術誌“Analytical and Bioanalytical Chemistry”に掲載されます。
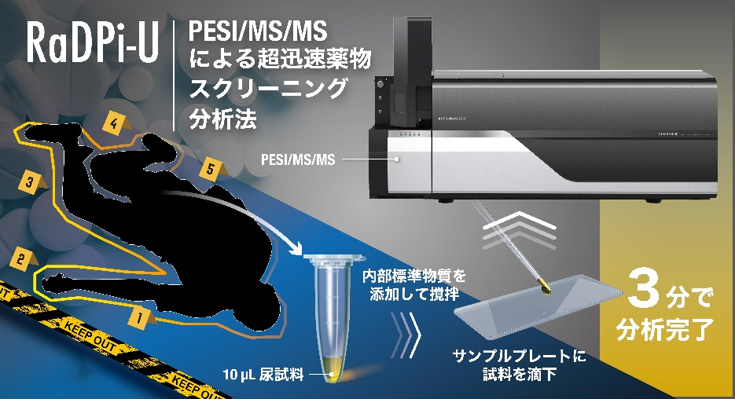
RaDPi-Uのイメージ図(作成者:名古屋大学 髙橋一誠 講師)
1. 本件のポイント
- 微量な尿試料から、薬物犯罪捜査において最も重要度の高い40種類の薬物を、たった3分で迅速に分析可能な手法「RaDPi-U」を開発
- 簡単な3つの手順で結果が得られるため、分析に不慣れな人でも利用可能
- 薬物犯罪捜査や急性薬物中毒の薬物分析などに貢献
2. 研究の背景
覚醒剤や麻薬などの規制薬物を摂取した疑いがある場合、薬物の摂取を証明するためには薬物分析が不可欠です。また、急性薬物中毒※1を起こした可能性がある場合も、原因となる薬物を特定するために薬物分析が必要となります。しかし、実際の犯罪捜査や中毒事故などでは、摂取した薬物が何なのか本人が分からないケースも非常に多くみられます。このような場合、採取が容易な「尿」を対象として薬物スクリーニング分析※2を行い、どのような薬物が含まれているかを迅速に探索するのが一般的です。薬物スクリーニング分析法の代表例としてはイムノアッセイ法※3があり、簡易的なキットを用いて、誰でも検査を行うことができるという長所があります。その反面、似た化学構造を持つ薬物群の推定しかできず、薬物を正確に特定できないことや、交差反応※4による偽陽性(誤判定)が生じやすいという大きな欠点があります。一方で、より専門的な分析方法である質量分析法※5(Mass spectrometry)を用いれば、尿試料に含まれている薬物の同定が可能となる反面、質量分析法を用いるためには高度な専門性が必要となり、煩雑な試料調製に加えて分析に時間を要するといった欠点があります。
3. 本件の内容
研究グループはこれまで、動物の生体試料から直接対象成分を迅速に分析できる探針エレクトロスプレーイオン化タンデム質量分析※6(Probe electrospray ionization tandem mass spectrometry:PESI/MS/MS)を用いた多様な研究を進めてきました。今回、この方法を利用して、イムノアッセイ法のように簡便で超迅速でありながら、質量分析法のように高い薬物の特定能力をもつ新たな薬物スクリーニング法の開発を試みました。
まず、薬物犯罪捜査において最も重要度の高い40種類の薬物を分析対象として選定しました。これらの薬物を、3つのシンプルな手順(①尿と標準液およびエタノールを混合する、②混合液をプレートにのせる、③PESI/MS/MSで分析する)で一度に分析が完了するように設計し、この分析法を「RaDPi-U」としました。その結果、RaDPi-Uでは操作に不慣れな人でも分析を実施でき、たった3分で結果を得ることに成功しました。さらに、実際の尿検体をRaDPi-Uで分析した結果、実用性が高いことも実証しました。
4. 論文掲載
掲載誌:Analytical and Bioanalytical Chemistry(インパクトファクター:4.3@2022)
論文名:Development of a rapid-fire drug screening method by probe electrospray ionization tandem mass spectrometry for human urine (RaDPi-U)
(探針エレクトロスプレーイオン化タンデム質量分析を用いたヒト尿中薬物の超迅速分析法RaDPi-Uの開発)
著者:久恒一晃1*、村田匡2、谷口賢3、浅野友美4、緒方是嗣2、井口亮5、財津桂6,7*
*責任著者
所属:1 愛知県警察本部科学捜査研究所、2 島津製作所、3 名古屋市衛生研究所、4 金城学院大学生活環境学部、5 国立研究開発法人 産業技術総合研究所、6 近畿大学生物理工学部、7 名古屋大学高等研究院
5. 研究詳細
研究グループは、PESI/MS/MSを用いた新たな尿中薬物のスクリーニング分析法「RaDPi-U」(Rapid-fire drug screening method by probe electrospray ionization tandem mass spectrometry (PESI/MS/MS) for human urine)を開発しました。対象成分として、規制薬物である覚醒剤や麻薬であるコカインに加え、ベンゾジアゼピン系睡眠薬や向精神薬などを中心に、薬物犯罪捜査において最も重要である40種類の薬物を選定しました。これまで研究グループは、PESI/MS/MSを用いて動物の脳試料などから対象成分を直接分析する手法などを多数報告(引用文献1~5)してきました。これらの経験を基に、尿試料から上記の40種類の薬物を直接分析する手法を開発しました。本分析法の手順を図1に示します。
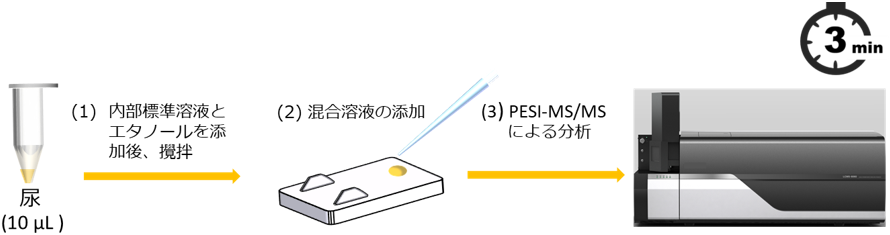
図1 RaDPi-Uでの分析の流れ
尿試料10μLに内部標準溶液(ジアゼパム-d5)および少量のエタノールを添加して1分間攪拌します。その後、専用のサンプルプレートに試料を入れてPESI/MS/MSの開始ボタンを押すだけで分析は完了し、結果が出力されます。特に、質量分析の際にScheduled-SRM法※7を用いることで多成分を一斉に分析することが可能となり、40種類の薬物について1.5分で質量分析を完了します。多成分の分析に少なくとも20分程度の時間を要するガスクロマトグラフィー質量分析(GC/MS)や液体クロマトグラフィータンデム質量分析(LC/MS/MS)といった質量分析法と比較して、RaDPi-Uでは極めて短時間で質量分析の結果を得ることに成功しました。
また、RaDPi-Uでは、対象となる40種類の薬物が尿試料に含まれていた場合、薬物濃度も同時に算出することが可能です。RaDPi-Uでは、各薬物について内部標準法※8を用いて正確な濃度を計測できることを、分析法バリデーション※9によって確認しています。最終的に、RaDPi-Uを用いて実際の尿検体3例を分析しました。例として図2に尿検体1の結果を示します。
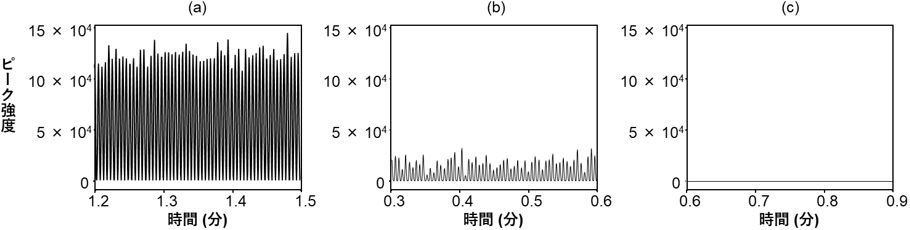
図2 検体1の尿試料より得られた結果の例。縦軸は薬物の検出強度を示す
(a)向精神薬リスペリドンが検出されている。(b)鎮咳薬ジヒドロコデインが検出されている。
(c)薬物(ここでは睡眠薬エチゾラム)が不検出の場合は波形が表示されない。
検体1の尿試料からは向精神薬リスペリドン(尿中濃度:143 ng/mL)と鎮咳薬ジヒドロコデイン(尿中濃度:101 ng/mL)、検体2の尿試料からは抗ヒスタミン薬ジフェンヒドラミン(尿中濃度:215 ng/mL)、検体3の尿試料からは鎮咳薬ジヒドロコデイン(尿中濃度:316 ng/mL)と睡眠薬ゾピクロン(尿中濃度:186 ng/mL)が検出され、RaDPi-Uは実検体から薬物を簡便かつ迅速に検出できることが示されました。
RaDPi-Uは、煩雑な試料調製を必要とせず、極めてユーザビリティの高い分析法であることに加え、質量分析に不慣れな人であっても分析結果を容易に得ることが可能です。よって今後、薬物犯罪捜査や薬物中毒における薬物分析に大きく貢献できる技術といえます。
6. 用語解説
- ※1 急性薬物中毒
- 薬物を過剰に摂取した場合、薬物によって引き起こされる急性中毒のこと。場合によっては死に至ることがあるため、摂取した人の尿試料などについて薬物分析を実施し、原因薬物を速やかに特定することが必要となる。
- ※2 薬物スクリーニング分析
- 摂取した薬物の見当を付けるために行う分析のこと。
- ※3 イムノアッセイ法
- 抗体抗原反応を利用した分析法のこと。薬物分析の場合、薬物を抗原と認識した抗体をキット化して、薬物の有無を判定する。操作性が高い一方で、特異性が低いため薬物の特定はできず、あくまで得られる結果は薬物種の推定に留まる。
- ※4 交差反応
- 特定の抗体が本来対象としている抗原以外のものにも反応してしまう現象のこと。結果として、偽陽性(誤判定)を引き起こす。
- ※5 質量分析法
- 分子をイオン化し、その質量電荷比(質量を電荷数で割ったもの)を測定することによって物質の特定を行う分析法のこと。化合物の同定法として極めて特異性が高い。
- ※6 探針エレクトロスプレーイオン化タンデム質量分析
- 先端直径700 nmの微細針を用いて試料の採取と質量分析を行うことが可能な技術であり、試料から対象成分を直接分析することが可能である。
- ※7 Scheduled-SRM法
- 質量分析法における手法の1つ。特定の時間において特定の対象成分だけを測定するように分析条件を設定することで、多成分を一斉に高感度検出することができるようになる。
- ※8 内部標準法
- 尿中の薬物濃度などを計測する際に用いられる手法のこと。予め準備した内部標準物質を尿試料に一定量加え、内部標準物質と対象成分の検出強度の比を用いて検量線を作成し、薬物濃度を計測する。
- ※9 分析法バリデーション
- 上述の内部標準法で作成した検量線が、薬物の濃度を正確に測定できるかを検証すること。
7. 引用文献
- Kei Zaitsu*, et al., Intact endogenous metabolite analysis of mice liver by probe electrospray ionization/triple quadrupole tandem mass spectrometry (PESI/MS/MS) and its preliminary application to in vivo real-time analysis. Analytical Chemistry. 2016. 88(7): 3556-3561.
- Kei Zaitsu*, et al., In vivo real-time monitoring system using probe electrospray ionization/tandem mass spectrometry (PESI/MS/MS) for metabolites in mouse brain. Analytical Chemistry. 2018. 90 (7): 4695-4701.
- Kei Zaitsu*, Akira Iguchi, et al., PiTMaP: A new analytical platform for high-throughput direct metabolome analysis by probe electrospray ionization/tandem mass spectrometry using an R software-based data pipeline. Analytical Chemistry. 2020. 92(12): 8514-8522.
- Kazuaki Hisatsune, Kei Zaitsu*, et al., RECiQ: A rapid and easy method for determining cyanide intoxication by cyanide and 2-aminothiazoline-4-carboxylic acid quantification in the human blood using probe electrospray ionization tandem mass spectrometry. ACS Omega. 2020. 5(36): 23351–23357.
- Akira Iguchi*, Kei Zaitsu*, et al., Single-polyp metabolomics for coral health assessment. Scientific Reports. 2024. 14:3369.
お問い合わせ
産業技術総合研究所