2024-04-12 理化学研究所,国立医薬品食品衛生研究所,新潟大学
理化学研究所(理研)生命医科学研究センター ファーマコゲノミクス研究チームの莚田 泰誠 チームリーダー、福永 航也 研究員(国立医薬品食品衛生研究所 医薬安全科学部 協力研究員)、国立医薬品食品衛生研究所 医薬安全科学部の斎藤 嘉朗 部長(研究当時、現 同研究所副所長)、新潟大学大学院 医歯学総合研究科の阿部 理一郎 教授らの共同研究グループは、関節リウマチ・潰瘍性大腸炎治療薬サラゾスルファピリジンの副作用である薬疹[1]の発症に、特定のHLAアレル[2]である「HLA-A*11:01」「HLA-B*39:01」「HLA-B*56:03」がそれぞれ独立して関連することを発見しました。
本研究で同定された三つのHLAアレルは、サラゾスルファピリジンによる薬疹の発症リスクを予測するバイオマーカー[3]としての活用が期待されます。
今回、共同研究グループは薬疹発症患者におけるHLA-A*11:01、HLA-B*39:01、HLA-B*56:03のうちいずれか一つでも保有している薬疹患者の割合は73%であり、日本人集団における保有率22%と比較して統計的に有意に高頻度であることを突き止めました。このことは、この三つをバイオマーカーとして用いることで、サラゾスルファピリジンによる薬疹患者の約4分の3を説明できることを示します。
本研究は、科学雑誌『The Journal of Allergy and Clinical Immunology: In Practice』オンライン版(4月11日付)に掲載されました。
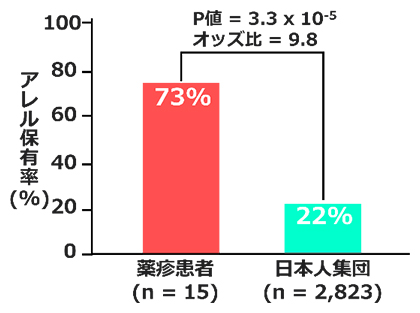
サラゾスルファピリジン誘発薬疹患者における三つのHLAアレルの保有率
背景
サラゾスルファピリジンは、関節リウマチ、潰瘍性大腸炎やクローン病の治療薬として広く使われていますが、副作用として一定の確率で薬疹が起こることが問題となっています。重症薬疹であるスティーヴンス・ジョンソン症候群(SJS)[4]や中毒性表皮壊死融解症(TEN)[5]、薬剤性過敏症症候群(DIHS)[6]に加えて、軽症薬疹である播種状紅斑丘疹型薬疹(MPE)[7]など多様なタイプの薬疹が存在し、症状や治療方法もさまざまです。いずれの薬疹も重篤化した場合、後遺症または死亡につながる可能性があります。
共同研究グループはこれまでに、サラゾスルファピリジンを含むサルファ剤による薬疹にはHLA-A遺伝子のアレルの一つであるHLA-A*11:01が関係することを見いだし、このアレルを持つ日本人の患者は、同アレルを持たない患者に比べて薬疹が9.8倍起こりやすいことを報告しました注1)。しかし、このアレルだけでは全ての患者の薬疹発症を予測することができませんでした。また、サルファ剤に共通の化学構造(スルホンアミド基)ではなく、サラゾスルファピリジンに特有の化学構造のみが原因の薬疹に関連する遺伝要因も不明でした。
そこで共同研究グループは、薬物治療開始前に薬疹の発症リスクを予測するバイオマーカーを同定するために、サラゾスルファピリジンによる薬疹患者のHLAアレルを対象に、詳細なゲノム解析を行いました。
注1)2020年1月28日プレスリリース「サルファ剤による重症薬疹のリスク因子を発見」
研究手法と成果
共同研究グループは、サラゾスルファピリジンによる薬疹患者15人のHLA-A、HLA-B、HLA-CおよびHLA-DRB1遺伝子のHLAアレルを調べ、日本人集団2,823人のデータと比較しました。対象とした薬疹患者のうち10人(67%)がHLA-A*11:01、6人(40%)がHLA-B*39:01、3人(20%)がHLA-B*56:03を保有しており、一般的な日本人集団における頻度より有意に高いことが分かりました(図1)。薬疹患者の中にはHLA-A*11:01やHLA-B*39:01など複数のアレルを1人で保有している患者もいることが分かりました。これらのHLAアレルのいずれか一つでも保有している薬疹患者の割合は73%であり、日本人集団における保有率22%と比較して統計的に有意に高頻度でした。また、薬疹の種類別に解析したところ、DIHS患者(10人)のHLA-A*11:01(P値[8]=2.7×10-4、オッズ比[9]=11.5)およびHLA-B*39:01(P値=1.2×10-5、オッズ比=22.2)の関連は特に強いことが分かりました。
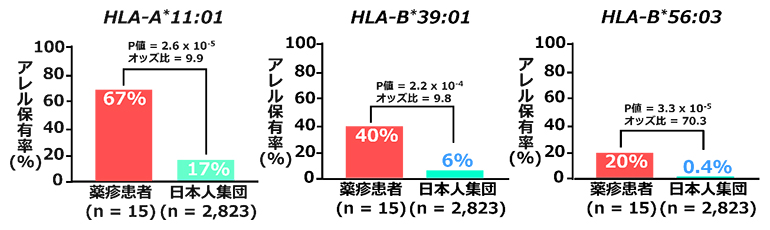
図1 薬疹患者におけるHLA-A*11:01、HLA-B*39:01、HLA-B*56:03の保有率
薬疹患者におけるHLA-A*11:01、HLA-B*39:01、HLA-B*56:03の保有率は、日本人集団における保有率と比較して、統計的に有意に高頻度であった。
HLA分子と薬物分子のドッキング・シミュレーション[10]により、特定のタイプのHLAに対する薬物の結合親和性を予測できます。サラゾスルファピリジン自体が体内に取り込まれる割合は少なく、腸管内で分解されてから吸収されます。そこで、サラゾスルファピリジンと、その代謝物であるスルファピリジン、スルファピリジン・ヒドロキシルアミン体、5-アミノサリチル酸のHLA-A*11:01、HLA-B*39:01、HLA-B*56:03との相互作用をそれぞれ解析したところ、いずれのHLA分子においてもサラゾスルファピリジンの結合自由エネルギー[11]が最も低く、結合親和性が高いことを推定しました(表1)。これはサラゾスルファピリジンの化学構造が薬疹を引き起こす原因である可能性を示唆しています。
| 薬物名 | 結合自由エネルギー(kcal/mol) | ||
|---|---|---|---|
| HLA-A*11:01 | HLA-B*39:01 | HLA-B*56:03 | |
| サラゾスルファピリジン | -8.32 | -8.48 | -8.73 |
| スルファピリジン | -6.47 | -6.50 | -7.01 |
| スルファピリジン・ヒドロキシルアミン体 | -6.83 | -6.51 | -7.32 |
| 5-アミノサリチル酸 | -5.32 | -6.27 | -5.95 |
表1 サラゾスルファピリジンとその代謝物のHLA分子への結合親和性
結合自由エネルギーが低いほど、それぞれの薬物とHLA分子の結合親和性が高いことを示す。サラゾスルファピリジンは他の代謝物に比べて、HLA-A*11:01、HLA-B*39:01、HLA-B*56:03の全てに対して結合が強いと推定される。
さらに、それぞれのHLA分子において、サラゾスルファピリジンが結合する確率が最も高い抗原提示部位[2]をシミュレーションしました(図2)。その結果、HLA-A*11:01とHLA-B*56:03では抗原提示部位のポケットA周辺に、HLA-B*39:01ではポケットF周辺にそれぞれ結合する可能性を明らかにしました。これは、HLA-A*11:01とHLA-B*56:03が引き起こす薬疹とHLA-B*39:01が引き起こす薬疹のメカニズムが異なっていることを示唆しています。
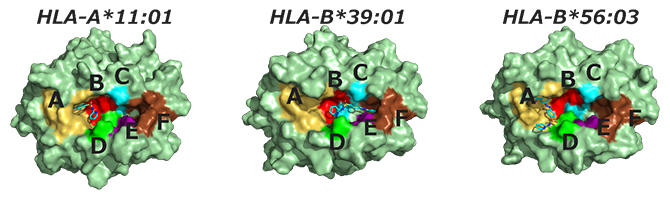
図2 サラゾスルファピリジンが結合する確率が最も高い抗原提示部位
それぞれのHLA分子の立体構造を示す。HLAにはA~Fのポケット状の抗原提示部位が存在する。サラゾスルファピリジンが結合する位置・角度を水色の化学構造で示した。
今後の期待
今回の研究結果から、HLA-A*11:01、HLA-B*39:01およびHLA-B*56:03のいずれかを保有する人は、保有しない人に比べてサラゾスルファピリジンによる薬疹を発症するリスクが高いことが示されました。薬疹発症患者における保有率から考えると、この三つのHLAアレルをバイオマーカーとして用いることで、サラゾスルファピリジンによる薬疹患者の約4分の3を説明できることになります。そこで、これらを組み合わせた遺伝子検査により、サラゾスルファピリジン治療開始前の薬疹発症リスクを予測し、治療薬の種類を替えることで副作用の回避が期待されます。
補足説明
1.薬疹
薬によって起こる皮膚や眼、口などの粘膜に現れる発疹。
2.HLAアレル、抗原提示部位
HLAアレルとはヒト白血球型抗原(HLA)を決定する遺伝子の型のこと。HLAは細胞表面に発現するタンパク質。免疫細胞による攻撃の目印となる抗原提示部位を持ち、多くの疾患の発症や副作用の発現のリスク因子であることが報告されている。HLA遺伝子には多くの種類が存在し、さらにそれぞれの遺伝子が数十種類の異なるタイプを持つ。アレルとは対立遺伝子のことで、同一の遺伝子座にありながらDNA塩基配列に差がある変異体を指す。HLA-A*11:01やHLA-B*39:01、HLA-B*56:03はHLAアレルの一つ。HLAはhuman leukocyte antigenの略。
3.バイオマーカー
疾患の発症や進行の予測に役立つ生体由来の物質のこと。特定の遺伝子配列や血液中のタンパク質や代謝産物などが対象になる。
4.スティーヴンス・ジョンソン症候群(SJS)
高熱(38℃以上)を伴って、発疹・発赤、火傷のような水ぶくれなどの激しい症状が、比較的短期間に全身の皮膚、口、目の粘膜に現れる病態。その多くは医薬品が原因と考えられており、原因となる医薬品は抗菌薬、解熱消炎鎮痛薬、抗けいれん薬などの広範囲にわたる。SJSはStevens-Johnson syndromeの略。
5.中毒性表皮壊死融解症(TEN)
全身の体表面積の10%を超える火傷のような水ぶくれ、皮膚の剝がれ、ただれなどが認められ、高熱(38℃以上)、目が赤くなるなどの症状を伴う重症の皮膚障害。中毒性表皮壊死融解症の症例の多くが、スティーヴンス・ジョンソン症候群の進展型と考えられている。TENはtoxic epidermal necrolysisの略。
6.薬剤性過敏症症候群(DIHS)
高熱(38℃以上)を伴って、全身に赤い斑点が見られ、さらに全身のリンパ節(首、わきの下、股の付け根など)が腫れたり、肝機能障害などの血液検査値の異常が見られたりする重症の皮膚障害。通常の薬疹とは異なり、原因となる医薬品の服用後すぐには発症せずに2週間以上経ってから発症することが多い。DIHSはdrug-induced hypersensitivity syndromeの略。
7.播種状紅斑丘疹型薬疹(MPE)
体幹・四肢近囲部に対称的な大小の紅斑が播種(はしゅ)状に多発し、しばしば融合するなどの症状を伴う軽症の皮膚障害。軽症であるがSJS/TENやDIHSに進展する場合があるので注意を要する。薬疹の臨床病型の中で最も頻度が高い。MPEはmaculopapular exanthemaの略。
8.P値
ある試験において、二つの群間の差が偶然生じる可能性を示す指標であり、小さいほど2群間の差が偶然によらず生じている可能性が高い。通常の統計解析では、P値が0.05未満である場合、統計的に意味があると判断する。これは、ある結果を偶然生じることが100回に5回未満であることを意味するが、複数回解析を行うと、全く関係がなくても偶然に関係があると誤って判断されてしまう場合がある。そこで本研究では、通常の判定基準である0.05を解析した回数で割った0.05/N回未満(今回の場合は0.05 / 56 = 8.93 x 10-4)という厳しい判定基準を採用している。
9.オッズ比
発症リスクの大きさの指標。健常者の集団のリスク要因を持つ人の割合(オッズ)に対する、発症患者でリスク要因を持つ人の割合の比で表す。
10.ドッキング・シミュレーション
薬物分子が薬理作用を発現するためには、薬理作用に密接に関わる生体内の標的分子(酵素や受容体など)と直接的に相互作用する必要がある。コンピュータを用いて、このような相互作用の強さ(結合親和性)を予測する手法がドッキング・シミュレーションである。
11.結合自由エネルギー
タンパク質(HLA分子)と化合物(サラゾスルファピリジンなどの薬物)の結合に伴うエネルギー変化であり、タンパク質と化合物の結合の強さを示している。結合を切るのに必要なエネルギーであり、常にマイナスの値である。絶対値が大きいほど、結合が強いことを示す。
共同研究グループ
理化学研究所 生命医科学研究センター ファーマコゲノミクス研究チーム
チームリーダー 莚田 泰誠(ムシロダ・タイセイ)
研究員(研究当時)大関 健志(オオゼキ・タケシ)
研究員 福永 航也(フクナガ・コウヤ)
(国立医薬品食品衛生研究所 医薬安全科学部 協力研究員)
国立医薬品食品衛生研究所 医薬安全科学部
部長(研究当時)斎藤 嘉朗(サイトウ・ヨシロウ)
(現 国立医薬品食品衛生研究所 副所長)
室長 中村 亮介(ナカムラ・リョウスケ)
研究員(現 主任研究官)塚越 絵里(ツカゴシ・エリ)
藤田医科大学 医学部 アレルギー疾患対策医療学講座
教授 松永 佳世子(マツナガ・カヨコ)
厚生労働省難治性疾患等政策研究事業(難治性疾患政策研究事業)重症多形滲出性紅斑に関する調査研究班
昭和大学 横浜市北部病院 皮膚科
教授 渡辺 秀晃(ワタナベ・ヒデアキ)
杏林大学 医学部 皮膚科学教室
教授 水川 良子(ミズカワ・ヨシコ)
講師 倉田 麻衣子(クラタ・マイコ)
横浜市立大学大学院 医学研究科 環境免疫病態皮膚科学
教授 山口 由衣(ヤマグチ・ユキエ)
講師 渡邉 裕子(ワタナベ・ユウコ)
島根大学 医学部 皮膚科学講座
教授(研究当時)森田 栄伸(モリタ・エイシン)
講師 新原 寛之(ニイハラ・ヒロユキ)
奈良県立医科大学 皮膚科学教室
教授 浅田 秀夫(アサダ・ヒデオ)
新潟大学大学院 医歯学総合研究科 皮膚科学分野
教授 阿部 理一郎(アベ・リイチロウ)
講師 濱 菜摘(ハマ・ナツミ)
助教 長谷川 瑛人(ハセガワ・アキト)
研究支援
本研究の一部は、厚生労働科学研究費補助金 難治性疾患政策等研究事業(難治性疾患政策研究事業)「重症多形滲出性紅斑に関する調査研究(研究代表者:阿部理一郎)」による支援を受けて行われました。
原論文情報
Koya Fukunaga, Eri Tsukagoshi, Ryosuke Nakamura, Kayoko Matsunaga, Takeshi Ozeki, Hideaki Watanabe, Akito Hasegawa, Natsumi Hama, Maiko Kurata, Yoshiko Mizukawa, Yuko Watanabe, Yukie Yamaguchi, Hiroyuki Niihara, Eishin Morita, Hideo Asada, Riichiro Abe, Yoshiro Saito, Taisei Mushiroda., “Association of HLA-A*11:01, HLA-B*39:01 and HLA-B*56:03 with salazosulfapyridine-induced cutaneous adverse drug reactions”, The Journal of Allergy and Clinical Immunology: In Practice, 10.1016/j.jaip.2024.02.041
発表者
理化学研究所
生命医科学研究センター ファーマコゲノミクス研究チーム
チームリーダー 莚田 泰誠(ムシロダ・タイセイ)
研究員 福永 航也(フクナガ・コウヤ)
(国立医薬品食品衛生研究所 医薬安全科学部 協力研究員)
国立医薬品食品衛生研究所 医薬安全科学部
部長(研究当時)斎藤 嘉朗(サイトウ・ヨシロウ)
(現 国立医薬品食品衛生研究所 副所長)
新潟大学大学院 医歯学総合研究科
教授 阿部 理一郎(アベ・リイチロウ)
報道担当
理化学研究所 広報室 報道担当
国立医薬品食品衛生研究所 業務課業務係
新潟大学 広報事務室