2024-09-15 東京大学
発表のポイント
◆p53ノックアウト細胞にERGを導入することにより、ヒト赤白血病の病態を再現した実験モデルを開発しました。
◆ERGが赤血球系遺伝子の発現抑制を介して赤血球分化を抑えること、p53欠失が赤血球系細胞の増殖を促進すること、両者が協調することで赤白血病の発症を誘導することを明らかにしました。
◆赤白血病の治療標的として、HDAC7を同定しました。既存の白血病治療薬がほとんど効かない赤白血病に対する新しい治療法の開発に貢献することが期待されます。
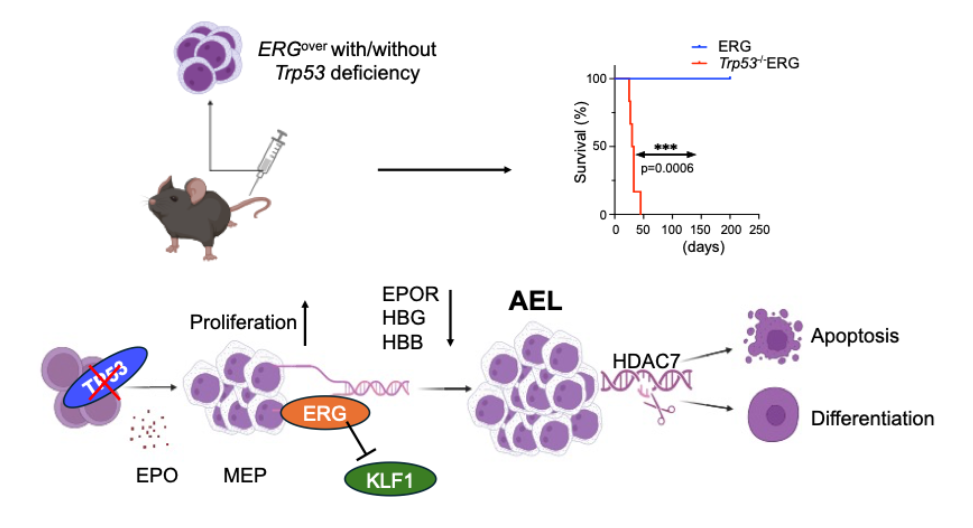
赤白血病モデルの作製と治療標的の同定
発表概要
東京大学大学院新領域創成科学研究科メディカル情報生命専攻先進分子腫瘍学の合山進教授、張分宇(ちょうぶんう)特任研究員(研究当時)、北村俊雄東京大学名誉教授らによる研究グループは、p53(注1)ノックアウトマウスから採取した骨髄細胞に転写因子ERG(注2)を導入して移植することにより、難治性で知られるヒト赤白血病の病態を再現したマウスモデルを作製しました。またメカニズムとして、ERGが赤血球分化を抑制していること、p53欠失が赤血球系細胞の増殖を促進すること、そして両者が協調して赤白血病の発症を誘導することを明らかにしました。さらに、赤白血病の治療標的としてHDAC7を同定しました。
これらの成果は、難治性で知られる赤白血病に対する新しい治療法の開発に貢献することが期待されます。
発表内容
<研究の背景>
急性赤白血病(注3)は、幼弱な赤芽球(注4)の増殖を特徴とする白血病です。最近のゲノム解析により、赤芽球系白血病細胞の割合が8割を超える難治症例の大部分でがん抑制遺伝子p53の変異が認められ、また転写因子ERGの高発現が高頻度に共存することが明らかとなっています。p53変異を持つ赤白血病は、現在の白血病治療薬がほとんど効かないため予後が極めて悪く、臨床上の大きな問題となっています。
本研究では、この難治性赤白血病に対する新しい治療法の開発を目的として、赤白血病の病態を再現するマウスモデルの作製と赤白血病の治療を可能とする新しい治療標的の探索に取り組みました。
<研究の内容>
ヒト赤白血病の病態を再現し、かつ遺伝子操作を容易に行うことのできるマウスモデルを作製するため、Cas9(注5)発現マウスとp53ノックアウトマウスを交配したp53-/-/Cas9マウスから採取した骨髄細胞に転写因子ERGを導入し、試験管内で培養可能で、マウス内で赤白血病を発症し、かつ任意の遺伝子を簡便にノックアウトすることのできるCas9発現赤白血病細胞(Cas9/ERG発現p53欠失細胞:CEP53細胞と命名)を作製しました(図1左)。また、このCEP53細胞や赤血球系のヒト白血病細胞を用いてRNA-Seq解析(注6)やChIP-Seq解析(注7)を行い、転写因子ERGが赤血球系遺伝子の発現抑制を介して赤血球分化を抑制すること、p53欠失が赤血球系細胞の増殖を促進すること、両者が協調することで赤白血病の発症を誘導することを明らかにしました。そして、赤白血病細胞の増殖・分化を制御する分子としてヒストン脱アセチル化酵素HDAC7(注8)を同定し、HDAC7欠失がヒト赤白血病細胞やCEP53細胞の分化を誘導し、赤白血病の発症を抑制することを見出しました(図1右)。ただし、HDAC7の酵素活性は赤白血病細胞の増殖には必要無く、HDAC7はヒストン脱アセチル化以外の機能を介して赤白血病細胞の増殖を促進していると考えられます。
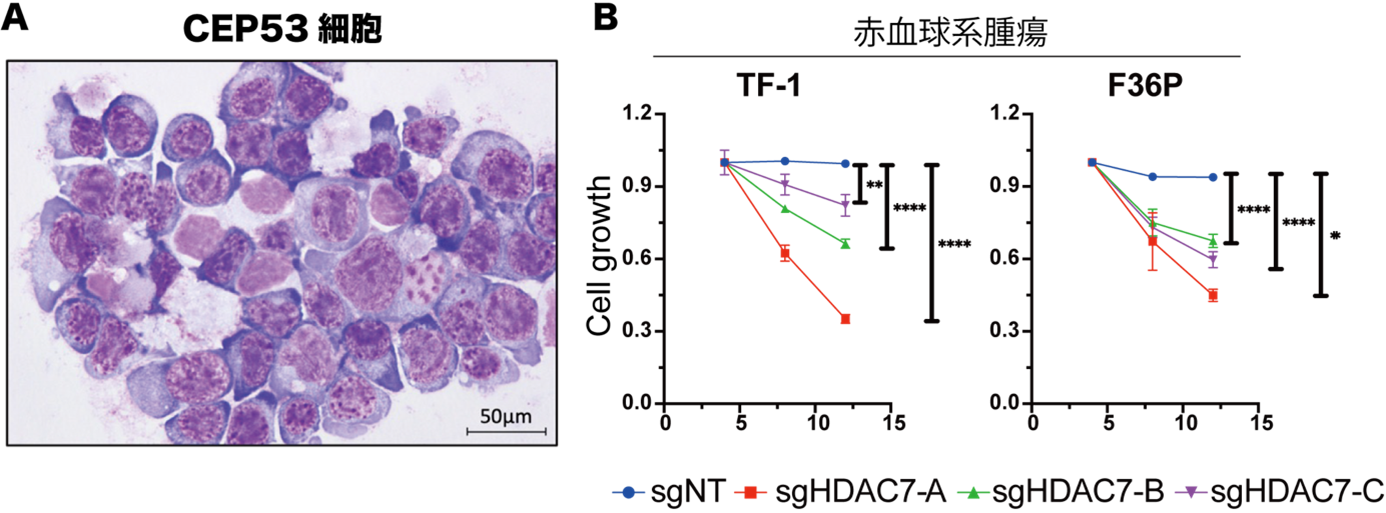
図1:赤白血病モデルの作製と治療標的の同定
A.Cas9+p53-/-骨髄細胞にERGを導入し、赤白血病細胞(CEP53細胞)を作製した。
B.赤血球系ヒト白血病細胞においてHDAC7をノックアウトすると、その増殖が低下した。
<今後の展望>
本研究で樹立したCEP53細胞は、今後赤白血病研究を進める上で貴重な実験ツールになると考えられます。また、HDAC7分解誘導薬を開発すれば、難治性で知られる赤白血病に対する画期的な治療薬となることが期待されます。
<研究助成>
本研究は、科研費「基盤研究B(課題番号:22H03100)」、「挑戦的研究(萌芽)(課題番号:21H00274、19H04756)」、「国際共同研究強化(B)(課題番号:22KK0127)」、「基盤研究A(課題番号:20H03537)」、「若手研究B(課題番号:22K16319)」、AMED(課題番号:22ck0106644s0202、23ama221514h0002、23ama221223)、日本血液学会、高松宮妃癌研究基金、第一三共生命科学研究振興財団、小林がん学術振興会の支援により実施されました。
発表者・研究者等情報
東京大学大学院新領域創成科学研究科 メディカル情報生命専攻 先進分子腫瘍学分野
合山 進 教授
張 文宇(ちょう ぶんう) 特任研究員(研究当時)
東京大学
北村 俊雄 名誉教授 兼 神戸医療産業都市推進機構 先端医療研究センター センター長
論文情報
雑誌名:Leukemia
題 名:HDAC7 is a potential therapeutic target in Acute Erythroid Leukemia
著者名:Wenyu Zhang, Keita Yamamoto, Yu-Hsuan Chang, Tomohiro Yabushita, Yangying Hao, Ruka Shimura, Jakushin Nakahara, Shiori Shikata, Kohei Iida, Qianyi Chen, Xichen Zhang, Toshio Kitamura, Susumu Goyama*
DOI: 10.1038/s41375-024-02394-5
URL: https://www.nature.com/articles/s41375-024-02394-5
用語解説
(注1)p53
細胞周期や細胞死、DNA損傷修復の制御に関与する転写因子で、がんの発症、進展を抑制するがん抑制遺伝子としての役割を持つ。
(注2)ERG
ETSファミリーに属する転写因子で、胚発生、細胞増殖、分化、そして細胞死の制御に関与している。前立腺がん、ユーイング肉腫、急性骨髄性白血病などの発症に関与するがん遺伝子でもあり、p53変異を持つ赤白血病では高頻度に活性化されている。
(注3)急性赤白血病
急性骨髄性白血病の一種で、幼弱な赤芽球の顕著な増殖を特徴とする稀な白血病。特にp53変異を持ち赤芽球の割合が高い赤白血病の予後は極めて悪いことが知られている。
(注4)赤芽球
造血幹細胞が分化・成熟して赤血球になる過程で出現する未熟な細胞。主に骨髄中に存在する。赤芽球が成熟すると赤血球となり、血液中に放出される。
(注5)Cas9
特定のDNA配列を切断する酵素で、ゲノム編集技術「CRISPR-Cas9」において重要な役割を果たす。ガイドRNAと呼ばれる短いRNA配列と結合し、そのガイドRNAがDNA内の特定の配列を認識すると、Cas9がその場所でDNAを切断する。この技術を利用することで、Cas9発現細胞内の特定の遺伝子を自在に切断(ノックアウト)することが可能となる。
(注6)RNA-seq解析
次世代シーケンサーを用いて、細胞の中の遺伝子発現を網羅的かつ定量的に解析する手法。
(注7)ChIP-Seq解析
クロマチン免疫沈降(Chromatin ImmunoPrecipitation: ChIP)アッセイとシーケンス(Seq)を組み合わせた実験手法で、転写因子のDNA結合部位を同定することができる。
(注8)HDAC7
タンパク質のリジン残基のアセチル基を取り除く酵素:ヒストン脱アセチル化酵素(HDAC)ファミリーに属する酵素の一種。ただし赤白血病の増殖には酵素活性が必要無く、HDAC7は他の機序を介して赤白血病の増殖を制御していると考えられる。
お問い合わせ
新領域創成科学研究科 広報室