2024-06-11 大阪大学
掲載誌 Nature Genetics
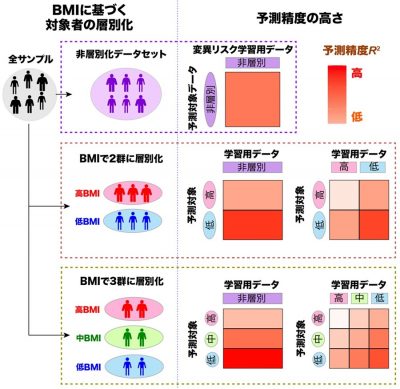
図1: 本研究の概要
研究成果のポイント
- 肥満ではない集団において2型糖尿病の遺伝的なリスク予測がしやすいことを発見。また、日本人集団と欧米人集団の遺伝的な違いを補正する機械学習手法と組み合わせることで予測精度を向上。
- 日本人集団に多い非肥満2型糖尿病は、これまでゲノム情報があまり詳しく調べられていなかったが、大規模ゲノム解析によって、インスリン分泌に影響する遺伝因子が背景にあることを実証。
- 糖尿病予防や合併症防止といった将来的な個別化医療へ貢献すると期待される。
概要
大阪大学大学院医学系研究科の小嶋崇史さん(遺伝統計学 博士課程/東北大学大学院医学系研究科AIフロンティア新医療創生分野 特別研究学生/理化学研究所生命医科学研究センター システム遺伝学チーム 研修生/理化学研究所革新知能統合研究センター遺伝統計学チーム 研修生)、岡田随象教授(遺伝統計学/東京大学大学院医学系研究科 遺伝情報学 教授/理化学研究所生命医科学研究センター システム遺伝学チーム チームリーダー)、東京大学大学院医学系研究科の山内敏正教授、門脇孝東京大学名誉教授、東北大学東北メディカル・メガバンク機構の田宮元教授(理化学研究所革新知能統合研究センター遺伝統計学チーム チームリーダー)らの共同研究グループは、体格指数(BMI)を使用することで2型糖尿病の遺伝的リスク予測精度が向上することを発見しました(図1)。
さらに、集団間の遺伝的な違いを補正できる機械学習手法を組み合わせることで、欧米人集団の豊富なゲノム情報を活用して、日本人集団に対する予測精度のさらなる向上を実現しました。 また、ゲノム解析により、2型糖尿病になりやすい遺伝的体質に関わるメカニズムを明らかにしました。
ゲノム全体の遺伝子変異から算出した2型糖尿病のポリジェニック・リスク・スコア(polygenic risk score;PRS)※1は、発症予測や予防に役立つ手段として臨床応用が期待されています。しかし、2型糖尿病が不均一な疾患であることや、ゲノム情報が多く集積している欧米人集団との遺伝的な違いによって、本邦における将来的なゲノム医療の質が低くなることが危惧されています。今回の研究成果は、2型糖尿病の遺伝的リスク予測制度を向上するとともに、将来的に、糖尿病予防や合併症予防といった個別化医療へ貢献することが期待されます。
本研究の背景
2型糖尿病は失明・神経障害・腎不全・脳卒中・心筋梗塞など、多くの合併症を起こす重大な病気であり、日本国内で1000万人以上の患者がいると言われています。2型糖尿病の発症には、加齢・肥満などの「環境因子」の他に、各個人の「遺伝因子」も重要であることが知られています。
近年、数百の遺伝的変異が2型糖尿病のかかりやすさに影響することが、ゲノムワイド関連解析(Genome-Wide Association Study;GWAS)※2によって分かってきました。これらの遺伝子変異を積算することで算出されるポリジェニック・リスク・スコア(PRS)は、2型糖尿病にかかりやすい遺伝的体質を反映します。そのためPRSは個々人の遺伝的体質に合わせて、糖尿病の発症や合併症を防止する個別化医療の有効な手段として期待されています。
しかし、日本で2型糖尿病PRS予測を臨床応用するためには、予測精度を低下させる2つの重大な問題を解決する必要があると考えられています。第一に、2型糖尿病がBMI分布や遺伝性の異なるいくつかのサブタイプ※3が集まった不均一な病気であり、遺伝率※4の低いサブタイプが予測を低下させる懸念があることです。第二に、ゲノム情報が多く蓄積されている欧米人集団と、比較的ゲノム情報が少ない日本人集団との間で、遺伝的な違いがあることです。これは、欧米人集団に比べて、将来的に日本のゲノム医療の質が劣ることになる「国際間の健康格差」として指摘されています。
これらの問題に対して、本研究グループは遺伝的に予測したい対象集団をBMIが高い群/低い群といったように層別化することで、予測精度がどのように変化するのか調べました。さらに、このBMI層別化に加えて、集団間の遺伝的な違いを調整する機械学習手法を組み合わせることで、日本人集団における予測の向上を目指しました(図2)。
本研究の成果
まず、本研究グループは、対象集団をBMIが高い群/低い群といったように層別化することで、2型糖尿病患者のサブタイプを疑似的に分け、PRS予測がどのように変わるのかを調べました。バイオバンク・ジャパン(BBJ)※5および英国のUKバイオバンク(UKBB)※6の参加者である2型糖尿病患者55,284人と非糖尿病群140,484人で構成されるゲノムデータセットでBMI層別化による影響を評価しました。
その結果、糖尿病の発症しやすさを反映するPRSの予測精度は、BMI低値群で高精度であることを発見しました。また、予測対象集団のBMI層別化は予測精度を高める一方で、学習データではサンプル数の多さが予測精度を高めるという性質も明らかになりました。PRSは遺伝率との関わりが深いため、BMIが高い群/低い群それぞれで遺伝率を算出したところ、BMIが低い群において遺伝率が高く、これがPRS予測にも影響していることが分かりました。
どのような生物学的メカニズムでBMI低値群における糖尿病の遺伝的予測精度が高いのかを調べたところ、膵臓からのインスリン分泌不全に関わる遺伝子群が影響していることが分かりました。さらに、BMIが低い糖尿病患者では神経障害と網膜症の合併率が高く、適切な治療薬選択による合併症予防の重要性が示唆されました。これらの結果は重症インスリン欠乏型糖尿病(severe insulin-deficient diabetes;SIDD) ※7という糖尿病サブタイプの特徴と類似しており、BMI低値群に遺伝性の高いSIDD患者が集中したことが遺伝的リスク予測を向上した一因と考えられます。
次に、BMI高値群/低値群といった層別化に加えて、集団間の遺伝的な違いを調整できる機械学習手法(PRS-CSx)を組み合わせることで日本人集団における予測精度の向上を目指しました。その結果、「BMI層別化による予測精度向上」と「PRS-CSxによる予測精度向上」の双方が相乗的に予測精度を高め、同一集団内のBMI非層別化予測と比較してBBJでは37.4%の予測精度向上を達成しました(図3)。この結果は、BBJとUKBBの学習データ統合による人数増加が予測を向上したことを示しており、今後のゲノム医療の発展にはゲノムコホートの参加人数の拡大が重要であると考えられます。
最後に、東北メディカル・メガバンク計画※8とBBJ 2次コホートの2型糖尿病患者17,236人と対照群41,860人を対象とした再現性検証においても、BMI25以下の集団では遺伝的予測精度が高い傾向が確認されました。これらの結果は、PRS予測のように多くのゲノム情報が必要な解析において、BBJ2次コホートのように既存コホートを拡張することや、東北メディカル・メガバンク計画とBBJのような国内の複数コホートが車の両輪のように協調しながら研究を前進させることの重要性を示しています。

図2: 各バイオバンクと予測手法の組み合わせ

図3: バイオバンク横断的なBMI層別化による2型糖尿病の予測精度の変化
本研究が社会に与える影響(本研究成果の意義)
本研究では、2型糖尿病の遺伝的リスク予測に関する問題を解決する糸口を示し、糖尿病になりやすい遺伝的体質に関わるメカニズムを明らかにしました。本研究の成果は、将来的に、日本の糖尿病・合併症予防に関する個別化医療、個別化予防※9の質を高めることに貢献すると期待されます。
研究者コメント
<小嶋 崇史さん(大学院生)のコメント>
ゲノム医療への期待は年々高まっており、特にPRS予測に基づく個別化予防は医療費抑制といった観点でも注目され、医療現場への導入がさかんに議論されています。私たちの研究が、糖尿病の遺伝的リスク体質への理解を深め、PRSの臨床応用に貢献し、患者さんのために役立つことを願っております。
また、今回の研究成果はバイオバンク・ジャパンや東北メディカル・メガバンク計画といった複数の大規模ゲノムコホートの協力により実現できました。こうした国内のゲノムコホートをさらに拡充すること、そしてコホート間の連携を強化することが、日本における今後のゲノム医療の質を高める重要な鍵となるでしょう。本研究にご協力いただいた全ての共同研究者や研究支援機構、そしてコホート参加者の皆様に深く感謝を申し上げます。今後もゲノム医療に関する研究を進め、成果を通じて皆様に還元していきたいと考えております。
用語説明
※1 ポリジェニック・リスク・スコア(polygenic risk score;PRS)
ヒトゲノム配列上に存在する数百万カ所の遺伝子変異のうち、疾患との関連が示唆された数十〜数十万の遺伝子変異について、効果量の重み付きの和を個人ごとに計算したスコア。このスコアは実際の疾患発症リスクと相関することが示されており、スコアを計算することで疾患にかかりやすい遺伝的体質を持っているかどうか調べることができる。
※2 ゲノムワイド関連解析(Genome-Wide Association Study;GWAS)
ヒトゲノム配列上に存在する数百万~数千万の遺伝子変異を対象に、疾患や検査値との関連を網羅的に探索する統計学的手法。ポリジェニック・リスク・スコアに用いられる遺伝子変異の効果量は、大規模なゲノムワイド関連解析研究をもとに算出される。
※3 サブタイプ
臨床的に同じ診断をされる2型糖尿病であっても、その原因や特徴の違いによって分類したものをサブタイプと呼ぶ。近年では、2型糖尿病は複数サブタイプが不均一に混ざり合った病態と考えられ、サブタイプをゲノムや臨床情報から推定して適切な治療法を選択する重要性が高まっている。
※4 遺伝率
特定の病気を発症する要因のうち、遺伝的要因がどの程度の割合を占めるのかを測る尺度のこと。一般的に遺伝率が高い疾患やサブタイプほどPRS予測精度も高い傾向にある。
※5 バイオバンク・ジャパン(BBJ)
日本人集団27万人を対象とした生体試料バイオバンクであり、ゲノムDNAや血清サンプルを臨床情報とともに収集・管理しており、研究者や企業へのデータ提供や分譲を行っている。2003年からの10年間で集められた1次コホートと2013年からの5年間で集められた2次コホートで構成される。病院で診断された患者で構成される疾患バイオバンクであるため、患者数が多いほど精度が上がるPRSの学習データに適する。(https://biobankjp.org/index.html)
※6 UKバイオバンク(UKBB)
英国の40~69歳の50万人を対象とした世界最大規模の生体試料バイオバンク。世界中の研究者にリソースを提供しており、がん、心血管疾患、糖尿病、認知症などさまざまな疾患の遺伝的・環境的要因の解明に貢献している。(https://www.ukbiobank.ac.uk/)
※7 重症インスリン欠乏型糖尿病(severe insulin-deficient diabetes;SIDD)
スウェーデンの研究者Ahlqvistが提唱した、インスリン分泌が非常に少ない一部の糖尿病サブタイプのこと。BMIが比較的低く、神経障害や網膜症といった合併症を併発しやすく、PRSでの予測精度が高いことが知られている。
※8 東北メディカル・メガバンク計画
日本人集団15万人を対象とした生体試料バイオバンクであり、ゲノムDNAや血清サンプルを臨床情報とともに収集・管理しており、研究者や企業へのデータ提供や分譲を行っている。東日本大震災の被災地域住民の健康情報やゲノム情報をもとに医療復興に取り組んでいる。一般集団から集められた前向きコホートであるため、PRSの予測対象集団として適する。(https://www.megabank.tohoku.ac.jp/)
※9 個別化医療、個別化予防
疾患ごとに決まった医療を行うのではなく、患者ひとりひとりに対して最適化された医療・予防を行うこと。
特記事項
本研究成果は、2024年6月11日(火)18時(日本時間)に米国科学誌「Nature Genetics」(オンライン)に掲載されました。
【タイトル】
“Body mass index stratification optimizes polygenic prediction of type 2 diabetes in cross-biobank analyses.”
【著者名】
Takafumi Ojima1,2,11,13, Shinichi Namba1, Ken Suzuki1,14, Kenichi Yamamoto1,4,5,6, Kyuto Sonehara1,7, Akira Narita8, the Tohoku Medical Megabank Project Study Group※, the Biobank Japan Project※, Yoichiro Kamatani9, Gen Tamiya2,8,10, Masayuki Yamamoto2,8, Toshimasa Yamauchi3, Takashi Kadowaki3,11, Yukinori Okada1,5,7,12,13
- 大阪大学 大学院医学系研究科 遺伝統計学
- 東北大学 大学院医学系研究科
- 東京大学 大学院医学系研究科 糖尿病代謝内科
- 大阪大学 大学院医学系研究科 小児科学
- 大阪大学 免疫学フロンティア研究センター(IFReC) 免疫統計学
- 大阪大学 大学院医学系研究科 保健学専攻 生命育成看護科学
- 東京大学 大学院医学系研究科 遺伝情報学
- 東北大学 東北メディカル・メガバンク機構
- 東京大学 大学院新領域創成科学研究科 複雑形質ゲノム解析分野
- 理化学研究所 革新知能統合研究センター
- 虎の門病院
- 理化学研究所 生命医科学研究センター
- 大阪大学ヒューマン・メタバース疾患研究拠点(PRIMe)
- 東京大学 医学部附属病院 糖尿病代謝内科*各バイオバンク研究グループ全員のリストは論文中に記載
DOI:10.1038/s41588-024-01782-y
本研究は、JSPS科研費JP22H00476、国立研究開発法人日本医療研究開発機構(AMED)JP23km0405211, JP23km0405217, JP23ek0109594, JP23ek0410113, JP23kk0305022, JP223fa627002, JP223fa627010, JP233fa627011, JP23zf0127008, JP23tm0524002、国立研究開発法人科学技術振興機構(JST)ムーンショット型研究開発事業JPMJMS2021, JPMJMS2024、JST 次世代研究者挑戦的研究プログラムJPMJSP2138、大阪大学卓越大学院プログラム教育研究支援経費、武田科学振興財団、大阪大学感染症総合教育研究拠点(CiDER)、大阪大学ワクチン開発拠点先端モダリティ・DDS研究センター(CAMaD)の支援を受けて行われました。