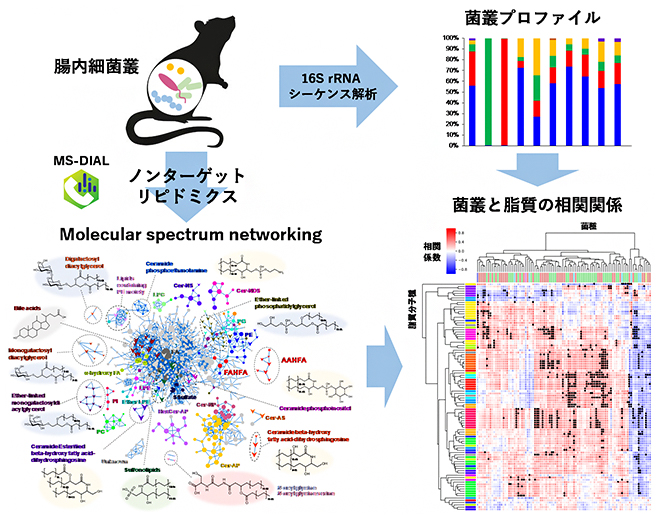
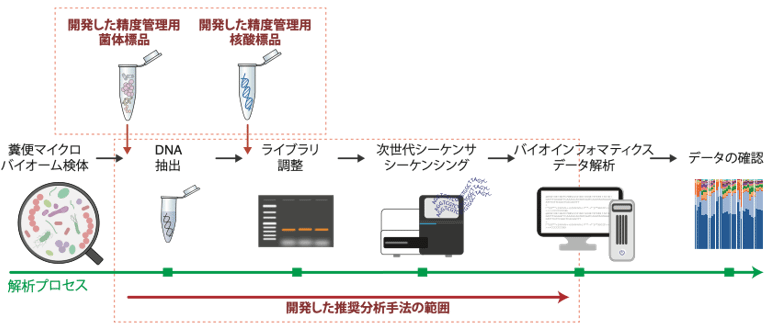
がん間質制御による新規治療法への可能性
2021-04-28 順天堂大学
順天堂大学 大学院医学研究科 呼吸器内科学の高橋和久 教授、十合晋作 准教授、岩井萌 大学院生ら、および理化学研究所予防医療・診断技術開発プログラム(PMI)林崎良英 プログラムディレクター (研究当時 現:株式会社ダナフォーム)、伊藤昌可 コーディネーター、川路英哉 コーディネーター (現:東京都医学総合研究所) らの共同研究チームは、肺がんの多くを占める「非小細胞肺がん*1」のがん関連線維芽細胞(CAF: Cancer-associated fibroblast)*2に対して「CAGE法*3」を用いた遺伝子発現の網羅的な解析を行い、細胞接着分子のインテグリンα11*4を介するCAFの活性化機序を解明しました。従来の研究はがん細胞の遺伝子変異やそのシグナルに着目したがん進展機序の研究が多く、本研究のようにがん間質*5におけるCAFの遺伝子発現を網羅的に解析し、その機能活性化制御因子を同定した報告はほとんどありません。本成果によりがん間質を標的とした新しい治療法の開発につながることが期待されます。本論文は学術誌Molecular Oncology 誌オンライン版にて公開されました。
本研究成果のポイント
- 非小細胞肺がんのがん関連線維芽細胞(CAF)の表現型解析としてCAGE法を用いたプロモーター活性の定量解析を実施
- インテグリンα11 、コラーゲンタイプXIαIの発現がCAFにおいて増加し、CAFの遊走能*6を活性化させた
- インテグリンα11+/コラーゲンタイプXIαI + CAFはがん間質を対象とした新たな治療法の標的として期待される
背景
近年、非小細胞肺がんは肺がんの多くを占め、国内におけるがん死亡原因の第1位となっています。昨今では分子標的治療薬の導入により薬剤療法の効果が認められるようになりましたが、非小細胞肺がんは予後が悪く、ほぼ全例で再発することが課題となっています。その理由はがん細胞とがん間質を含めた肺がん組織において、薬剤感受性の多様性が存在するためと考えられます。また、がん間質の量やがん間質における線維芽細胞の増殖能の高さが予後の悪化と強く相関することから、がん間質の制御の重要性が指摘され始めています。高い治療効果を得るためには、「がん関連肺線維芽細胞(CAF)」と称される、がん間質を主に構成している線維芽細胞の機能を制御する因子の解明が必要と考えられます。そこで本研究では、このCAFの機能活性に直接関与する特異的制御因子を明らかにするため、理化学研究所が独自に開発したCAGE法を用いて、CAFの遺伝子発現を網羅的に探索しました。
内容
本研究では、まず、がん間質中に集まるCAFの遊走能について検討を行いました。CAFは、周囲のがん細胞と相互に影響を及ぼしあう環境下において活性化し、がん細胞の進展を促進させます。CAFの遊走能を検討した結果、がん間質から分離したCAFは、正常肺分離した正常肺線維芽細胞と比較して、がん間質中の主要な構成たんぱく質であるI型コラーゲンやフィブロネクチンに向かう遊走能が活性化していることを発見しました。
つぎに、このCAFに特異的な遊走能の活性化に関与している機能制御因子を探るため、CAGE法による転写プロモーター活性の網羅的解析を行いました。その結果、下記5点の新しい知見が得られました。
I型コラーゲンの受容体であるインテグリンα11がCAFで高活性であること。
たんぱく質の発現レベルにおいてCAFでインテグリンα11の発現が増加していること(図1)。

図1:がん関連線維芽細胞のインテグリンα11の発現
正常線維芽細胞(Control)と比較してCAFでインテグリンα11のたんぱくレベルでの発現が増加していた。
さらにCAFを含むがん間質組織中のインテグリンα11の発現が高いほど術後再発を起こしやすく、進行病期によってその発現量が増加することから、インテグリンα11の発現と予後の悪化との相関性が確認できました。
加えてがん間質内のインテグリンα11の発現は、CAFの特異的マーカーとして報告されているコラーゲンタイプXIαI*7の発現と相関がみられ、CAGE法解析やたんぱく質の発現レベルにおいても、CAFでコラーゲンタイプXIαIの転写活性や発現が高いことも明らかになりました。
一方、サイトカインのTGF-β1*8はCAFの遊走能を刺激するだけではなく、インテグリンα11とコラーゲンタイプXIαIの発現を増加させ、肺がん細胞がCAFに向かって遊走することもわかりました。
以上の結果から、CAFとがん細胞が互いに連携することでがん間質にがん細胞を取り込み、積極的にがんの進展を促進させるという、非小細胞肺がんにおけるCAFの活性化機序が明らかになりました(図2)。つまり、インテグリンα11 +/コラーゲンタイプXIαI + CAFを標的とした新たな治療法が、がんの進展をより効果的に抑制する可能性が示されました。

図2:本研究で明らかになったがん関連線維芽細胞(CAF)の活性化機序
CAFで高発現しているインテグリンα11が、フィブロネクチン受容体であるインテグリンα5β1とは独立して、ERK1/2シグナルを介しI型コラーゲンやフィブロネクチンに向かうCAFの遊走能を高めていた。また、がん間質内のインテグリンα11の発現は、CAFの特異的マーカーのコラーゲンタイプXIαIの発現と相関していた。さらにがん細胞との共存下においてインテグリンα11およびコラーゲンタイプXIαIの発現がより増強したことから、インテグリンα11 +/コラーゲンタイプXIαI + CAFががんの進展に大きく関与している可能性がある。これらの結果からインテグリンα11 +/コラーゲンタイプXIαI + CAFを標的とした新たな治療法が、がんの進展をより効果的に抑制する上で有効である可能性が示唆された。
今後の展開
CAFは多様性を持っており、これまでに様々な特異的なマーカーが報告されています。本研究ではその中でもインテグリンα11 +/コラーゲンタイプXIαI + CAFの活性化が肺がんの進展に特に重要な役割を担っている可能性を明らかにしました。今回の発見は、がん間質に存在するCAFを標的とした従来の治療法とは異なる、新たな肺がん治療法への足掛かりとなる可能性があります。今後さらに研究を重ねることで、CAFの機能解明に関する研究は 肺がん死亡者数の減少を導くブレークスルーとなりうることが期待されます。
用語解説
*1 非小細胞肺がん:肺がんの組織型のひとつ。腺がん・扁平上皮がん・大細胞がんに分類される。
*2 がん関連線維芽細胞(CAF):がん細胞の周囲に存在する線維芽細胞のこと。がん細胞の増殖・浸潤や生存維持などに関与しているといわれている。
*3 CAGE法:各遺伝子を転写開始点ごとに定量する方法。他の方法に比べ幅広く高感度に遺伝子を定量できる。
*4 インテグリンα11:インテグリンα鎖の一種。細胞表面に存在するタンパク質でありβ鎖と結合し細胞接着などを担う。
*5 がん間質:腫瘍組織のうちがん細胞以外の部分のこと。
*6 遊走能:細胞などが生体内のある位置から別の位置に移動すること。
*7 コラーゲンタイプXIαI:CAFに存在するコラーゲンの一種であり、予後との関連が指摘されている。
*8 TGF-β1:形質転換増殖因子。線維化促進因子の一つであり、線維芽細胞の遊走や筋線維芽細胞への分化を促進し、ファイブロネクチンをはじめとする細胞外マトリックスの産生をもたらす。
原著論文
本研究はMolecular Oncology誌のオンライン版で(2021年3月7日付)先行公開されました。
タイトル: Cancer-associated fibroblast migration in non-small cell lung cancers is modulated by increased integrin α11
タイトル(日本語訳):非小細胞肺がんにおけるintegrin α11によるがん関連線維芽細胞の制御
著者:Moe Iwai 1, Miniwan Tulafu 2, Shinsaku Togo 1, Hideya Kawaji 3 4 5, Kotaro Kadoya 1, Yukiko Namba 1, Jin Jin 1 6, Junko Watanabe 1, Takahiro Okabe 2, Moulid Hidayat 1 7, Issei Sumiyoshi 1, Masayoshi Itoh 5, Yu Koyama 8 9, Yasuhiko Ito 8, Akira Orimo 8, Kazuya Takamochi 10, Shiaki Oh 10, Kenji Suzuki 10, Yoshihide Hayashizaki 5, Koji Yoshida 11, Kazuhisa Takahashi 1
著者(日本語表記):岩井萌1)、Miniwan Tulafu2)、十合晋作1)、川路英哉3,4,5)、門屋講太郎1)、難波由喜子1)、Jin Jin1,6)、渡邊純子1)、岡部隆宏2)、Moulid Hidayat1,7)、住吉一誠1)、伊藤昌可5)、小山侑8,9)、伊藤恭彦8)、折茂彰8)、高持一矢10)、王志明10)、鈴木健司10)、林崎良英5)、吉田浩二11)、高橋和久1)
著者所属:1)順天堂大学呼吸器内科学講座、2)順天堂大学先導的がん医療開発研究センター、3)公益財団法人 東京都医学総合研究所、4)理化学研究所予防医療・ゲノミクス応用開発ユニット、5)理化学研究所予防医療・診断技術開発プログラム、6) Department of Respiratory and Critical Care Medicine, Beijing Hospital, National Center of 、7) Department of Pulmonology and Respiratory Medicine, Universitas Indonesia Faculty of Medicine、8)順天堂大学病理・腫瘍学講座、9)東京歯科大学口腔病態外科学講座、10)順天堂大学呼吸器外科学講座、11)近畿大学生物理工学講座
DOI: 10.1002/1878-0261.12937.
本研究はJSPS科研費JP15K19430, JP 19K17683, JP 23591161および理化学研究所との共同研究の基に実施されました。本研究にご協力いただいた皆様には深謝いたします。