2024-12-10 国立がん研究センター
発表のポイント
- 国内154施設が参加する研究プロジェクトLC-SCRUM-Asiaにおいて、小細胞肺がんの患者さん1035名の遺伝子解析を行い、がんの遺伝子情報を調べました。
- その結果、小細胞肺がんが遺伝子の変化によって五つのサブグループに分類可能であることが明らかになりました。
- この遺伝子の変化に基づいた分類が、小細胞肺がんの治療方法の選択と治療効果の予測に有用な指標となる可能性が示されました。
- この研究成果によって、より多くの小細胞肺がん患者さんの治療成績の改善が期待されます。
概要
国立研究開発法人国立がん研究センター(理事長:中釜 斉、東京都中央区)東病院(病院長:土井 俊彦、千葉県柏市、以下東病院)は、肺がん遺伝子スクリーニング基盤「LC-SCRUM-Asia」(研究代表者:東病院 呼吸器内科長 後藤 功一)の臨床ゲノムデータベースを用いて、肺がんの中でも特に予後の悪い小細胞肺がんの1035例を対象とした研究を行いました。1035例中944例において遺伝子解析に成功し、遺伝子の変化によって以下の五つのサブグループ(グループ A~E)に分類することができました。
【表1】小細胞肺がんのサブグループの概要
| グループA(NSCLC-subgroup) | 非小細胞肺がんに関連した遺伝子変化を有するサブグループ(8.5%) |
| グループB(MYC-subgroup) | MYCファミリー遺伝子増幅を有するサブグループ(13%) |
| グループC(Hotspot-subgroup) | 様々ながんで比較的高頻度に認められ、治療標的となりうる遺伝子変異を有するサブグループ(3.0%) |
| グループD(PI3K-subgroup) | PI3K/AKT/mTOR経路の遺伝子変異を有するサブグループ(7.4%) |
| グループE(HME-subgroup) | ヒストン修飾酵素に遺伝子変異を有するサブグループ(17.6%) |
グループA (患者さんの8.5%) とグループB (患者さんの13%) の二つのサブグループは、従来のプラチナ製剤を併用した化学療法に対して効果が乏しいことが明らかになりました。また、グループC (患者さんの3%) とグループD (患者さんの7.4%)の二つのサブグループにおいては、新しい治療薬の標的となりうる遺伝子変異が検出されました。一方、グループE (患者さんの17.6%) では、免疫チェックポイント阻害薬が高い効果を有する可能性が示されました。
小細胞肺がんにおいては、これまで本研究のような大規模なデータベースを用いた研究がほとんど行われてきませんでした。そのため、他の肺がんと比べて個別化医療の確立が立ち遅れており、治療成績も長い期間停滞しています。本研究の成果は、小細胞肺がんの個別化医療を促進し、より多くの患者さんの治療成績の改善に貢献すると期待されます。
この研究成果は国際学術誌「Journal of Thoracic Oncology」に、米国時間2024年10月10日付で掲載されました。
背景
肺がんは現在、日本人のがん死因の第1位です。日本人の肺がんのうち約90%を占める非小細胞肺がんは、近年多くの分子標的治療薬が開発され、治療成績の著しい改善が認められています。一方、肺がんのうち10-15%を占める小細胞肺がん注1は、5年生存率約10%注2と予後の悪いがんです。
小細胞肺がんは、非小細胞肺がんとは対照的に、新しい治療手段の開発が乏しく、治療成績の改善が大きな課題です。その理由として、小細胞肺がんがこれまで単一の疾患として診断・治療されてきたため、患者さんの遺伝子やタンパク質などの分子レベルでの特徴を捉える個別化医療を目指した研究が立ち遅れていたことが挙げられます。
今回本研究グループは、1000例を超える小細胞肺がん患者さんが登録されているLC-SCRUM-Asiaの臨床ゲノムデータベースを用いて、小細胞肺がんの遺伝子変化と患者さんの臨床経過および治療の効果を調べました。小細胞肺がんを、遺伝子の変化に基づいてサブグループに分類することにより、治療効果の予測や最適化、新たな治療法の開発に役立てることができないかと考え、研究を進めました。
注1:肺癌診療ガイドライン2024年版
注2:2020 国立がん研究センター院内がん登録生存率
https://hbcr-survival.ganjoho.jp/graph?year=2014-2015&elapsed=5&type=c07#h-title
本研究方法・成果
本研究では、2015年7月から2020年3月の間にLC-SCRUM-Asiaに登録された小細胞肺がん患者さん1035例を対象に、がん組織の遺伝子変化を、次世代シーケンサーを用いたがん遺伝子パネル検査で解析しました。この方法では、個々のがん患者さんのサンプルについて、一度に143~161個の遺伝子について調べることが可能です。その結果、遺伝子変化の種類に応じて五つのサブグループに分類することに成功しました。さらに、これら五つのグループの特徴や治療の効果を検討しました。
小細胞肺がんのサブグループ分類
1035例中944例において遺伝子解析が成功し、遺伝子変化の種類によって、五つのサブグループ(グループ A~E)に分類することができました。サブグループの詳細に関しては、【表1】を参照ください。

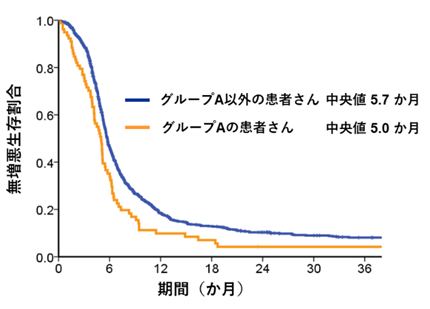 グループA(NSCLC-subgroup)に属する患者さんに対するプラチナ製剤を併用した化学療法の効果
グループA(NSCLC-subgroup)に属する患者さんに対するプラチナ製剤を併用した化学療法の効果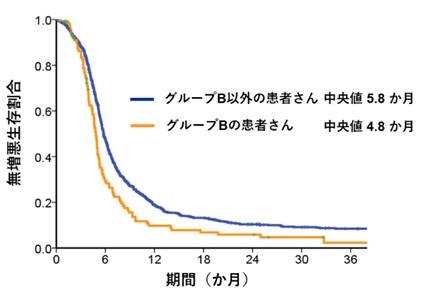 グループB(MYC-subgroup)に属する患者さんに対するプラチナ製剤を併用した化学療法の効果
グループB(MYC-subgroup)に属する患者さんに対するプラチナ製剤を併用した化学療法の効果
グループA(NSCLC-subgroup)またはグループB(MYC-subgroup)に属する小細胞肺がんは、それ以外の小細胞肺がんと比較して、従来のプラチナ製剤を併用した化学療法における無増悪生存期間(PFS)が短く、治療の効果が乏しいことが分かりました。
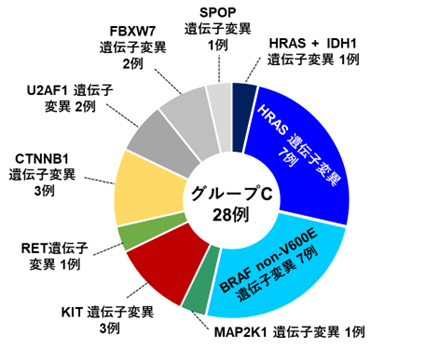 グループC(Hotspot-subgroup)の変異の内訳
グループC(Hotspot-subgroup)の変異の内訳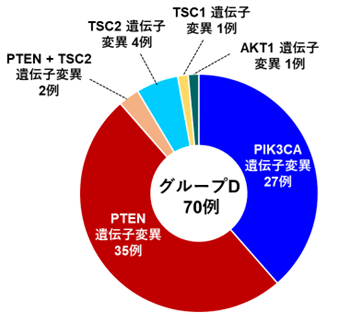 グループD(PI3K-subgroup)の変異の内訳
グループD(PI3K-subgroup)の変異の内訳
また、3%の患者さんには、様々ながんで一般的に高頻度に認められ、かつ治療標的となりうる遺伝子変異を認めました(グループC)。そして7.4%の患者さんには、PI3K/AKT/mTOR経路の遺伝子変異が認められました(グループD)。これら2つのサブグループでは、遺伝子の変異に基づいて新たな治療薬が開発できる可能性があります。
ヒストン修飾酵素の遺伝子変異の頻度
ヒストン修飾酵素の遺伝子変異は、小細胞肺がんで比較的高頻度に認められることがこれまでにも報告されています。今回、ヒストン修飾酵素の遺伝子変異に関しては、632名で評価が可能でした。ヒストン修飾酵素に遺伝子変異を有する小細胞肺がんは、17.6%であり、これらをグループE(HME-subgroup)と定義しました。
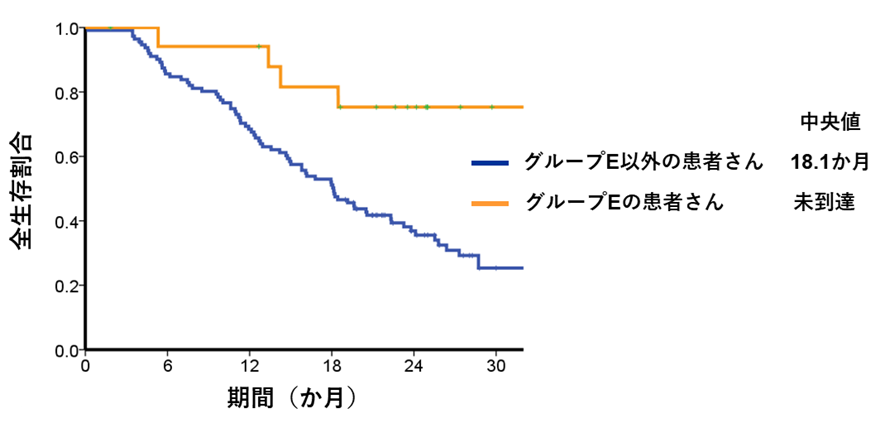
免疫チェックポイント阻害剤PD-1/PD-L1阻害薬を使用した患者さん130名の全生存期間
代表的な免疫チェックポイント阻害薬として広く用いられているPD-1/PD-L1阻害薬を使用した患者さん130名の中で、グループEに属する患者さんは、そうでない患者さんと比較して、生存期間が有意に長いことが明らかになりました。このことは、グループEの患者さんにおいて、免疫チェックポイント阻害剤が有用となる可能性を示しています。
以上の結果から、小細胞肺がんの遺伝子の変化に基づいた分類が、治療結果の予測と治療選択において、効果的な指針となる可能性があることが示されました。
展望
本研究は、小細胞肺がんの遺伝子変化と治療に対する反応性の違いを、大規模な臨床ゲノムデータベースを用いて解明した初めての研究です。小細胞肺がんを五つのサブグループに分類し、既存のプラチナ製剤を併用した化学療法や免疫チェックポイント阻害剤がどのグループで有効であるかを明らかにしたことは、今後の治療開発を行っていく上で重要な知見であると考えられます。この研究成果を通じて、小細胞肺がんの個別化医療を推進し、より多くの患者さんの治療成績の改善に貢献していきたいと考えております。一方、今回の研究では小細胞肺がんの約半数が、五つのサブグループのいずれにも分類されませんでした。これは小細胞肺がんに対する遺伝子の変化に基づいた分類の限界を示しています。これら「分類不能」群に関しては、遺伝子の変化以外にも、タンパク質やRNAといった様々な分子の情報を包括的に解析する技術(マルチオミックス)を用いた、より精緻な分類が期待されます。
発表論文
雑誌名
Journal of Thoracic Oncology
タイトル
Clinical significance of a prospective large genomic screening for small-cell lung cancer: the genetic classification and a biomarker driven phase II trial of gedatolisib
著者
Shigeki Umemura, Hibiki Udagawa, Takaya Ikeda, Haruyasu Murakami, Haruko Daga, Ryo Toyozawa, Toshiyuki Kozuki, Jun Sakakibara-Konishi, Yuichiro Ohe, Masahiro Morise, Terufumi Kato, Masato Shingyoji, Satoshi Hara, Naoki Furuya, Shuhei Teranishi, Saori Takata, Shingo Miyamoto, Ichiro Nakachi, Masashi Wakabayashi, Shogo Nomura, Akihiro Sato, Genichiro Ishii, Katsuya Tsuchihara, Eri Sugiyama, Keisuke Kirita, Tetsuya Sakai, Yuji Shibata, Hiroki Izumi, Kaname Nosaki, Yoshitaka Zenke, Shingo Matsumoto, Kiyotaka Yoh, Seiji Niho, Koichi Goto
DOI
10.1016/j.jtho.2024.10.004.
掲載日
2024年10月10日
URL
http://www.jto.org/article/S1556-0864(24)02378-5/abstract
研究費
研究費名
国立研究開発法人日本医療研究開発機構(AMED)
研究事業名
革新的がん医療実用化研究事業
研究課題名
希少遺伝子変異を有する小細胞肺癌に対する新規治療法の確立に関する研究
(JP21ck0106289; JP16ck0106111)
研究代表者名
後藤 功一
お問い合わせ先
研究に関するお問い合わせ
国立研究開発法人国立がん研究センター東病院
呼吸器内科 梅村茂樹
広報窓口
国立研究開発法人国立がん研究センター
企画戦略局 広報企画室(柏キャンパス)