2025-06-10 京都大学
<関連情報>
- https://www.kyoto-u.ac.jp/ja/research-news/2025-06-10-0
- https://www.kyoto-u.ac.jp/sites/default/files/2025-06/web_2506_Jo-fac62e9aa5e3e1f4c01e788e99ccec0c.pdf
- https://www.isct-cytotherapy.org/article/S1465-3249(25)00739-X/fulltext
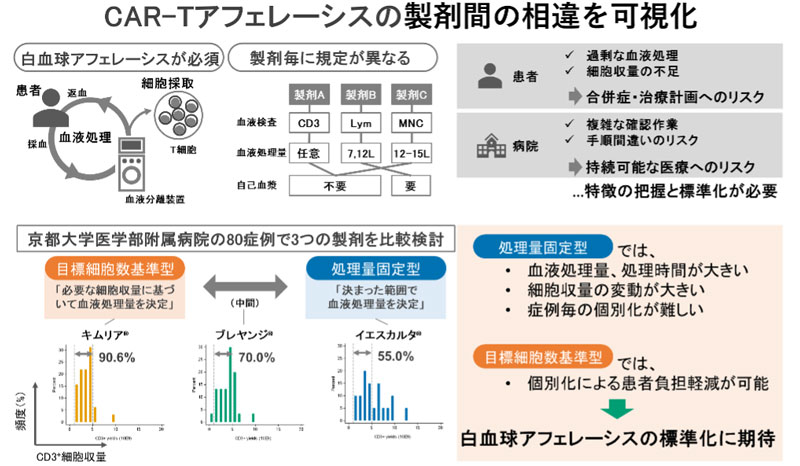
リンパ腫患者に対するCD19 CAR-T細胞療法のアフェレーシスを最適化する歩留まり重視のアプローチ Yield-driven approach optimizes apheresis of CD19 CAR-T cell therapy for patients with lymphoma
Tomoyasu Jo ∙ Toshio Kitawaki ∙ Takashi Sakamoto ∙ … ∙ Miki Nagao ∙ Akifumi Takaori-Kondo ∙ Yasuyuki Arai
Cytotherapy Published:June 6, 2025
DOI:https://doi.org/10.1016/j.jcyt.2025.06.002
Highlights
•Specifications for leukapheresis vary among CAR-T products, affecting outcomes such as blood volume processed and cell yields.
•A yield-driven approach may reduce variability in cell yields to optimize leukapheresis.
ABSTRACT
Leukapheresis for chimeric antigen receptor (CAR) T-cell therapy requires optimization according to product-specific manufacturing requirements. We retrospectively analyzed 80 patients with large B-cell lymphoma, who underwent leukapheresis for tisagenlecleucel (tisa-cel, n=31), lisocabtagene maraleucel (liso-cel, n=29), or axicabtagene ciloleucel (axi-cel, n=20) at Kyoto University Hospital between January 2022 and October 2024. Peripheral blood CD3+ cell counts before leukapheresis (median, 504/μL) and collection efficiencies (median, 62.1%) were similar among groups. The axi-cel group required significantly larger processing blood volumes (axi-cel, 12 L; liso-cel, 12 L; tisa-cel, 10 L; p<0.001) and longer processing times (axi-cel, 240 min; liso-cel, 204 min; tisa-cel, 203 min; p=0.002), resulting in higher CD3+ cell yields. Moreover, the standard deviation of CD3+ cell yields was significantly larger in the axi-cel group (axi-cel, 3.04 × 109 cells; liso-cel, 1.54 × 109 cells; tisa-cel, 1.59 × 109 cells; p=0.003). The axi-cel group more frequently exceeded estimated blood volumes needed to achieve 5 × 109 CD3+ cells (axi-cel, 45.0%; liso-cel, 17.2%; tisa-cel, 16.1%; p=0.048). These findings highlight variability in leukapheresis procedures among CAR-T products. Protocols targeting cell yields based on peripheral blood cell counts may optimize blood volume to be processed so as to reduce patient burden.