2026-05-12 アメリカ国立衛生研究所(NIH)
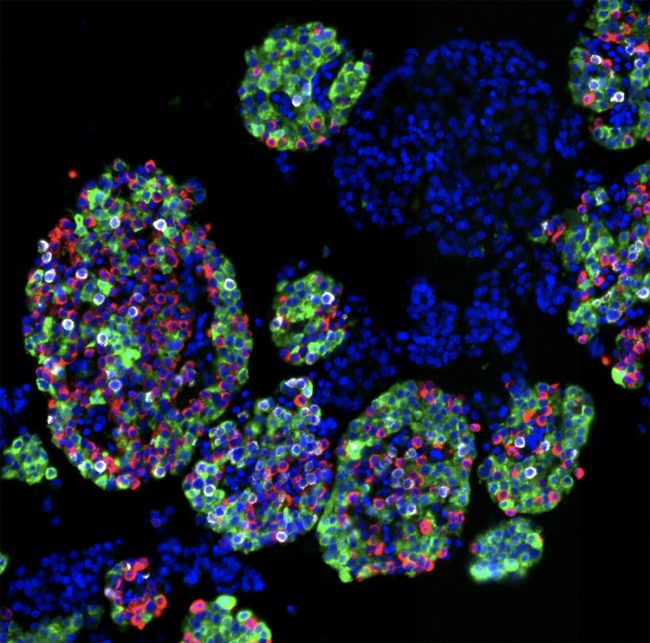
Isolated islets showing cell nuclei (blue) and three main endocrine cell types: insulin-producing beta cells (green), glucagon-producing alpha cells (red), and somatostatin-producing delta cells (white). IIDP Islet Collection in Pancreatlas, Vanderbilt University Medical Center.
<関連情報>
- https://www.nih.gov/news-events/news-releases/nih-funded-study-maps-human-pancreatic-islet-cells-offering-new-clues-diabetes-risk
- https://www.nature.com/articles/s41467-026-70689-5
内分泌細胞の組成の不均一性がヒト膵島機能表現型を規定する Heterogeneous endocrine cell composition defines human islet functional phenotypes
Carmella Evans-Molina,Yasminye D. Pettway,Diane C. Saunders,Seth A. Sharp,Thomas SR. Bate,Han Sun,Heather Durai,Shaojun Mei,Anastasia Coldren,Corey Davis,Conrad V. Reihsmann,Alexander L. Hopkirk,Jay Taylor,Amber Bradley,Radhika Aramandla,Greg Poffenberger,Adel Eskaros,Regina Jenkins,Danni Shi,Ke Xu,Hakmook Kang,Varsha Rajesh,Swaraj Thaman,Fan Feng,The IIDP Consortium,… Marcela Brissova
Nature Communications Published:12 May 2026
DOI:https://doi.org/10.1038/s41467-026-70689-5
Abstract
Phenotyping and genotyping initiatives within the Integrated Islet Distribution Program (IIDP), the largest source of human islets for research in the U.S., provide standardized assessment of islet preparations distributed to researchers and enable the integration of multiple data types. Data from islets of the first 299 organ donors without diabetes analyzed using this pipeline highlights substantial heterogeneity in islet cell composition associated with hormone secretory traits, sex, reported race and ethnicity, genetically predicted ancestry, and genetic risk for type 2 diabetes (T2D). While α and β cell composition influenced insulin and glucagon secretory traits, the abundance of δ cells showed the strongest association with insulin secretion and was also associated with the genetic risk score (GRS) for T2D. These findings have important implications for understanding mechanisms underlying diabetes heterogeneity and islet dysfunction and may provide insight into strategies for personalized medicine and β cell replacement therapy.

