2021-05-25 筑波大学,株式会社IDファーマ,慶應義塾大学,日本医療研究開発機構
心臓を構成する心筋細胞は、再生能力が乏しく、心機能が著しく低下した場合の根本的な治療法は、心臓移植しかありません。しかし、ドナー不足などの問題があり、十分な治療の提供は困難です。心臓移植に代わる方法として、ES細胞やiPS細胞などの多能性幹細胞を用いた再生医療が注目されていますが、これにも、腫瘍形成の可能性、組織生着率の低さ、工程の複雑さや高コストといった課題があります。
本研究グループは、これまでに、これらの課題を解決し得る別の方法として、幹細胞を用いずに心臓線維芽細胞から直接心筋細胞を誘導する「心筋直接リプログラミング法」を開発しています。しかしながら、生体内の心臓線維芽細胞に心筋リプログラミング遺伝子を導入して作製する心筋細胞が、真に心臓線維芽細胞由来の誘導された再生心筋細胞か、あるいは心臓線維芽細胞と周囲の心筋細胞が融合してできた見かけ上再生して見える心筋細胞かは不明でした。そこで本研究では、細胞の系譜と融合を明らかにする遺伝子改変マウスを用いて、生体内で新たに作製された心筋細胞が、心臓線維芽細胞由来の真の再生心筋細胞であることを、世界で初めて明らかにしました。
本研究により、マウス生体内に心筋リプログラミング遺伝子を導入することで、心臓線維芽細胞から直接心筋細胞を誘導できることが分かりました。本研究結果は心疾患に対する新しい心臓再生医療の実現を大きく前進させることが期待されます。
研究代表者
筑波大学医学医療系
家田 真樹 教授
株式会社IDファーマ
朱 亜峰 取締役副社長
慶應義塾大学医学部循環器内科
福田 恵一 教授
自治医科大学遺伝子治療研究部
水上 浩明 教授
研究の背景
心臓を構成する心筋細胞は、再生能力が乏しいため、心疾患により心筋細胞が壊死し、線維芽細胞の増殖により線維化が進行すると、心臓のポンプ機能が低下して心不全に至ります。現在、心機能が著しく低下した患者に対する根本的な治療は心臓移植しかありませんが、ドナー不足の問題等により十分な治療が供給できているとは言えません。そこでES細胞やiPS細胞など多能性幹細胞を用いた再生医療の開発に注目が集まっています。ES細胞やiPS細胞などの多能性幹細胞は、様々な細胞に分化できる多分化能と高い増殖能から心筋再生への応用も期待されていますが、腫瘍形成の可能性、組織生着率の低さ、作業工程が複雑で高コストであること等、克服すべき課題も残っています。これらの課題を解決し得る別の方法として、本研究グループは、幹細胞を用いずに心臓線維芽細胞から直接心筋細胞を誘導する「心筋直接リプログラミング法」を開発しています。
しかしながら、近年、心臓組織幹細胞から作製されると考えられていた心筋細胞が、実は心臓組織幹細胞と周囲の心筋細胞との融合によりできた、見かけ上再生してみえる心筋細胞であることが判明し、心臓組織幹細胞による心筋再生に大きな疑問が生じている状況があります注1)。心臓再生医療を進める上で、心筋再生の由来を明らかにすることは非常に重要です。そこで本研究では、2色の蛍光で細胞を標識できる遺伝子改変マウスを用いて、心筋直接リプログラミング法において、マウス生体内で作製される心筋細胞が、真に心臓線維芽細胞由来の直接誘導により作製されたものか、あるいは心臓線維芽細胞が周囲の心筋細胞と融合してできたものか、検証を行いました。
研究内容と成果
本研究ではまず、ホルモン剤の一つであるタモキシフェン投与前は全ての細胞が赤で標識され、投与後には心臓線維芽細胞のみが赤色を消失して緑色に変化する遺伝子改変マウスを作製しました注2)。これを用いると、マウスの心臓線維芽細胞に心筋リプログラミング遺伝子注3)の導入により心臓線維芽細胞(緑)から心筋細胞が直接誘導される場合は緑色の心筋細胞が作製され(真の心筋再生)、一方、心臓線維芽細胞(緑)が周囲に存在する心筋細胞(赤)と融合した場合は黄色の心筋細胞(緑+赤=黄色、見かけ上の再生)として観察されます(図1)。
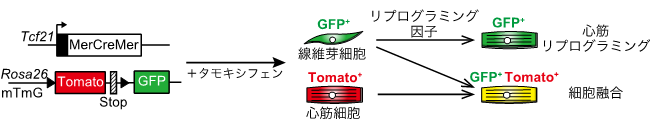
図1 本研究に用いた遺伝子改変マウスタモキシフェンを投与すると、心臓線維芽細胞が緑色(GFP陽性)、それ以外の細胞が赤色(Tomato陽性)に光る。心臓線維芽細胞から直接誘導された心筋細胞は緑色(真の再生心筋)であるのに対し、細胞融合により作製された心筋細胞は黄色(見かけ上の再生心筋)を示す。
このようにして心筋梗塞4週間後のマウスの心臓を観察すると、心筋リプログラミング遺伝子を導入しないコントロール群では、細胞融合を示す黄色の心筋細胞が約0.3%観察され(図2左)、緑色の再生心筋細胞は全く見られませんでした。一方、センダイウイルスベクター注4)を用いて心筋リプログラミング遺伝子を導入したマウスでは、心臓線維芽細胞から直接誘導された緑色の心筋細胞が約1.5%認められました(図2右)。また、細胞融合の頻度に関して、心筋リプログラミング遺伝子導入による変化は見られませんでした。これらの結果から、心筋直接リプログラミング法により新しく作製された心筋細胞の大部分が、心臓線維芽細胞からの直接誘導による真の再生心筋細胞であることが証明されました。
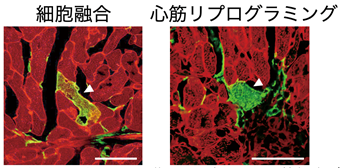
図2 心筋梗塞4週間後のマウスの心臓の観察(左図)細胞融合による心筋細胞(黄色部分)と、(右図)心筋リプログラミングにより誘導された真の再生心筋細胞(緑色部分)
今後の展開
本研究により、生体内で心筋直接リプログラミングによる真の心筋再生が可能であることが証明されました。今後、生体内心筋リプログラミング効率の改善やリプログラミング遺伝子の導入方法などの検討は必要ですが、本研究成果は新しい心臓再生医療の実現を大きく前進させるものと期待されます(図3)。本研究チームは、幹細胞を介さずに心筋細胞を再生する新しい再生医療技術の臨床応用を目指して、さらに研究を進めていきます。
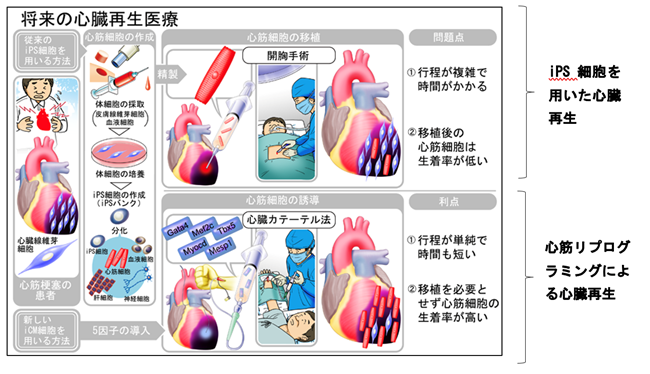
図3 将来の心臓再生医療の展望(上段)iPS細胞を用いる心筋細胞移植による心臓再生、(下段)本研究グループが開発している細胞移植を必要としない心筋リプログラミングによる心臓再生
用語解説
- 注1)心臓組織幹細胞と心筋細胞の融合による見かけ上の心筋再生
- 心臓組織幹細胞は、心臓内に存在する、心筋細胞に分化可能な細胞としてAnversaらにより2003年に報告された。これに対して、この細胞は周囲の心筋細胞と融合することで、見かけ上、心筋に分化して見えるが、真の心筋再生には寄与しないとする反駁論文が、2014年にvan Berloらによりに報告された。その後も、心臓組織幹細胞による心筋再生に関して否定的な研究結果が複数報告され、現在では、心臓組織幹細胞の存在自体が否定的となっている。
- 注2)本研究に用いた遺伝子改変マウス
- タンパク質Creと変異エストロゲン受容体が融合したMerCreMerタンパク質は、通常細胞質に存在するが、エストロゲン誘導体であるタモキシフェンと結合することにより核内に移行し、loxP配列(特定のDNA配列)に対して組換えを起こす。これを利用して、タモキシフェン投与により、Cre-loxPシステムの働く細胞や時期を調節することが可能である。今回用いた遺伝子改変マウスでは、Tcf21遺伝子を発現する心臓線維芽細胞のみがMerCreMerタンパク質を発現し、タモキシフェン投与によりloxP配列で挟まれたTomato(赤色蛍光タンパク質)が取り除かれてGFP(緑色蛍光タンパク質)を発現する。一方、心臓線維芽細胞以外の細胞はMerCreMerタンパク質を発現しないため、Cre-loxPシステムが働かず、Tomato陽性(赤色)のままである。これにより心筋リプログラミングによる真の心筋再生と、心臓線維芽細胞と心筋細胞の融合による見かけ上の再生心筋を区別できる(図1)。
- 注3)心筋リプログラミング遺伝子
- 本研究グループが発見した、マウス線維芽細胞から心筋細胞を直接作製するために必要な3遺伝子(Gata4, Mef2c, Tbx5)。
- 注4)センダイウイルスベクター
- RNAウイルスベクターの一つで、宿主の細胞に感染した後、宿主のゲノム(DNA)に入り込むことなく細胞質内で遺伝子を効率的に発現し、ゲノムを損傷することがないという特徴を持つ。
研究資金
本研究は、国立研究開発法人日本医療研究開発機構(AMED)の難治性疾患実用化研究事業「拡張型心筋症に対する革新的な心筋再生遺伝子治療薬の開発」(20ek0109305h0003)、および、再生医療実現拠点ネットワークプログラム「幹細胞・再生医学イノベーション創出プログラム」(20bm0704030h0002)、公益財団法人武田科学振興財団、科研費(19K22613,19K17550)の支援によって行われました。
掲載論文
- 題名
- Overexpression of Gata4, Mef2c, and Tbx5 Generates Induced Cardiomyocytes via Direct Reprogramming and Rare Fusion in the Heart
(Gata4,Mef2c,Tbx5過剰発現は心筋直接リプログラミングと低頻度の細胞融合により心筋再生する) - 著者名
- Mari Isomi,Taketaro Sadahiro,Hiroyuki Yamakawa,Ryo Fujita,Yu Yamada,Yuto Abe,Yoshiko Murakata,Tatsuya Akiyama,Tsugumine Shu,Hiroaki Mizukami,Keiichi Fukuda,Masaki Ieda
- 掲載誌
- Circulation
- 掲載日
- 2021年5月25日
- DOI
- 10.1161/CIRCULATIONAHA.120.052799
お問合わせ先
研究内容に関すること
家田 真樹(いえだ まさき)
筑波大学 医学医療系(循環器内科)教授
取材・報道に関すること
筑波大学広報室
株式会社IDファーマ
慶應義塾大学 信濃町キャンパス総務課
AMED事業に関すること
日本医療研究開発機構
再生・細胞医療・遺伝子治療事業部 遺伝子治療研究開発課
難治性疾患実用化研究事業 担当