2021-08-31 京都大学iPS細胞研究所
ポイント
- ダウン症(トリソミー21)の患者さんのiPS細胞由来神経細胞は、健常対照細胞よりも多くのアミロイドβを分泌する。
- 抗酸化剤であるN-アセチルシステインが、このアミロイドβの分泌を抑制することを明らかにした。
1. 要旨
利川寛実大学院生(CiRA臨床応用研究部門、現:済生会吹田病院)、齋藤潤准教授(CiRA同部門)らの研究グループは、ダウン症患者さん由来のiPS細胞から作製した神経細胞を用い、ダウン症の神経細胞ではアミロイドβが過剰産生されることと、これが抗酸化剤であるN-アセチルシステインの添加によって抑制されることを示しました。本研究の成果は、ダウンの神経症状に対する治療の選択や、今後の治療法の研究に役立つと期待されます。
本研究は、大阪医科歯科大学、済生会吹田病院、京都大学医学部人間健康学科、鳥取大学、米ワシントン大学との共同研究の成果です。
この研究成果は2021年8月30日に「Scientific Reports」誌に公開されました。
2. 研究の背景
ダウン症は21番染色体を3本持つ(トリソミー21)先天性の染色体異常症です。特徴的な顔貌をもち、先天性心疾患や骨格の異常、免疫の異常など様々な症状を認めますが、最も特徴的な症状は発達および知的障害です。また、約60%の方が若年性アルツハイマー病を発症することが知られています。
ダウン症における若年性アルツハイマー病の発症原因の1つとして、アルツハイマー病の原因物質の一つと考えられているアミロイドβという物質を産生する、APP遺伝子が過剰にあることが考えられています。APP遺伝子は21番染色体上にあり、通常2本存在しますが、ダウン症候群では3本存在します。APPタンパクは脳内で切断され、アミロイドβとなります。ダウン症患者さんの脳内には多くのアミロイドβがあり、病理学的にアルツハイマー型認知症の患者さんと同様の形態を示します。また、高い酸化ストレスが神経障害を引き起こしていることも原因の1つであると考えられています。アミロイドβと酸化ストレスは複雑に関係しているため、抗酸化剤は治療のターゲットになりうると考えられています。
そこで本研究では、ダウン症の患者さんの神経細胞に抗酸化剤であるN-アセチルシステインを投与し、アミロイドβ分泌に及ぼす効果を検証しました。
3. 研究結果
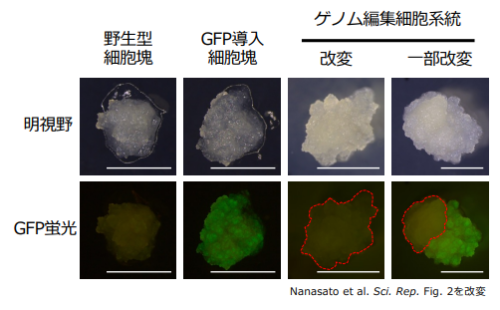
まず、NGN2 遺伝子を過発現する手法を用い、ダウン症の患者さんのiPS細胞から神経細胞を作成しました(D-iNs)。また、事前に上記と同じダウン症iPS細胞から21番染色体を1本削除した細胞を作成しており、その細胞からも同様に神経細胞を作成しました(E-iNs)。
次に、この二つの神経細胞のアミロイドβの分泌量を測定しました。分泌されるアミロイドβには様々な種類がありますが、その多くがアミロイドβ40(Aβ40)、アミロイドβ42(Aβ42)です。今回はその2種類のアミロイドβを測定しました。D-Ns からは、E-iNsよりも多くのAβ40、Aβ42が分泌されていました(図1)。
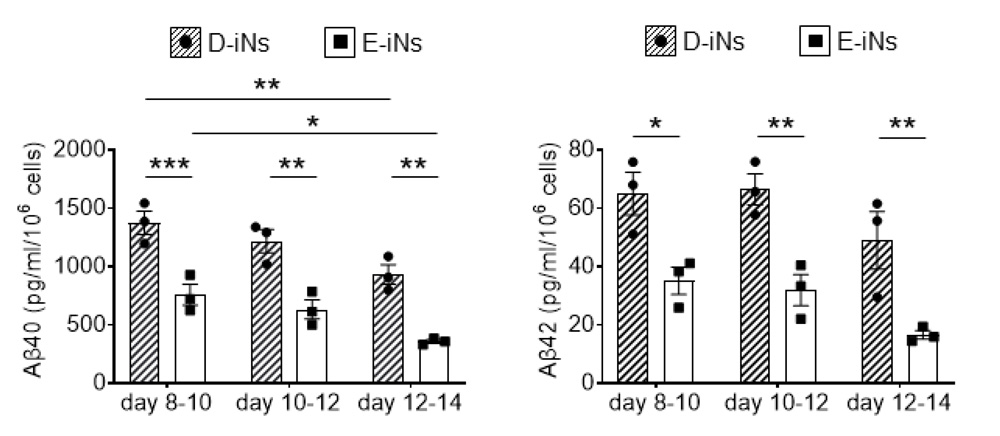
図1:D-iNsとE-iNsのアミロイドβの分泌量
神経分化開始後、8日目~10日目、10日目~12日目、12日目~14日目の3つの期間で比較しました。いずれの期間でも、ダウン症由来神経細胞(D-iNs)の方が多くのアミロイドβを分泌しています。
これらの神経細胞に、抗酸化剤であるN-アセチルシステインを投与したところ、分泌されるアミロイドβは優位に減少しました。また反対に、酸化剤である過酸化水素(H2O2)を投与すると、アミロイドβの分泌が亢進しました(図2)。
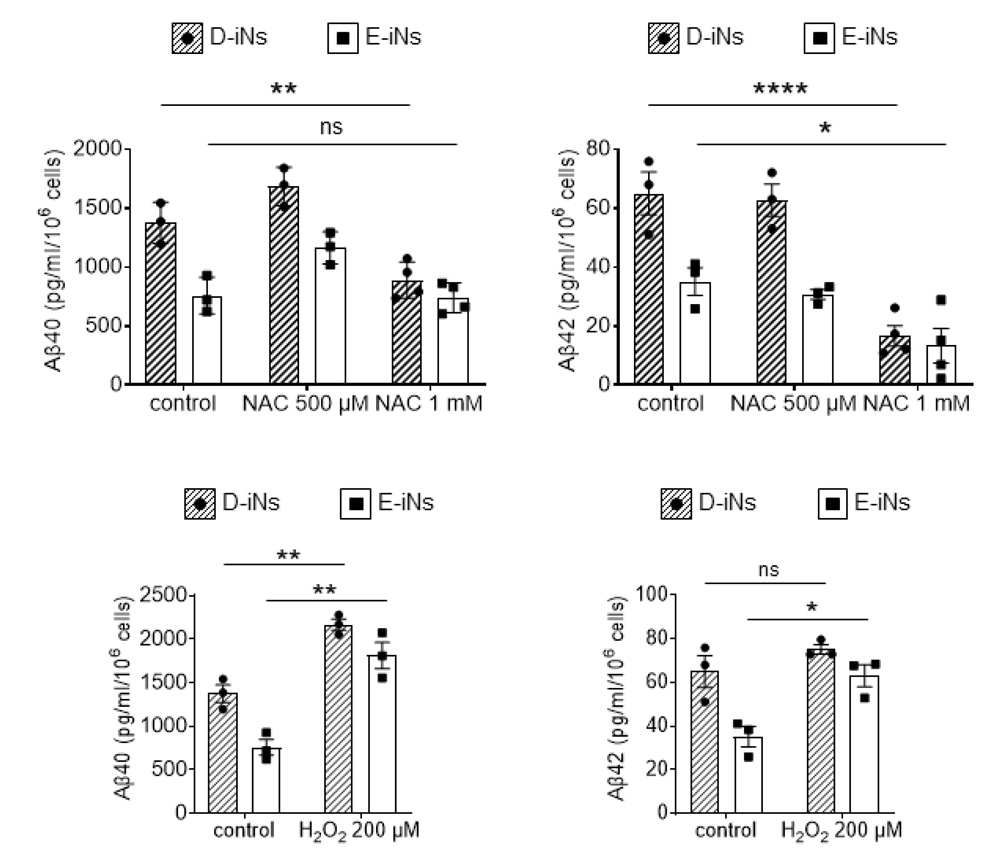
図2:N-アセチルシステイン(NAC)で処理したときのアミロイドβの分泌量と、
過酸化水素(H2O2)で処理したときのアミロイドβの分泌量
8日目~10日目で比較しました。N-アセチルシステインで処理した細胞ではアミロイドβの分泌が抑制されていますが、過酸化水素で処理した細胞ではアミロイドβは増加しています。
4. まとめ
本研究では、ダウン症患者さんの多能性幹細胞と、同質遺伝子を持つ健常コントロールを用い、N-アセチルシステインがアミロイドβ分泌を有意に抑制することを確認しました。N-アセチルシステインはアルツハイマー病のモデルマウスの認知機能を改善する効果や、酸化ストレスによる神経細胞死を改善する効果などが報告されており、様々な神経心理疾患、神経変性疾患での研究が進んでいます。本研究の成果は、ダウン症の治療の選択や、今後の治療法の研究に役立つと期待されます。
5. 論文名と著者
- 論文名
N-Acetylcysteine Prevents Amyloid-β Secretion in Neurons Derived from Human Pluripotent Stem Cells with Trisomy 21 doi: 10.1038/s41598-021-96697-7 - ジャーナル名
Scientific Reports - 著者
Hiromitsu Toshikawa1,2,3,9, Akihiro Ikenaka1,9, Li Li4, Yoko Nishinaka-Arai1,5, Akira Niwa1, Akira Ashida2, Yasuhiro Kazuki6,7, Tatsutoshi Nakahata1, Hiroshi Tamai2,8, David W. Russell4, Megumu K. Saito1,* - 著者の所属機関
- 京都大学iPS細胞研究所
- 大阪医科薬科大学小児科
- 済生会吹田病院
- ワシントン大学
- 京都大学医学部人間健康科学科
- 鳥取大学染色体工学研究センター
- 鳥取大学医学部
- 大阪医科薬科大学小児高次脳機能研究所
- 共同筆頭著者
6. 本研究への支援
本研究は、下記機関より支援を受けて実施されました。
- AMED再生医療実現ネットワークプログラム 中核拠点
- AMED再生医療実現ネットワークプログラム
疾患特異的iPS細胞の利活用促進・難病研究加速プログラム - JST CREST