2022-01-26 東京大学,日本医療研究開発機構
発表者
小林 修(東京大学大学院理学系研究科化学専攻 教授)
石谷 暖郎(東京大学大学院理学系研究科化学専攻 特任教授)
齋藤 由樹(東京大学大学院理学系研究科化学専攻 特任助教)
発表のポイント
- 尿路結石や前立腺肥大症に対して用いられる排尿障害治療剤(商品名:ハルナール)の医薬有効成分であるタムスロシンの連続合成を達成した。
- タムスロシンは、排尿障害治療剤として全世界90カ国以上で承認・販売されており、今後高齢化する社会における需要は更に高まっていくと予想されている。
- 適切な合成ルート設計と研究グループが独自に開発した高性能な固定化触媒により、医薬有効成分の様な複雑な構造を有する光学活性化合物(注1)の連結・連続生産が可能となることが実証された。
発表概要
医薬品等の高付加価値化合物の連続生産は高効率・オンデマンド・省スペースな製造プロセスを実現する次世代の製造法として注目を集めている。石油化学等のバルクケミカルの製造ではすでに連続合成が実現されている一方、複雑な構造を有するファインケミカルの合成では多段階での合成が必要となるため連続合成への展開は非常に限定的であった。
本研究は不均一系触媒(注2)を用いるフロー水素化反応を活用することで医薬有効成分であるタムスロシンの連結・連続合成を達成した。触媒的水素化反応を基軸とする合成ルートの設計を行い、独自に開発した固定化パラジウム触媒を用いることで、鍵となるフェネチル基の加水素分解反応とニトリルとの還元的アミノ化反応を温和な反応条件下高収率で実現した。本合成により4段階の反応を中間体の単離・精製を行うことなく、タムスロシンを直接良好な収率で連続的に得ることが可能となった。
本研究成果は、高性能不均一系触媒を活用するフロー反応を活用することで連結・連続合成が可能であることを実証するものである。今後、更なる高活性・高選択性を有する不均一系触媒の開発により、さまざまな医薬品の連続生産が実現されると期待される。
本研究成果は、ドイツの化学雑誌「Angewandte Chemie International Edition」のオンライン速報版で日本時間2022年1月26日午前0時に公開された。
発表内容
研究の背景
タムスロシン(1a)は山之内製薬(現 アステラス製薬)により開発されたα1受容体遮断薬であり、前立腺肥大症に伴う排尿障害治療剤(商品名:ハルナール)として全世界90カ国以上で承認・販売されている。特に米国では全医薬品中28番目に多く処方されており、今後高齢化する社会における需要は更に高まっていくと予想される。一方で、一般的に医薬品のような複雑な構造を有する化合物のほとんどはバッチ法と呼ばれるタンク型の反応器を用いて合成されているが、近年医薬品・機能性材料といった高付加価値化合物の製造法を刷新する動きが盛んになっている。連続フロー法(注3)と呼ばれる新たな手法は、原料溶液を筒状の反応器に連続的に送液することで目的物を連続的に得る製造法であり、従来までのバッチ法と比較し効率性・安全性・環境調和性に優れる。しかしながら、高付加価値化合物のフロー合成では中間体の単離・精製を行うことなく多段階の反応を行うため、各反応における過剰量の試薬・副生成物・共生成物を最小限にする必要があり挑戦的な課題であった。
研究の内容
本研究では、水素化反応を基軸とする合成ルートの設計と高機能固定化パラジウム触媒の開発により、タムスロシンの連結・連続合成を達成した。連続フロー法での不均一系触媒を用いる水素化反応は、バッチ法での反応とは異なりガスと固体触媒が直接反応できるため効率的に反応が進行する。また、共生成物は水などの無害かつ除去が容易な化合物であり、しかも原子効率に優れた反応であるため、連結・連続フロー法に適した反応形式である。これまで、研究グループではフロー水素化反応のための市販の触媒性能を大きく上回る独自の固定化触媒の開発を行ってきた。本合成ではこれまで開発してきた固定化パラジウム触媒を活用し、適切な反応剤を用いることで不斉炭素の構築・脱保護・骨格形成反応の3ステップ全てを水素化反応で行っている(図1)。
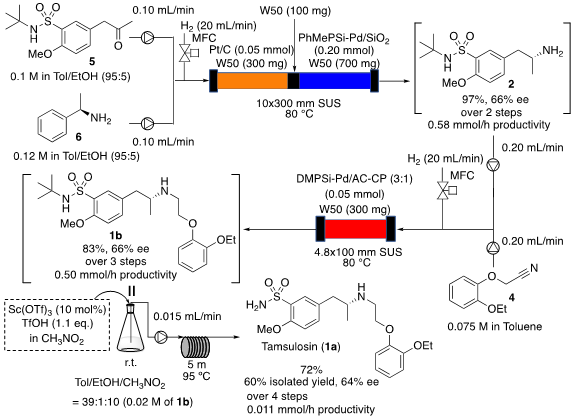
図1: (R)-タムスロシンの連結・連続合成
合成が容易なケトン(5)を出発物質として、1段階目ではPt/C触媒を用いる光学活性アミン(6)との立体選択的還元的アミノ化反応により、第二級アミン(7)を良好な立体選択性で得ている。
2段階目のフェネチル基の加水素分解反応により鍵中間体である光学活性第一級アミン(2)を合成しているが、本反応では独自に開発を行った固定化パラジウム触媒が市販のパラジウム触媒を大きく上回る活性・耐久性を発揮し、11時間以上の連続反応も可能であった。また、この2段階の反応は同一カラム内に2種の触媒を充填することにより単一のカラムを用いた反応も可能であった。
3段階目では還元的C-N結合生成反応によりタムスロシンの分子骨格形成を行っている。通常の還元的C-N結合生成反応ではアルデヒドやケトンを基質として用いるが、本反応ではより安定性の高いニトリル(4)を基質として用いている。このような基質を用いるC-N結合生成反応はほとんど報告されていないが、独自に開発した固定化パラジウム触媒を用いることで目的物(1b)を高収率で得ることに成功した。
特に本反応はバッチ条件ではほとんど反応が進行しないのに対し、フロー条件では温和な反応条件で目的物が得られ、フロー反応の優位性が示された。最終段階のSc(OTf)3を触媒とするtBu基の脱保護もフロー反応にて行い、総収率60%でタムスロシン(1a)の連結・連続合成を達成した。本合成は中間体の単離・精製を行うことなく直接最終生成物を連続的に合成することを可能とし、共生成物は水・エチルベンゼン・アンモニア・イソブテンと全て揮発性の低分子量化合物のみであるため、容易に生成物と分離が可能である。
今後の展開
本研究成果は、触媒的水素化反応と高性能不均一系触媒を活用することで複雑な分子の連結・連続合成が可能となることを実証するものである。特に、医薬品などの光学活性高付加価値化合物の連続合成は今後ますます需要が高まると考えられ、本研究で示された不均一系触媒反応による連結合成を活用することでさまざまな医薬品の連続合成の実現が期待される。
本研究は、日本医療研究開発機構(AMED)創薬基盤推進研究事業の支援を受け、研究課題「原薬の実生産に向けたフロー精密有機合成の高度化」の一環として行われた。
発表雑誌
- 雑誌名
- Angewandte Chemie International Edition
- 論文タイトル
- Continuous-Flow Synthesis of (R)-Tamsulosin Utilizing Sequential Heterogeneous Catalysis
- 著者
- Yuki Saito, Ken Nishizawa, Benjamin Laroche, Haruro Ishitani, Shū Kobayashi *
- DOI番号
- 10.1002/anie.202115643
用語解説
- (注1)光学活性化合物
- 分子が自身の鏡像と重ね合わせられない場合これをキラル分子といい、鏡像体のペアは「右手型」と「左手型」に分類される。どちらかの型が過剰に存在する場合旋光性を有し、その様な化合物は光学活性化合物と呼ばれる。医薬有効成分のほとんどはキラル分子であり、片方の異性体のみが目的の生理活性を有するため、化合物には非常に高い光学純度が求められる。
- (注2)不均一系触媒
- 触媒は均一系触媒と不均一系触媒に分類される。均一系触媒は金属錯体など反応溶液に溶解する触媒であり、合成や構造のチューニングが容易である一方、反応終了後に生成物との分離が必要となり、触媒の回収・再使用も困難である。不均一系触媒は固体そのものや固体表面に活性種が固定化された触媒である。一般に、不均一系触媒は高選択性の実現や活性種の溶出が問題となる一方、触媒の分離・回収・再使用がろ過により容易に可能である利点を有する。
- (注3)連続フロー法
- 反応原料を連続的に反応器に供給し、同時に生成物を反応器から連続的に取り出す合成法を連続フロー法と呼ぶ。不均一系触媒を用いる場合は触媒が充填された筒状のカートリッジを反応器として使用する。送液速度や運転時間を調整することでさまざまなスケールの合成に対応でき、省スペース・高エネルギー効率・安全性といった利点を有する。
お問い合わせ先
研究に関すること
東京大学大学院理学系研究科化学専攻
教授 小林 修 (コバヤシ シュウ)
報道に関すること
東京大学大学院理学系研究科・理学部
主事員 吉岡奈々子、教授・広報室長 飯野 雄一
AMEDの事業に関すること
日本医療研究開発機構 創薬事業部 医薬品研究開発課
創薬基盤推進研究事業