NMDA受容体の活性を調節することが治療成功の鍵であることを発見 Scientists discover that modulating NMDA receptor activity is the key to successful treatment
2022-04-13 大韓民国・基礎科学研究院(IBS)
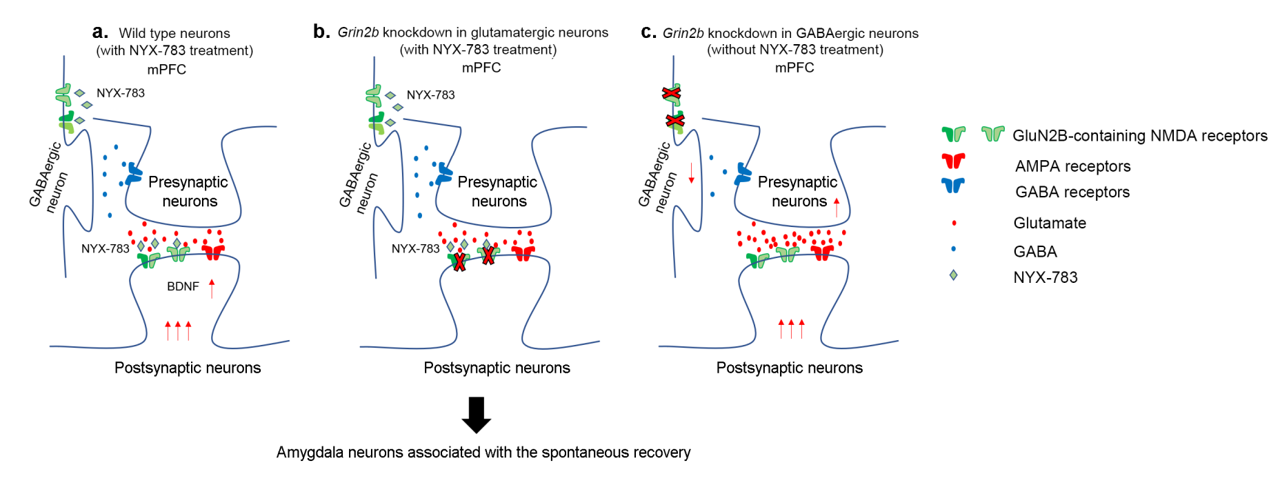 Figure 3. Putative molecular mechanism of PTSD treatment. A) In normal mice, NYX-783 acts on the GluN2B subunit of NMDA receptors in glutamatergic neurons, which results in upregulation of BDNF and inhibition of PTSD spontaneous recovery. B) When GluN2B is knocked down in glutamatergic neurons, it eliminated the effectiveness of NYX-783, since the drug no longer has a valid target. C) When GluN2B is knocked down in GABAergic neurons, it lessens the degree of inhibition on the glutamatergic neuron. More glutamate is released, which activates the postsynaptic pyramidal neuron, resulting in a baseline reduction in spontaneous recovery.
Figure 3. Putative molecular mechanism of PTSD treatment. A) In normal mice, NYX-783 acts on the GluN2B subunit of NMDA receptors in glutamatergic neurons, which results in upregulation of BDNF and inhibition of PTSD spontaneous recovery. B) When GluN2B is knocked down in glutamatergic neurons, it eliminated the effectiveness of NYX-783, since the drug no longer has a valid target. C) When GluN2B is knocked down in GABAergic neurons, it lessens the degree of inhibition on the glutamatergic neuron. More glutamate is released, which activates the postsynaptic pyramidal neuron, resulting in a baseline reduction in spontaneous recovery.
PTSDをその根源から取り組むために、基礎科学研究所内の認知・社会性研究センターの研究者は、イェール大学と共同で、PTSD治療の分子メカニズムを探りました。Molecular Psychiatry誌に掲載された最新の研究では、NYX-783というPTSDの治験薬をマウスで実験し、その作用の分子メカニズムを調べました。NYX-783は、神経細胞におけるNMDARの機能を調節することが知られている新発見の薬剤です。
<関連情報>
- https://www.ibs.re.kr/cop/bbs/BBSMSTR_000000000738/selectBoardArticle.do?nttId=21197&pageIndex=1&searchCnd=&searchWrd=
- https://pubmed.ncbi.nlm.nih.gov/35418600/
脳下垂体におけるN-methyl-D-aspartate受容体のポジティブモジュレーションは恐怖の自然回復を減少させる Positive modulation of N-methyl-D-aspartate receptors in the mPFC reduces the spontaneous recovery of fear
Boyoung Lee , Santosh Pothula , Min Wu , Hyeyeon Kang , Matthew J Girgenti , Marina R Picciotto , Ralph J DiLeone , Jane R Taylor , Ronald S Duman
Molecular Psychiatry Published:2022 Apr 14
doi: 10.1038/s41380-022-01498-7
Abstract
N-methyl-D-aspartate receptor (NMDAR) modulators have recently received increased attention as potential therapeutics for posttraumatic stress disorder (PTSD). Here, we tested a novel NMDAR-positive modulator, NYX-783, in the following two rodent models of PTSD: an auditory fear-conditioning model and a single-prolonged stress (SPS) model. We examined the ability of NYX-783 to reduce subsequent fear-based behaviors by measuring enhanced fear extinction and reduced spontaneous recovery (spontaneous return of fear) in male mice. NYX-783 administration significantly reduced spontaneous recovery in both PTSD models and enhanced fear extinction in the SPS model. Furthermore, NYX-783 increased the NMDA-induced inward currents of excitatory and inhibitory neurons in the infralimbic medial prefrontal cortex (IL mPFC) and that the GluN2B subunit of NMDARs on pyramidal neurons in the IL mPFC is required for its effect on spontaneous recovery. The downstream expression of brain-derived neurotrophic factor was required for NYX-783 to achieve its behavioral effect. These results elucidate the cellular targets of NYX-783 and the molecular mechanisms underlying the inhibition of spontaneous recovery. These preclinical findings support the hypothesis that NYX-783 may have therapeutic potential for PTSD treatment and may be particularly useful for inhibiting spontaneous recovery.