2022-06-28 理化学研究所,ロボティック・バイオロジー・インスティテュート株式会社,エピストラ株式会社,科学技術振興機構
理化学研究所(理研)生命機能科学研究センター網膜再生医療研究開発プロジェクト(研究当時)の神田元紀上級研究員(研究当時、現バイオコンピューティング研究チーム上級研究員)、髙橋政代プロジェクトリーダー(研究当時、現バトンゾーン研究推進プログラム眼科領域遺伝子細胞治療研究チーム客員研究員、株式会社VC Cell Therapy代表取締役)、バイオコンピューティング研究チームの髙橋恒一チームリーダー、ロボティック・バイオロジー・インスティテュート株式会社の夏目徹取締役、エピストラ株式会社の都築拓取締役・CTO、小澤陽介代表取締役・CEOらの共同研究グループは、細胞培養の条件検討を自律的に試行錯誤するロボット・AIシステムを開発し、実際に再生医療で用いられる細胞培養のレシピを改善させることに成功しました。
本研究成果は、科学実験のデザインと実行を自動化する要素技術となり、生命科学実験全般の効率的な試行錯誤や再現性の向上に貢献すると期待できます。
今回、共同研究グループは、高精度な生命科学実験動作が可能な汎用ヒト型ロボットLabDroid「まほろ」[1]と新たに開発した人工知能(AI)ソフトウェア(最適化アルゴリズム)を組み合わせたシステムを設計し、このシステムがiPS細胞(人工多能性幹細胞)[2]から網膜色素上皮細胞(RPE細胞)[3]への分化誘導工程において、分化誘導効率を高める培養条件を人間の介在なしに自律的に発見できることを実証しました。
本研究は、科学雑誌『eLife』(6月28日付:日本時間6月28日午後4時)に掲載されました。
背景
科学は人類の英知を広げる営みであり、科学の自動化はこの営みを究極的に加速させる方法です。研究は数多くの実験によって成り立ち、個々の実験は多くの条件検討と数回の本番実験で構成されます。条件検討は、実験が成立するための反応時間・試薬濃度・操作順序などの細かいパラメータを探索する工程であり、膨大な試行錯誤が求められます。
この試行錯誤を自動化する取り組みとして、科学実験を人間の介在なしに自律的に実行する「自律実験」がさまざまな分野で開発されつつあります。自律実験は、ロボットによる実験操作と人工知能(AI)による実験結果の評価、および次の実験計画の策定までの一連のプロセスを繰り返します。
例えば、これまでに、英国リバプール大学の研究チームは燃料電池に用いる光触媒混合物の組成比を対象として、混合物の活性を向上させる組成を自走式ロボットとAIによって自律的に探索することに成功しています注1)。また、米国イリノイ大学の研究チームは微生物による物質生産を対象として、生産効率を向上させる微生物の遺伝子配列の組み合わせをレール付き単腕ロボットとAIによって自律的に探索することに成功しています注2)。
このように、いくつかの分野では自律実験の成功例が出つつあるものの、iPS細胞(人工多能性幹細胞)の分化誘導に代表される再生医療分野や細胞生物学分野での実施例はありませんでした。特に、細胞培養は、微細な操作の違いが品質に大きな影響を与えること、分化誘導には長時間(数週間~数カ月)の培養が必要であることの二つが技術検証の障壁となっていました。
そこで、共同研究グループは、滲出型加齢黄斑変性[4]を含む網膜色素上皮(RPE)不全症[5]の再生医療において重要な工程である、iPS細胞から網膜色素上皮細胞(RPE細胞)への分化誘導をモデル実験として、高精度な生命科学実験動作が可能な汎用ヒト型ロボットLabDroid「まほろ」と今回開発した人工知能(AI)ソフトウェア(最適化アルゴリズム)を組み合わせた細胞培養分野における自律実験の実証に取り組みました。
注1)Burger et al. “A mobile robotic chemist”. Nature, 2020
注2)HamediRad et al. “Towards a fully automated algorithm driven platform for biosystems design”. Nature Communications, 2019
研究手法と成果
本研究は、次の(1)プロトコルのロボット実装、(2)自律実験戦略の決定、(3)実証実験の三つのステップで実施しました。
(1)プロトコルのロボット実装
まず、iPS細胞からRPE細胞への分化誘導工程をA~Eの五つの工程に分解し、それぞれの工程に必要な手順(プロトコル)の動作をLabDroid「まほろ」に実装しました(図1)。1回の実験につき8枚の6ウェル(穴)プレートを扱うことで、合計48個のウェルでの細胞培養を同時に実行できるように設計しました。

図1 iPS細胞からRPE細胞への分化誘導工程を実装したLabDroid「まほろ」
iPS細胞から分化誘導したRPE細胞を患者に移植するまでの全工程のうち、分化誘導工程を自律実験の対象とした。分化誘導工程はA~Eの5ステップに分けられる。
実際にロボットを用いて培養を行ったところ、48個のウェル全てで、分化したRPE細胞を示す着色細胞が出現したことから、当該プロトコルをロボットに正常に実装できたことが分かりました。分化前のiPS細胞は無色であり、分化後のRPE細胞は茶色の細胞であるため、分化誘導の効率を着色した細胞の割合で評価することができます。この結果、ウェル内における着色細胞の割合は4~5割程度であったことから、分化誘導効率は不十分であり、さらなる向上が求められました(図2)。
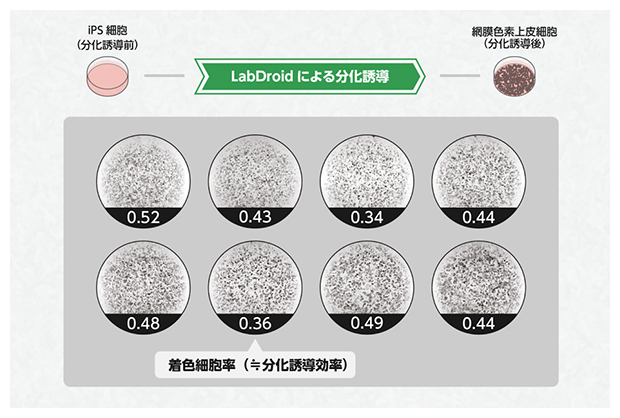
図2 LabDroid「まほろ」が分化誘導したRPE細胞の分化誘導効率(着色状態)
一般的な人間の手作業と同じ条件(標準条件)で、LabDroid「まほろ」が分化誘導を行った結果。黒い部分は正しく分化誘導されたと考えられるRPE細胞、白い部分はそれ以外の細胞を示す。全ての条件で4~5割程度の着色が観察された。
このときの培養条件と動作は、一般的な人間の手作業と同じ条件(以下、標準条件)でした。標準条件をそのままロボットに実装した場合に誘導効率が不十分であったという事実は、記録されていない人間の動きを含む物理的な諸条件を詳細に記述することは本質的に困難であることや、そもそもロボットと人間では、最適な条件が異なることを示唆します。そこで次に、自律実験によりロボットが培養する際の分化誘導効率の向上を試みました。
(2)自律実験戦略の決定
iPS細胞からRPE細胞への分化誘導工程には、試薬の濃度や処理時間、細胞を取り扱う際の強度など、適切に設定すべきさまざまな数値(パラメータ)が存在します。本研究では、分化誘導効率を向上させるパラメータの組み合わせを導出するための戦略を「ブラックボックス最適化問題」として定式化し、具体的な手法を選択しました。
細胞培養においては、細胞の内部状態が複雑であるため、どのパラメータをどう変化させると分化誘導効率が向上するかを直感的に導き出すことは困難です。このように入力と出力の関係性が不明な状況を「ブラックボックス」と呼び、ブラックボックスの出力を最大化/最小化する入力を、試行錯誤を通じて発見する問題をブラックボックス最適化問題と呼びます。本研究では、ブラックボックス最適化問題を解決するアルゴリズムとしてよく用いられるベイズ最適化[6]を、自律実験のための最適化手法として利用することにしました。
一方で、一般的なベイズ最適化は実験→評価→計画を1条件ずつ多数ラウンド繰り返すものですが、iPS細胞からRPE細胞への分化誘導工程は1ラウンドあたり40日間の培養を要するため、一般的なベイズ最適化を単純に適用することは現実的ではありませんでした。そこで本研究では、ベイズ最適化の拡張手法として用いられるバッチベイズ最適化[6]を採用しました。バッチベイズ最適化は1ラウンドあたりの条件を複数条件化したものであり、本研究では最終的に48条件の実験→48条件の評価→48条件の計画を3ラウンド繰り返しています。
次に、バッチベイズ最適化を適用するために必要な変化させるパラメータ(探索範囲)と、最大化させたい値(評価値)を定めました。探索範囲は専門家の助言と計算機によるシミュレーションを参考にして、iPS細胞からRPE細胞への分化誘導工程のうち七つをパラメータと定めました(図3)。また、評価値は分化誘導効率として着色細胞率を用いることにしました。
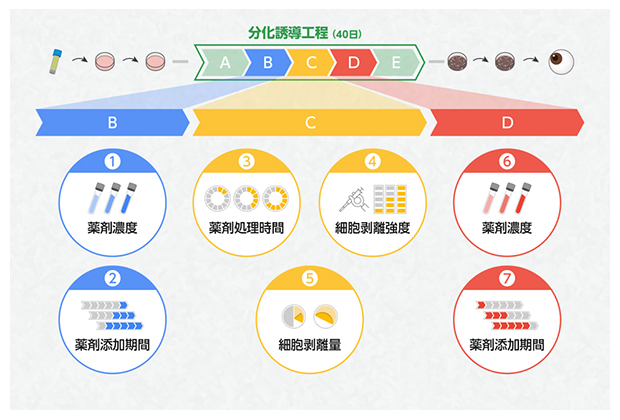
図3 本研究で設定した探索範囲のパラメータ
試薬の濃度や処理時間、細胞を取り扱う際の強度など適切に設定すべきさまざまな数値(パラメータ)から、専門家の助言と計算機によるシミュレーションを参考にして、A~Eの分化誘導工程のうちステップBから二つ、ステップCから三つ、ステップDから二つの計七つのパラメータを探索範囲として選択した。
以上により、本研究では以下の3要件を自律実験戦略として決定し、戦略を実行可能な人工知能(AI)ソフトウェア(最適化アルゴリズム)を開発しました(図4)。
- バッチベイズ最適化を用いる。
- 分化誘導効率(着色細胞率)を向上させる七つのパラメータの組み合わせを探索する。
- 1ラウンドあたり48条件の実験を行う。
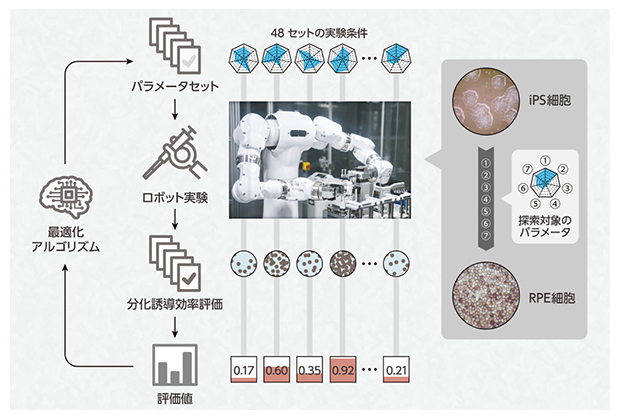
図4 本研究の自律実験戦略とワークフロー
48セットの実験条件をLabDroid「まほろ」が実際に実験し、それぞれの条件における分化誘導効率(着色細胞率)を評価する。実験結果を基に、最適化アルゴリズムは次のラウンドで実施すべき48セットの実験条件を提案する。実験計画・実験実行・評価・予測を繰り返すことで、最適なパラメータを探索する。
(3)実証実験
最初のラウンドには過去の結果が存在しないため、ラウンド1の実験計画はランダムにパラメータセットを47セット設定し、比較のための一つの標準条件を加えた計48条件でロボットによる分化誘導操作を行い、それぞれの条件における分化誘導効率(着色細胞率)の値を獲得しました(図5左)。続くラウンド2では、ラウンド1の結果を基に最適化アルゴリズムにより導出された46条件およびラウンド1における上位2条件(比較のための対照条件)のパラメータセットを用いて、ロボットによる分化誘導操作と評価値の取得を行いました(図5中)。さらにラウンド3では、ラウンド1およびラウンド2の結果を基に最適化アルゴリズムにより導出された46条件およびラウンド2における上位2条件(比較のための対照条件)のパラメータを用いて、ロボットによる分化誘導操作と評価値の取得を行いました(図5右)。3ラウンド合計で144条件(うちラウンド1の1条件は機器エラーにより失敗したため除外)の分化誘導培養を実施した結果、ラウンド3において最も高い評価値(91%)を獲得することに成功しました。
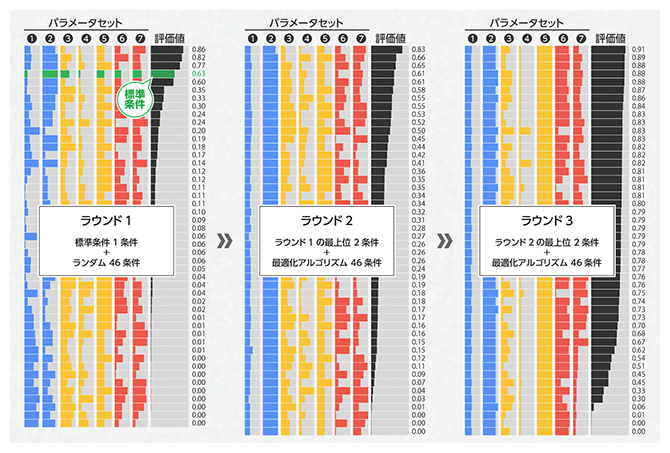
図5 実証実験の結果
ラウンド1~3におけるパラメータセット(実験条件)と評価値(着色細胞率)。ラウンド1の緑色は標準条件を示す。ラウンド3において最も高い評価値(91%)を獲得した。
最後に、これまでの培養は各条件1ウェルのみで行ったため、高い評価値を得た条件が偶然によるものではないことを検証するために、ラウンド3の上位5条件と探索前の条件の計6条件で複数ウェルにおける最終評価試験を行いました。その結果、ラウンド3の上位5条件は全てにおいて、探索前の条件に対して統計学的に有意に評価値が向上していると判定されました。
これらの結果から、汎用ヒト型ロボットLabDroid「まほろ」と最適化アルゴリズムを組み合わせたシステムにより、iPS細胞からRPE細胞への分化誘導効率を高める培養条件を人間の介在なしに自律的に発見し、細胞培養分野における自律実験が可能であることが示されました。
今後の期待
本研究の成果は、科学の自動化を達成するための要素技術となり、生命科学実験全般の効率的な試行錯誤や再現性の向上に寄与し、生命科学研究を加速するものと考えられます。今回の研究では、iPS細胞からRPE細胞への分化誘導工程をモデルとした実証を行いましたが、原理的にはLabDroid「まほろ」と最適化アルゴリズムの組み合わせを用いることで、多くの生命科学実験における試行錯誤を自律的に遂行可能になると考えられます。
分化誘導や細胞移植を伴う再生医療の基礎研究では、高水準の細胞培養が求められますが、培養者の手技の差や暗黙知に起因して効率的な技術移転が難しいことが知られており、研究の進展における大きな問題の一つになっています。本研究の成果は「専門家の手技に依存することなく、ロボットとAIのみで専門家と同等の高品質な結果を得る条件の探索に成功した」とも捉えることができます。技術移転がかなわずに共有されてこなかった「匠の技」を広く世界に開放するための一つの方法論になりえると期待できます。
これからの生命科学分野の実験室では、ロボット・AI・人間の協同作業がこれまで以上に増えることが予想されます。今回のシステムでは、対象工程・探索範囲・評価値の定義は専門知識を持つ人間が担当し、ロボットとAIが実験の試行錯誤をするという役割分担がなされています。この役割分担により、研究者は知的創造に専念することが可能になります。さらに技術開発が進んだ未来では、ロボット・AI・人間はどのようなパートナーシップを結ぶのでしょうか(図6)。

図6 近未来の研究室像
さまざまなロボットやAIが実験の遂行を担当し、研究者は知的創造に専念する。
補足説明
1.汎用ヒト型ロボットLabDroid「まほろ」
ロボティック・バイオロジー・インスティテュート株式会社(株式会社安川電機の子会社)により開発された生命科学実験用のヒューマノイドロボットシステム。株式会社安川電機の産業用7軸双腕ロボットの周辺に、人間が実験で用いるものと同じ実験器具を配置している。ピペット操作やインキュベーターの扉の開け閉めなど、人間が手で行っていた実験操作がロボットでも実行可能になった。
2.iPS細胞(人工多能性幹細胞)
成人の皮膚細胞などの体細胞にOct3、Sox2、Klf4遺伝子などを導入して初期化し多能性を持たせることで、人工的に作製した多能性幹細胞。
3.網膜色素上皮細胞(RPE細胞)
網膜を構成する細胞の一つ。理研や神戸市立神戸アイセンター病院などにより、iPS細胞由来RPE細胞を用いた再生医療の臨床研究が行われている。RPEはretinal pigment epitheliumの略。
参考:
-
- 2014年9月18日お知らせ「滲出型加齢黄斑変性に対する自家iPS細胞由来網膜色素上皮シート移植に関する臨床研究」第1症例目の被験者の退院について」
- 2017年3月28日お知らせ「滲出型加齢黄斑変性に対する他家iPS細胞由来網膜色素上皮細胞懸濁液移植に関する臨床研究」の1例目の移植手術の実施について」
- 2021年3月11日神戸市立神戸アイセンター病院プレスリリース「網膜色素上皮(RPE)不全症に対する同種 iPS細胞由来 RPE細胞懸濁液移植に関する臨床研究」の1例目の移植手術の実施について(外部サイト)」
4.滲出型加齢黄斑変性
加齢黄班変性とは加齢により網膜の中心部である黄斑に障害が発生して、見えにくくなる疾患で、滲出型と萎縮型がある。滲出型は異常な血管(脈絡膜新生血管)が脈絡膜から網膜色素上皮の下あるいは網膜と網膜色素上皮の間に侵入して網膜に障害が起こる病気。異常な血管は、血液の成分を漏出させたり、破れたりする。血液成分が漏出すると網膜が腫れたり(網膜浮腫)、網膜下に液体が溜まったり(網膜下液)して、網膜が正常に働かなくなり視力が低下する。血管が破れると出血し、網膜に障害を引き起こす。
5.網膜色素上皮(RPE)不全症
網膜色素上皮細胞の異常が原因で起こる網膜変性疾患の疾患群。加齢黄斑変性の萎縮型、網膜色素変性の一部およびその類縁疾患などが該当する(神戸市立神戸アイセンター病院報道発表資料より一部改変して転載)。
6.ベイズ最適化、バッチベイズ最適化
ベイズ最適化はこれまでの実験結果を基に、良いと予測される条件(活用)とまだ実験していない未知の条件(探索)をバランス良く選ぶアルゴリズム。形状が不明な関数(ブラックボックス関数)の最大値や最小値を求めるために用いられる。通常は、実験→評価→計画を1条件ずつ多数ラウンド繰り返すが、1ラウンド当たりの条件を複数条件化したものがバッチベイズ最適化と呼ばれる。本研究では、48条件の実験→48条件の評価→48条件の計画を繰り返している。
共同研究グループ
理化学研究所 生命機能科学研究センター
網膜再生医療研究開発プロジェクト(研究当時)
プロジェクトリーダー(研究当時) 髙橋 政代(タカハシ・マサヨ)
(現 バトンゾーン研究推進プログラム 眼科領域遺伝子細胞治療研究チーム 客員研究員、株式会社VC Cell Therapy代表取締役)
上級研究員(研究当時) 神田 元紀(カンダ・ゲンキ)
(現 バイオコンピューティング研究チーム 上級研究員)
テクニカルスタッフⅡ(研究当時) 寺田 基剛(テラダ・モトキ)
(現 株式会社VC Cell Therapy)
テクニカルスタッフⅠ(研究当時) 坂井 徳子(サカイ・ノリコ)
(現 株式会社VC Cell Therapy)
大学院生リサーチ・アソシエイト(研究当時) 許沢 尚弘(モトザワ・ナオヒロ)
研究員(研究当時) 増田 智浩(マスダ・トモヒロ)
(現 株式会社VC Cell Therapy)
テクニカルスタッフⅡ(研究当時) 西田 光宏(ニシダ・ミツヒロ)
(現 株式会社VC Cell Therapy)
上級研究員(研究当時) 砂川 玄志郎(スナガワ・ゲンシロウ)
(現 老化分子生物学研究チーム 上級研究員)
バイオコンピューティング研究チーム
チームリーダー 髙橋 恒一(タカハシ・コウイチ)
ロボティック・バイオロジー・インスティテュート株式会社
代表取締役社長 松熊 研司(マツクマ・ケンジ)
取締役 夏目 徹(ナツメ・トオル)
チームリーダー(研究当時) 亀井 泉寿(カメイ・モトヒサ)
(現 株式会社安川電機)
開発員 工藤 拓(クドウ・タク)
エピストラ株式会社
代表取締役・CEO 小澤 陽介(オザワ・ヨウスケ)
代表取締役・COO 櫻田 剛史(サクラダ・タケシ)
取締役・CTO 都築 拓(ツヅキ・タク)
リサーチエンジニア 東 達軌(ヒガシ・タツキ)
リサーチエンジニア 堀口 修平(ホリグチ・シュウヘイ)
リサーチエンジニア(研究当時) 渡邉 千早(ワタナベ・チハヤ)
研究支援
本研究は、理化学研究所運営費交付金(生命機能科学研究)で実施し、科学技術振興機構(JST)「未来社会創造事業」の「探索加速型・共通基盤領域(運営統括:長我部信行)」における研究課題「ロボティックバイオロジーによる生命科学の加速(研究代表者:髙橋恒一)」、日本医療研究開発機構(AMED)再生医療実現拠点ネットワークプログラム「疾患・組織別実用化研究拠点(拠点A)」の「視機能再生のための複合組織形成技術開発および臨床応用推進拠点(拠点長:髙橋政代)」による支援および新エネルギー・産業技術総合開発機構(NEDO)の委託業務により行われました。
原論文情報
Genki N. Kanda*,#, Taku Tsuzuki*, Motoki Terada, Noriko Sakai, Naohiro Motozawa, Tomohiro Masuda, Mitsuhiro Nishida, Chihaya T. Watanabe, Tatsuki Higashi, Shuhei A. Horiguchi, Taku Kudo, Motohisa Kamei, Genshiro A. Sunagawa, Kenji Matsukuma, Takeshi Sakurada, Yosuke Ozawa#, Masayo Takahashi, Koichi Takahashi#, Tohru Natsume#(*共同筆頭著者、#責任著者), “Robotic search for optimal cell culture in regenerative medicine”, eLife, 10.7554/eLife.77007
発表者
理化学研究所
生命機能科学研究センター 網膜再生医療研究開発プロジェクト(研究当時)
上級研究員(研究当時) 神田 元紀(カンダ・ゲンキ)
(現 バイオコンピューティング研究チーム 上級研究員)
プロジェクトリーダー(研究当時) 髙橋 政代(タカハシ・マサヨ)
(現 バトンゾーン研究推進プログラム 眼科領域遺伝子細胞治療研究チーム 客員研究員、株式会社VC Cell Therapy 代表取締役)
バイオコンピューティング研究チーム
チームリーダー 髙橋 恒一(タカハシ・コウイチ)
ロボティック・バイオロジー・インスティテュート株式会社
取締役 夏目 徹(ナツメ・トオル)
エピストラ株式会社
代表取締役・CEO 小澤 陽介(オザワ・ヨウスケ)
取締役・CTO 都築 拓(ツヅキ・タク)
報道担当
理化学研究所 広報室 報道担当
ロボティック・バイオロジー・インスティテュート株式会社 広報担当
エピストラ株式会社 広報・渉外担当
科学技術振興機構 広報課
JST事業に関すること
科学技術振興機構 未来創造研究開発推進部
小泉 輝武(コイズミ・テルタケ)