2024-10-02 量子科学技術研究開発機構,日本医療研究開発機構
発表のポイント
- 肝がんへの進行が懸念される非アルコール性脂肪性肝炎(NASH)の確定診断は現在のところ、肝臓組織を取り出す肝生検が唯一の方法ですが、容易に行えないため、身体を傷つけずに診断する方法が求められています
- 身体への負担が少ないPET 検査の臨床利用を見据え、検査に用いる[11C]グルタミンPET 薬剤の自動合成技術を開発し、NASH 動物モデルにおいて病気の進行や治療薬剤の効果を可視化し、診断法としてだけでなく治療の評価法としての有用性を明らかにしました
- [11C]グルタミンPET はNASH を画像で診断する方法として、またNASH 治療薬剤の効果の評価法として応用が期待されます
概要
量子科学技術研究開発機構(理事長 小安重夫、以下「QST」)量子医科学研究所 先進核医学基盤研究部の謝琳主幹研究員らは、罹患数が日本の人k口の約3~5%と推定される非アルコール性脂肪性肝炎(Nonalcoholicsteatohepatitis:NASH)の進行や治療薬剤の効果をPET 検査で初めて可視化することに成功し、身体に負担が少ないPET 検査がNASH の診断法や治療の評価法として有用であることを明らかにしました。
近年、生活習慣の変化からカロリーの摂取過多が原因となる脂肪肝が増加し、一部はNASH を介して肝がんに進行することが懸念されています。NASH の唯一の確定診断法は肝臓の組織を採取する肝生検ですが、患者への負担が大きく容易には実施できないため、負担が少ない、より簡便な診断方法が期待されています。また、主な治療法は食事および運動療法であり、有効な薬物療法がないため、世界中で創薬や臨床試験が盛んに行われる中、効果を評価する方法も求められています。
NASH では肝臓においてグルタミン代謝1)が亢進していることが知られています。また、マウスにおいてグルタミン代謝酵素であるGLS12)の阻害剤の投与により症状の改善が見られたと国内の他の研究グループから報告がされ(出典)、臨床試験を目指している治療薬候補もあります。そこでQST ではPET 薬剤である[11C]グルタミンの将来的な臨床での利用を見据え、ヒトに投与可能な品質基準で当該PET 薬剤を自動合成する技術を開発しました。さらに自動合成した[11C]グルタミンを用いてNASH の診断や、グルタミン代謝を標的とした薬剤の効果の評価における有用性を検討しました。
 GLS1 阻害剤による治療群と無治療群のNASH モデルマウスに対して[11C]グルタミンPET 撮像を行い、肝臓におけるPET 薬剤の放射能濃度とGLS1 遺伝子の発現量およびNASH 病態の進行を反映する病理スコアを比較しました。その結果、無治療群に比べて治療群では放射能濃度、遺伝子の発現量、病理スコアいずれも低くなり、3者間にそれぞれ強い関連性があることが示されました。
GLS1 阻害剤による治療群と無治療群のNASH モデルマウスに対して[11C]グルタミンPET 撮像を行い、肝臓におけるPET 薬剤の放射能濃度とGLS1 遺伝子の発現量およびNASH 病態の進行を反映する病理スコアを比較しました。その結果、無治療群に比べて治療群では放射能濃度、遺伝子の発現量、病理スコアいずれも低くなり、3者間にそれぞれ強い関連性があることが示されました。
[11C]グルタミンPETはNASHを画像で診断する方法として、またNASH治療薬の効果の評価法として臨床での利用が期待されます。また、グルタミン代謝の異常が原因とされる疾患には肥満性糖尿病や動脈硬化症などもあり、これら疾患に対するグルタミン代謝を標的とした治療薬の開発にも有用な可能性があります。
本成果は、薬学分野のトップジャーナルの一つで科学的インパクトの大きい論文が数多く発表されている科学誌「Acta Pharmaceutica Sinica B」のオンライン版に2024年9月30日(月)に掲載されました。
研究開発の背景と目的
我が国において、肝がんは罹患数7位、死亡数5位となっています。これまで肝がんの病因は主に肝炎ウイルスの感染でしたが、生活習慣の変化によって、非アルコール性脂肪性肝炎(non-alcoholic steatohepatitis, NASH)を介した肝がんの割合が増えています。我が国ではNASH罹患数が人口の約3〜5%、400万人と推定され、そのうち約5%が10年で肝がんに進行します(日内会誌 110: 1670〜1676, 2021)。
NASHの唯一の確定診断法は肝生検ですが、患者への負担が大きく容易には実施できないため、負担が少ない、より簡便な診断方法が期待されています。また、主な治療法は食事および運動療法であり、有効な薬物療法がないため、世界中で創薬や臨床試験が盛んに行われる中、効果を客観的に定量的に評価する方法も求められています。
NASHでは肝臓においてグルタミン代謝が亢進しており、グルタミン代謝酵素の一種であるGLS1遺伝子が高発現していることが知られています。また、東京大学医科学研究所らの研究グループは、GLS1阻害剤を投与するとNASHの症状が改善したと報告しており、NASHを含む様々な疾患でGLS 1阻害剤を用いた治療に関する臨床研究の実施を目指しています。これらのことから、我々はグルタミン代謝を標的としたPETが将来的に臨床で利用できると考えました。
そこで本研究では、グルタミン代謝を捉えるPET薬剤[11C]グルタミンを日本核医学会PET薬剤製造基準3)に準拠する品質で、簡便に製造する技術の確立と、[11C]グルタミンPETによるNASHの診断や、グルタミン代謝を標的とした薬剤の効果の評価における有用性を明らかにすることを目的としました。
研究の手法と成果
1.[11C]グルタミンを完全自動合成する技術の確立
まず、サイクロトロンより製造された[11C]二酸化炭素(11CO2)を出発原料として製造した[11C]シアン(H11CN)を複数工程で反応させ、[11C]グルタミンを合成します(図2)。これらの合成過程は、独自に開発した自動合成装置内で進み、[11C]グルタミンを安定した収率と収量で製造できることを確認しました。また、この自動合成装置を用いて製造することにより、日本核医学会PET薬剤製造基準に準拠した製造環境で品質保証された薬剤として、ヒトへの投与も可能となります。

図2. [11C]グルタミンの合成工程と自動合成装置
2.[11C]グルタミンPETによるNASHの診断や、GLS1阻害剤による治療効果の評価における有用性の検討
NASHマウスモデルはメチオニン・コリン欠乏食を与えて飼育することにより作成しました(図3A)。8週経過後の肝臓の組織を観察すると、メチオニン・コリン欠乏食を与えたマウス(NASHマウス)は、通常飼料を与えたマウス(通常マウス)に比べて、脂肪の蓄積や、炎症、線維化が見られ、NASHを発症していることが確認できました。
次に、[11C]グルタミンPETがNASHの診断や、GLS1阻害剤による治療効果の評価において有用かを検討しました。8週後の通常マウス、NASHマウス、およびGLS1阻害剤(BPTES)を投与したNASH治療マウスを用いて、[11C]グルタミンPET、病理組織検査、およびGLS1遺伝子発現解析を行いました。
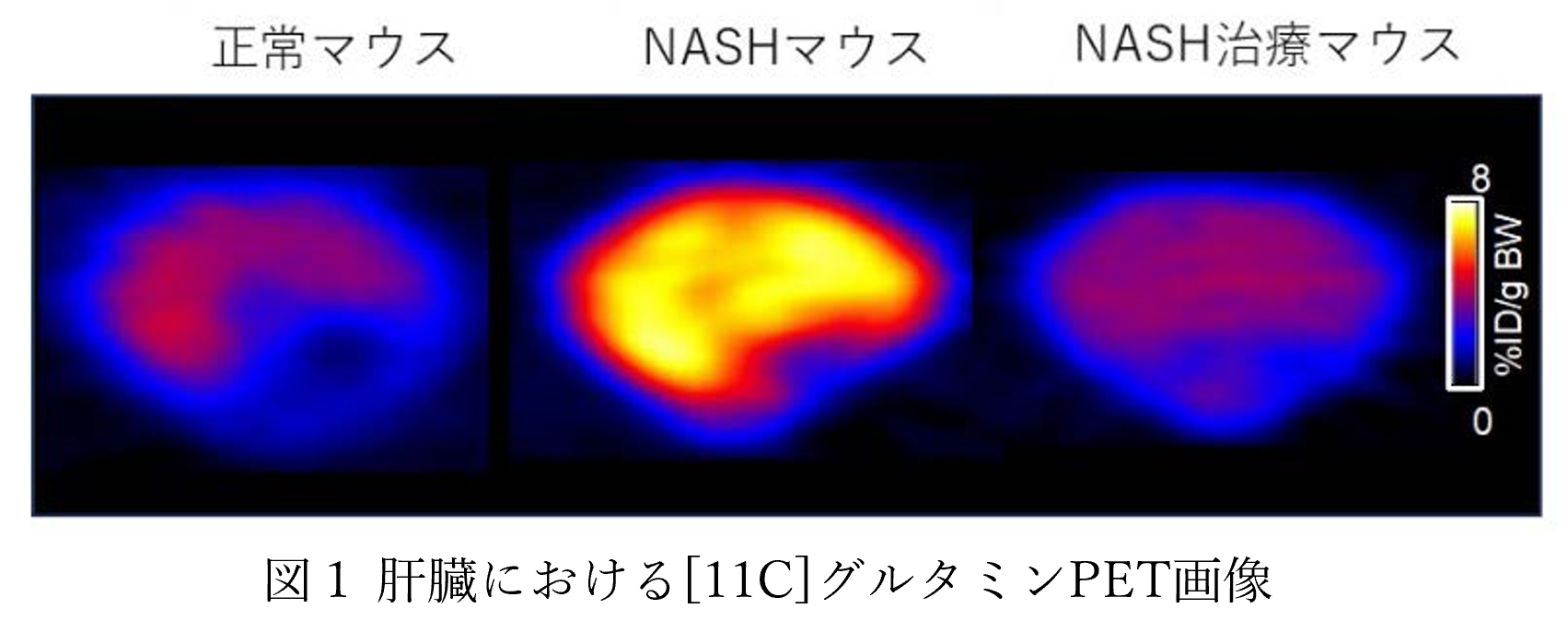
[11C]グルタミンPETの結果、肝臓における放射能濃度は、NASHマウスが最も高く、次いでNASH治療マウス、通常マウスとなりました(図3B)。病理組織検査および免疫染色によるGLS1遺伝子発現解析では、NASHマウスに比べて、NASH治療マウスでは蓄積した脂肪の減少や、炎症と繊維化の改善が認められ、GLS1遺伝子の発現も低下していました(図3C)。
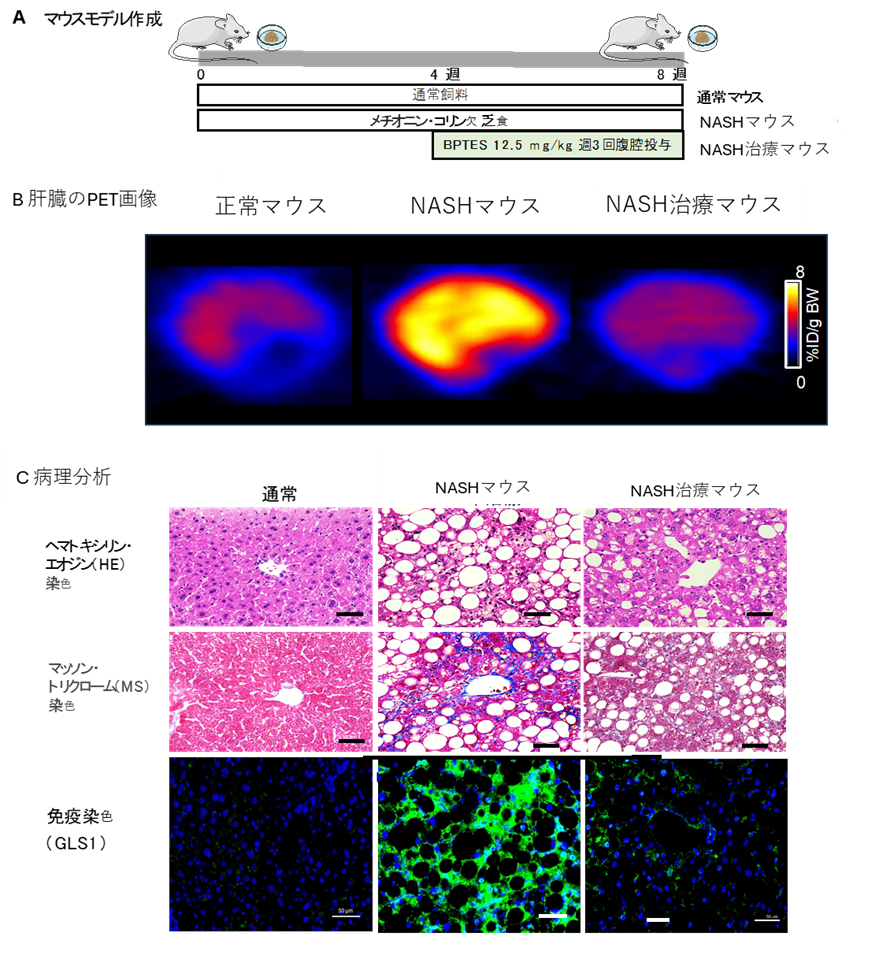
図3. NASHマウスモデルの作成とGLS1阻害剤投与後の解析結果
肝臓における放射能濃度の結果と、GLS1遺伝子の発現量、および病理組織検査の結果を比較したところ、肝臓における放射能濃度がGLS1遺伝子の発現量、NASH病態を反映する病理スコアそれぞれと正比例の相関関係にあることがわかりました(図4)。
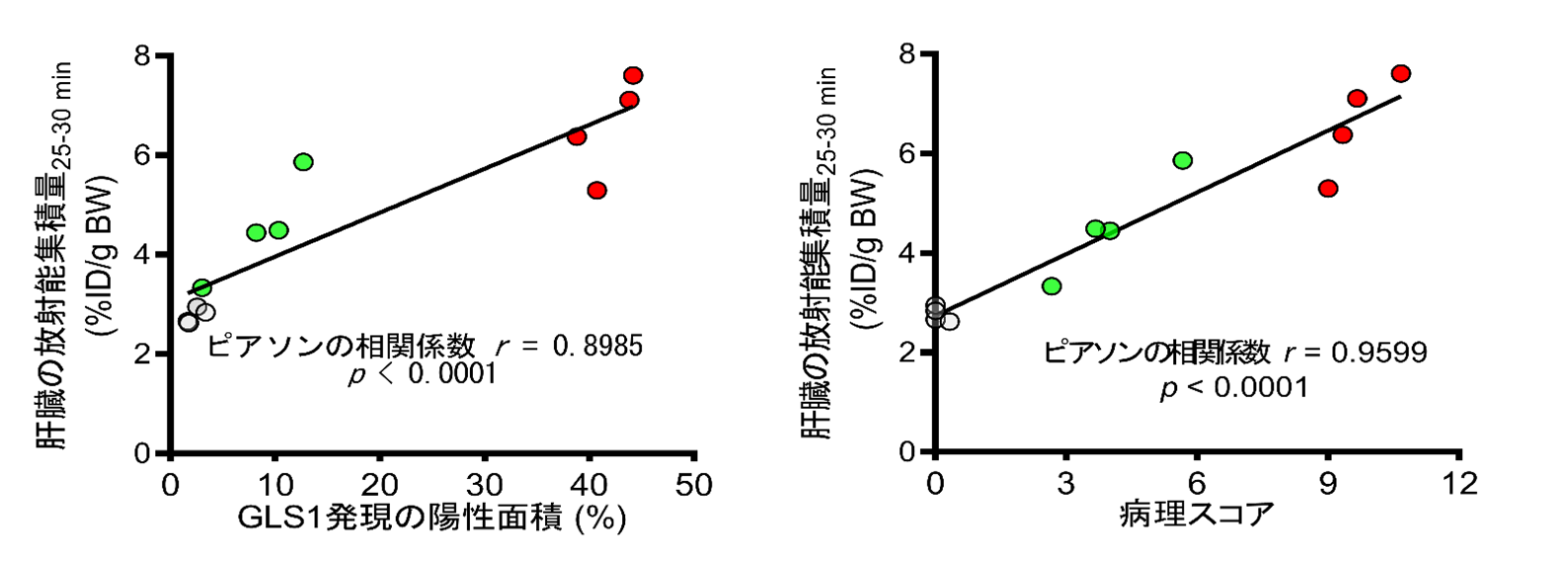
図4. 肝臓内の放射能濃度と GLS1 タンパク質発現(左)およびNASH病理スコアとの相関分析結果
灰色:通常マウス、緑色:NASH治療マウス、赤色: NASHマウス
以上の結果から、[11C]グルタミンPETはNASHの診断や、グルタミン代謝を標的とした薬剤の治療効果を評価に有用と考えられます。
今後の展開
[11C]グルタミンPETはNASHを画像で診断する方法として、また、グルタミン代謝などを標的としたNASH治療薬の効果の評価法として、診断での利用や、NASH治療薬の開発への応用が期待されます(図5)。グルタミン代謝を標的とした薬剤の治療効果を評価する臨床試験では、治療効果を予測する方法として全身のグルタミン代謝を捉えることが重要視されています。グルタミン代謝を標的とした、がんに対する治療薬剤の臨床研究がいくつか進められており、[11C]グルタミンPETは、そうした薬剤が全身のグルタミン代謝に与える影響を評価する方法としても利用できる可能性があります。
![[11C]グルタミン PET/CT マウス全身画像](https://www.qst.go.jp/uploaded/image/23976.png)
図5. [11C]グルタミン PET/CT マウス全身画像
謝辞
本研究は、「ムーンショット型研究開発事業『炎症誘発細胞除去による100歳を目指した健康寿命延伸医療の実現』」、JSPS科研費(JP23K27558、24K21295)における結果を一部活用したものです。
研究助成
AMEDでは、ムーンショット型研究開発事業の目標7「2040年までに、主要な疾患を予防・克服し100歳まで健康不安なく人生を楽しむためのサステイナブルな医療・介護システムの実現」の達成にむけて研究開発を推進しています。
出典
Yoshikazu Johmura, Takehiro Yamanaka, Satotaka Omori, Teh Wei Wang, Yuki Sugiura,
Masaki Matsumoto, Narumi Suzuki, Soichiro Kumamoto, Kiyoshi Yamaguchi, Seira Hatakeyama,
Tomoyo Takami, Rui Yamaguchi, Eigo Shimizu, Kazutaka Ikeda, Nobuyuki Okahashi, Ryuta Mikawa,
Makoto Suematsu, Makoto Arita, Masataka Sugimoto, Keiichi I. Nakayama, Yoichi Furukawa,
Seiya Imoto, and Makoto Nakanishi, Senolysis by glutaminolysis inhibition ameliorates various age-associated disorders, Science, Vol 371, Issue 6526, pp. 265-270
用語解説
1)グルタミン代謝
グルタミンは、アミノ酸の一種で、急速に増殖する細胞において重要な代謝燃料です。老化細胞、癌細胞などは増加したエネルギー需要を満たすためにグルタミン代謝の亢進が見られることがあります。
2)GLS1
グルタミナーゼ1の略称。アミドヒドラーゼ酵素の一種で、グルタミンからグルタミン酸、およびアンモニアを産生します。
3) 日本核医学会PET薬剤製造基準
欧米とのハーモナイゼーション、治験や研究のグローバル化、新たな臨床研究指針の制定等、個々の PET 施設における説明責任の重要性がますます高まる中で、常に一定の品質を保証できる信頼性の高い PET 薬剤の製造を実現させ、新しいPET 薬剤の臨床展開を促進するため、日本核医学会が定めたPET 薬剤製造基準です。
掲載論文
タイトル: L-[5-11C]glutamine PET imaging noninvasively tracks dynamic responses of glutaminolysis in non-alcoholic steatohepatitis
著者: Zhang Y1, Xie L1, Fujinaga M1, Kurihara Y1,2, Ogawa M1,2, Kumata K1, Mori W1, Kokufuta T1, Nengaki N1, Wakizaka H1, Luo R1,3, Wang F3, Hu K4, Zhang MR1
著者所属:
1; Department of Advanced Nuclear Medicine Sciences, Institute for Quantum Medical Science, National Institutes for Quantum Science and Technology, Chiba 263-8555, Japan
2; SHI Accelerator Service, Ltd, Tokyo 141-0031, Japan
3; Department of Nuclear Medicine, Nanjing First Hospital, Nanjing Medical University, Nanjing12 210006, China
4; State Key Laboratory of Bioactive Substance and Function of Natural Medicines, Institute of Materia Medica, Chinese Academy of Medical Sciences & Peking Union Medical College, Beijing 100050, China
雑誌名: Acta Pharmaceutica Sinica B, 2024.
DOI: https://doi.org/10.1016/j.apsb.2024.07.023