2022-10-21 理化学研究所,北海道大学,大阪大学
理化学研究所生命機能科学研究センターナノバイオプローブ研究チームの神隆チームリーダー、坪井節子テクニカルスタッフ、北海道大学大学院先端生命科学研究院化学生物学研究室の門出健次教授、村井勇太助教、マハデバ M. M. スワミー助教、大阪大学大学院医学系研究科中性脂肪学共同研究講座の平野賢一特任教授(常勤)らの共同研究グループは、心筋における脂肪酸代謝[1]を光で可視化するための近赤外蛍光[2]プローブの開発に成功しました。
本研究成果は、心筋における脂肪酸代謝を、放射線を使わずに非侵襲的にイメージングする手法として、心臓疾患の研究に貢献するものと期待できます。
脂肪酸は心筋のエネルギー源であり、その代謝状況は心臓の状態を反映します。従来医療現場では、心臓の診断に放射性プローブ123I-BMIPP[3]による心筋脂肪酸代謝のシンチグラフィー[4]が用いられています。
今回、共同研究グループは、体を透過する近赤外蛍光を用いた心筋脂肪酸代謝の生体蛍光イメージング[5]を実現するため、BMIPPの放射性ヨウ素の代わりに近赤外蛍光色素Alexa680[6]で修飾した近赤外蛍光プローブ「Alexa680-BMPP」を開発しました。この化合物が発する近赤外蛍光の観測により、ヒト心筋培養細胞およびマウス個体において心筋での脂肪酸代謝が可視化できることを確認しました。
本研究は、科学雑誌『Analyst』の表紙に採用され、10月7日に掲載されました。
近赤外蛍光プローブAlexa680-BMPPを用いた心筋における脂肪酸代謝の生体イメージング
背景
心臓に生じた障害は生命の危機に直結するため、心臓機能の状態を正確に把握することが臨床では非常に重要です。正常な心臓の筋肉(心筋)はエネルギー源として主に脂肪酸(長鎖脂肪酸[7])を利用していますが、虚血状態(血液が十分に供給されない状態)の心筋は脂肪酸に代わってブドウ糖を利用するようになります。従って、心筋における長鎖脂肪酸代謝を非侵襲的にイメージングすることは、心臓機能の評価に不可欠であり、健康あるいは病気の心臓の状態の理解につながります。
心筋における長鎖脂肪酸代謝を非侵襲的にイメージングする手法として、放射性ヨウ素(123I)で標識したヨードフェニル-ペンタデカン酸などの長鎖脂肪酸類似体(123I-BMIPP)を利用したSPECT(単一光子放出コンピュータ断層撮影)[8]が広く使用されています。SPECTは高感度な心筋代謝イメージングを可能にしますが、放射線を検出し画像化するための大掛かりな診断機器や、放射性物質による標識合成が必要であるなど、コスト面などで課題があります。
一方、放射線を用いない非侵襲イメージング法として、赤っぽい光が体を通りやすいことを利用し、可視光の赤い光よりも波長の長い波長700~900ナノメートル(nm、1nmは10億分の1メートル)の近赤外光を用いるイメージングがあります。本研究では、長鎖脂肪酸に近赤外蛍光を発する色素を結合させて、心筋における脂肪酸代謝の近赤外生体蛍光イメージング技術の開発を試みました。
研究手法と成果
近赤外蛍光を発する長鎖脂肪酸を設計するにあたっては、心筋代謝イメージングのためのSPECTプローブとして利用されているBMIPPを基本骨格としました(図1a、b)。近赤外蛍光標識には、波長700nm以上で蛍光発光するAlexa680蛍光色素を用いました。この2種の分子を材料として、放射性ヨウ素の代わりにAlexa680を持つ近赤外蛍光を発する長鎖脂肪酸「Alexa680-BMPP」を合成しました。分岐した長鎖脂肪酸であるBMIPPは、β酸化[1]が阻害されるため代謝されにくく、心筋に長くとどまる性質があります。従って、BMIPPを基本骨格とする近赤外蛍光標識Alexa680-BMPPも、BMIPP同様に心筋において脂肪酸代謝のイメージングに利用可能なものと期待されます。またAlexa680-BMPPは出発化合物BMIPPから3ステップで合成でき、製造も簡単です(図1c)。
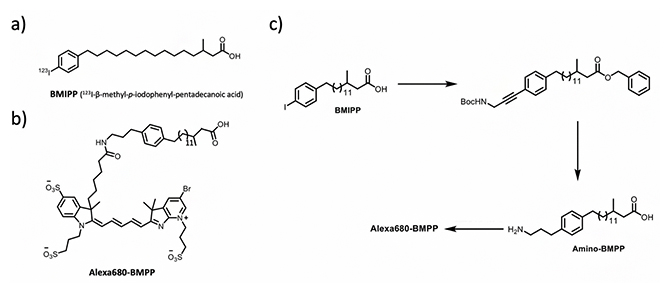
図1 SPECTプローブ123I-BMIPPと近赤外蛍光プローブAlexa680-BMPP
(a)現在使用されている123I-BMIPの分子構造。
(b)今回、開発したAlexa680-BMPPの分子構造。
(c)123I-BMIPPを出発物質とした、3ステップによるAlexa680-BMPPの合成法。
開発したAlexa680-BMPPの分子量は1231で、分子構造は高分解能質量分析[9]、アガロースゲル電気泳動[10]および蛍光スペクトルの測定から確認できました(図2a、b)。蛍光の最大ピークは近赤外波長領域にあり、当てた光(励起光)のエネルギーが蛍光のエネルギーに使われる変換効率(量子収率)は39%でした。これは、一般的な近赤外蛍光色素であるインドシアニングリーンの量子収率が1%程度であるのに比べて、高い蛍光輝度を示しています。
Alexa680-BMPPが長鎖脂肪酸として機能するかどうかを確認するため、培養下でのヒト心筋細胞への取り込みを調べました。その結果、Alexa680-BMPPは、コントロールの色素(脂肪酸と結合していないAlexa680)に比べ有意に心筋細胞に取り込まれることが分かりました(図2c)。このことから、Alexa680-BMPPが蛍光性の長鎖脂肪酸として機能することが明らかになりました。
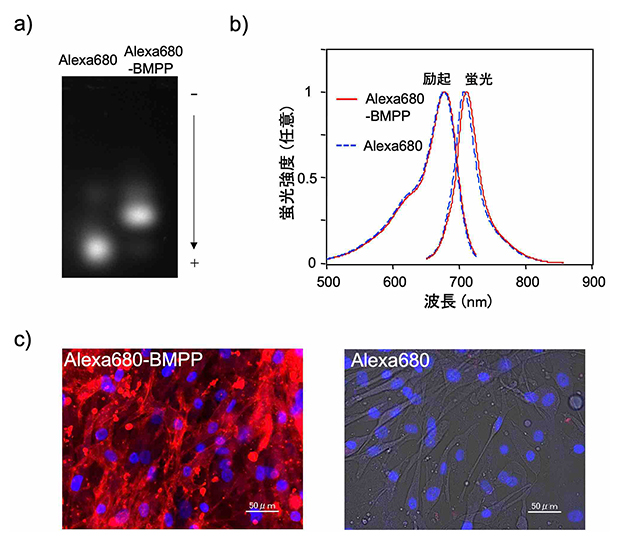
図2 蛍光性の長鎖脂肪酸として機能するAlexa680-BMPP
(a)Alexa680-BMPPとAlexa680(コントロール色素)のアガロースゲル電気泳動。分子量の大きいAlexa680-BMPPは泳動が遅い。
(b)Alexa680-BMPPとAlexa680はほぼ同じ蛍光スペクトルを示し、蛍光の最大ピークは近赤外波長領域にある。
(c)Alexa680-BMPPとAlexa680のヒト心筋細胞への取り込みの違いを示した細胞の蛍光画像。赤の蛍光が細胞に取り込まれたAlexa680-BMPPを、青の蛍光は細胞核を示している。右の画像のように、Alexa680はヒト心筋細胞には取り込まれない。
次に、生きたマウスの心筋で脂肪酸代謝が蛍光イメージングできるかどうかを確かめるため、ヘアレスマウス[11](4週齢、Hos:HR-1)にAlexa680-BMPPを尾静脈から注入し、近赤外蛍光を観測しました(図3a)。マウスの心臓部位の近赤外蛍光強度はAlexa680-BMPP注入後30分で最大に達し、時間とともにその蛍光強度は徐々に減少しました(図3b、c)。コントロールとして同量のAlexa680を尾静脈投与しましたが、蛍光はほとんど観測されませんでした(図3b、c)。また、蛍光色素注入後に切除した心臓組織の蛍光イメージング画像からは、Alexa680-BMPPがAlexa680に比べ5~6倍量心臓に取り込まれていることが分かりました(図3d)。これらの実験結果は、Alexa680-BMPPが蛍光性の長鎖脂肪酸として機能し、マウス心筋に取り込まれたことを示しています。
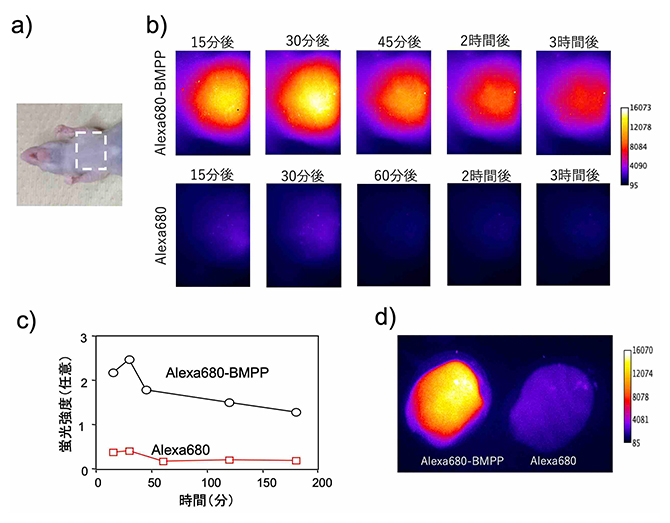
図3 Alexa680-BMPPを用いたヘアレスマウスの心筋脂肪酸代謝イメージング
(a)ヘアレスマウスの明視野画像。点線四角部分は蛍光を観測した胸部領域を示す。
(b)Alexa680-BMPPとAlexa680それぞれをヘアレスマウスに尾静脈から注入後に撮影した近赤外蛍光画像。マウスの心臓部位の近赤外蛍光強度はAlexa680-BMPP注入後30分で最大に達し、時間とともにその蛍光強度は徐々に減少した。
(c)(b)で撮影した蛍光画像の蛍光強度の時間変化を表したグラフ。
(d)Alexa680-BMPPとAlexa680をヘアレスマウスに注入してから30分後に切除した心臓組織の近赤外蛍光画像。
次に、Alexa680-BMPPの心筋への取り込みが、心筋の生理状態によって変化するか調べました。マウスを長期間絶食させると、心臓への脂肪酸の取り込みが増強されることが一般的に知られています。そこで、24時間絶食させたマウスと、比較のため通常の飼料で飼育したマウスの心臓組織の近赤外蛍光イメージングを行いました。その結果、生体蛍光イメージング(図4a、b)、および分離切除した心臓の蛍光画像(図4c、d)のいずれにおいても、Alexa680-BMPPの心臓への取り込みは、絶食させたマウスの方が給餌されたマウスよりも有意に大きいことが観測されました。以上の結果から、蛍光性の長鎖脂肪酸であるAlexa680-BMPPは心筋の生理的状態を観測できる蛍光プローブとして機能するが示されました。
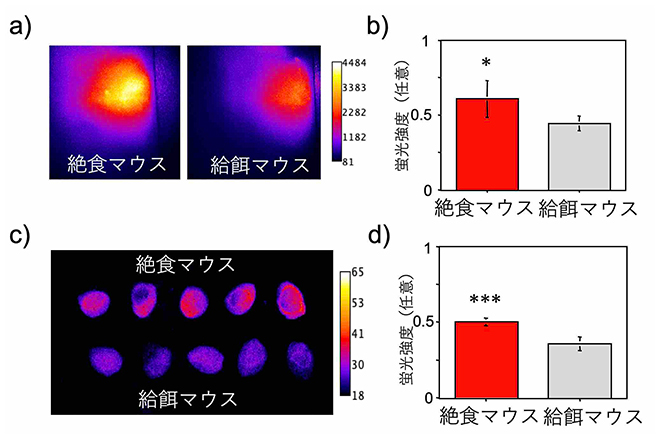
図4 心筋の生理的状態を反映するAlexa680-BMPPの蛍光強度
(a)24時間絶食および給餌マウスの心臓領域の近赤外生体蛍光イメージング。画像は、Alexa680-BMPPを静脈内投与30分後に撮影した。
(b)絶食および給餌マウス(各5匹ずつ)の心臓領域の蛍光強度。絶食マウスの蛍光強度は給餌マウスに比べて有意に高い(*p<0.05、n=5)。
(c)24時間絶食および給餌マウス(各5匹ずつ)から切除した心臓組織の近赤外蛍光画像。画像はAlexa680-BMPPを静脈内投与30分後に撮影した。
(d)絶食および給餌マウスの切除した心臓組織の蛍光強度。絶食マウスの蛍光強度は給餌マウスに比べて有意に高い(*p<0.001、n=5)。
今後の期待
これまで、心筋の脂肪酸代謝を非侵襲的に計測するための蛍光性の長鎖脂肪酸は開発されていませんでした。今回、世界に先駆けて合成に成功した近赤外蛍光を発する長鎖脂肪酸(Alexa680-BMPP)は、心筋における脂肪酸代謝の蛍光イメージングを可能にします。これにより、SPECTなどの放射線イメージングでしか検査できなかった心筋の脂肪酸代謝を、より簡便に画像化できるようになります。この近赤外蛍光を用いた心筋イメージング技術は、さまざまな心臓疾患研究への応用が期待できます。
補足説明
1.脂肪酸代謝、β酸化
心筋はエネルギー源として、主に脂肪酸とブドウ糖を利用している。酸素供給の良い健常心筋では、空腹時にエネルギー源の約80%は脂肪酸のβ酸化が用いられる。β酸化は、脂肪酸からアセチルCoAを生成する代謝反応。
2.近赤外蛍光
近赤外とは可視よりも波長の長い領域で、波長700~900nmの光を指す。近赤外蛍光とは、近赤外の蛍光である。
3.123I-BMIPP
βの位置にメチル基のついた側鎖脂肪酸。放射性同位体ヨウ素で標識することで心筋脂肪酸代謝を画像化する、心筋シンチグラフィーの放射性造影剤として用いられる。123I-BMIPPは123I-β-methyl-P-iodophenyl-pentadecanoic acidの略。
4.シンチグラフィー
放射性医薬品を静脈注射やカプセルで飲み、体内に取り込まれた部分から放出されるガンマ線を専用の装置で体外から計測することで、薬の分布を画像化する検査方法。
5.生体蛍光イメージング
生体内部を非侵襲で可視化する技術。これまで実用化している方法としては、X線CT(コンピュータトモグラフィー)、MRI(磁気共鳴断層撮影)、PET(陽電子放出断層撮影)などがある。蛍光を利用した生体イメージングでは、組織透過性が良い近赤外や短波赤外蛍光を利用して生体内部を可視化する。
6.Alexa680
シアニン系の蛍光色素。従来の蛍光色素よりも強い蛍光強度を示し,光安定性にも優れている。青から赤までの色調の種類があり,マルチカラー検出にも適する。核酸や抗体、タンパク質などの蛍光ラベルに汎用される。Alexa680の色素は、吸収極大を680nm付近に持ち、700nm以上の近赤外領域で蛍光発光する。
7.長鎖脂肪酸
脂肪酸とは、長鎖炭化水素の1価のカルボン酸であり、炭素数に応じて短鎖・中鎖・長鎖脂肪酸と区別される。長鎖脂肪酸は、炭素数が11~22の脂肪酸を指す。
8.SPECT(単一光子放出コンピュータ断層撮影)
シンチグラフィーの応用で、体内に投与した放射性同位体から放出されるガンマ線を検出し、その分布を断層画像にする手法。薬剤の投与は、主に静脈注射によって行われる。脳血流、骨、心筋などの断層画像の取得ができる。SPECTは、Single Photon Emission Computed Tomographyの略。
9.質量分析
分子をイオン化して、得られたイオンを高真空中で加速し、電場や磁場の中を移動させて、各イオン種の質量の違いにより分離・検出する分析。化合物の分子量、分子式などに関する情報を得ることができる。
10.アガロースゲル電気泳動
寒天の主成分であるアガロースを使用する電気泳動で、核酸、タンパク質、脂質などをその分子の大きさ、電荷などに応じて分離する方法である。
11.ヘアレスマウス
一般毛の形成・伸長がないため、脱毛の必要がなく、生体蛍光イメージングに適したマウスである。ヌードマウスとは異なり、免疫機能は正常である。
共同研究グループ
理化学研究所生命機能研究センターナノバイオプローブ研究チーム
チームリーダー神隆(ジン・タカシ)
テクニカルスタッフ坪井節子(ツボイ・セツコ)
北海道大学大学院先端生命科学研究院化学生物学研究室
教授門出健次(モンデ・ケンジ)
助教村井勇太(ムライ・ユウタ)
助教マハデバ M. M. スワミー(Mahadeva M. M. Swamy)
大阪大学大学院医学系研究科中性脂肪学共同研究講座
特任教授(常勤)平野賢一(ヒラノ・ケンイチ)
研究支援
本研究は、理化学研究所運営費交付金(生命機能科学研究)で実施し、日本学術振興会(JSPS)科学研究費助成金基盤研究(B)「「生体の第2光学窓」近赤外蛍光イメージング技術の開発(研究代表者:神隆)」「ヒト乳がんの光診断を目指した短波赤外蛍光分子イメージング技術の開発(研究代表者:神隆)」、同研究拠点形成事業「次世代ケミカルバイオロジーアジア拠点」、文部科学省北海道大学機能強化促進事業「フォトエキサイトニクス研究拠点」、日本医療研究開発機構(AMED)橋渡し研究戦略的推進プログラム(シーズA)「戦略的TR推進による自立循環型新規医療創出拠点の実現」における研究開発課題「中性脂肪蓄積心筋血管症(TGCV)に対する末梢血を使った診断機器の開発」の助成を受けて行われました。
原論文情報
Mahadeva M. M. Swamy, Mohamad Zarif Mohd Zubir, Mutmainah, Setsuko Tsuboi, Yuta Murai, Kenji Monde, Ken-ichi Hirano and Takashi Jin, “A near-infrared fluorescent long-chain fatty acid toward optical imaging of cardiac metabolism in living mice”, Analyst, 10.1039/d2an00999d
発表者
理化学研究所
生命機能科学研究センターナノバイオプローブ研究チーム
チームリーダー神隆(ジン・タカシ)
テクニカルスタッフ坪井節子(ツボイ・セツコ)
北海道大学大学院先端生命科学研究院化学生物学研究室
教授門出健次(モンデ・ケンジ)
助教村井勇太(ムライ・ユウタ)
助教マハデバ M. M. スワミー(Mahadeva M. M. Swamy)
大阪大学大学院医学系研究科中性脂肪学共同研究講座
特任教授(常勤)平野賢一(ヒラノ・ケンイチ)
報道担当
理化学研究所 広報室 報道担当
北海道大学社会共創部広報課広報・渉外担当
大阪大学大学院医学系研究科広報室