2023-03-24 京都大学iPS細胞研究所
ポイント
- ヒト気道オルガノイド注1)を用いたオートファジー注2)関連化合物スクリーニングの結果、シクロヘキシミドとタプシガルギンが新型コロナウイルス(SARS-CoV-2)注3)に対して強い抗ウイルス効果を示した。
- シクロヘキシミドは、多様なSARS-CoV-2変異株や他のヒトコロナウイルス(HCoV-229E注4)、HCoV-OC43注5))に対しても抗ウイルス効果を示した。
1. 要旨
橋本 里菜 研究員(CiRA増殖分化機構研究部門)、渡邉 幸夫 研究員(CiRA同部門)、高山 和雄 講師(CiRA同部門)らの研究チームは、ヒト気道オルガノイドを用いたオートファジー関連化合物スクリーニングを実施し、SARS-CoV-2に対してシクロヘキシミドとタプシガルギンが強い抗ウイルス効果を示すことを見出しました。また、シクロヘキシミドは、6種類のSARS-CoV-2変異株と他のヒトコロナウイルスにも効果があることを確認しました。
本研究では、まず、ヒト気道オルガノイドとオートファジー関連化合物ライブラリーを用いたスクリーニングを実施し、SARS-CoV-2の感染を制御できる化合物の同定を試みました。80化合物のうち、シクロヘキシミドとタプシガルギンは用量依存的に感染効率を低下させました。シクロヘキシミドは6種類の SARS-CoV-2変異株だけでなく、ヒトコロナウイルスであるHCoV-229EおよびHCoV-OC43の感染効率も低下させました。残念ながら、シクロヘキシミドはヒトに使用すると毒性を示す恐れがあるため、COVID-19治療薬としての応用は見込めません。しかし、今回の結果から、気道オルガノイドと化合物ライブラリーを用いた創薬スクリーニングは有用な手段であることが分かりました。今後は大規模なスクリーニングを行うことで、有望な薬の開発が期待されます。
この研究成果は2023年3月22日(米国時間)に「Molecular Pharmaceutics」でオンライン公開されました。
2. 研究の背景
新型コロナウイルス感染症(COVID-19)注6)治療薬の開発に向けて、大きく二つのアプローチがあります。ウイルスタンパク質を標的にする薬と感染に関与する宿主タンパク質を制御する薬です。次々と登場する変異株に対応するためには、宿主タンパク質を制御する薬が有効だと考えられています。本研究では、オートファジーに着目してCOVID-19治療薬の探索を試みました。
オートファジーはウイルスの排除を促進することもありますが、ウイルスがオートファゴソームを感染に必要な小胞として利用することもあります。オートファジーとSARS-CoV-2は密接に関係しているため、オートファジーを制御する化合物がCOVID-19治療薬候補となる可能性があります。
3. 研究結果
1)オートファジー関連化合物ライブラリーを用いたCOVID-19治療薬探索
オートファジー関連化合物ライブラリーがヒト気道オルガノイドにおけるSARS-CoV-2感染効率に影響を与えるかを調べました(図1A)。80化合物のうち14化合物は、化合物を作用していない群と比較して、細胞培養上清中のウイルスゲノム量を25%以下に低下させました(図1B)。14化合物のうち、6化合物(バルプロ酸ナトリウム、ペニトレムA、ニグルジピン、タプシガルギン、シクロヘキシミド、LY294002)を作用させた細胞生存率は50%以上でした(図1C)。同定した6化合物は、細胞毒性が少なく抗ウイルス効果が高い化合物であることが示唆されました。
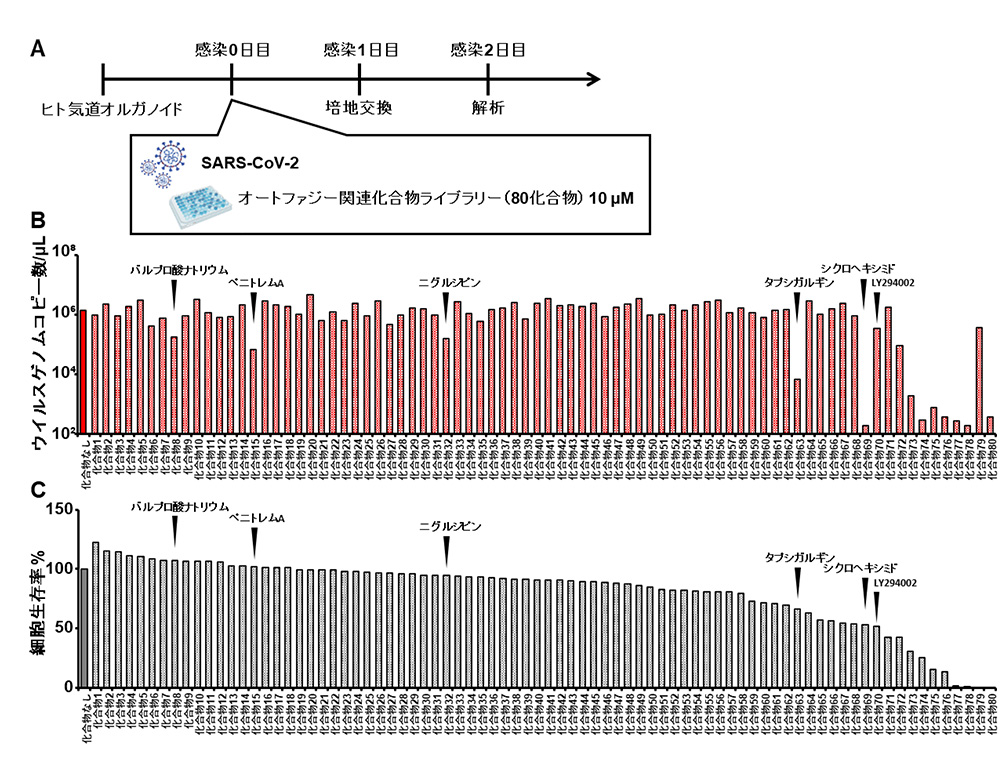
図1:ヒト気道オルガノイドとオートファジー関連化合物ライブラリーを用いたスクリーニング
(A) 感染実験の手順
(B) 80化合物作用による培養上清中のウイルスゲノム量への影響を評価
(C) 80化合物作用による細胞生存率への影響評価
75%以上の抗ウイルス効果と50%以上の細胞生存率の両方を示した6化合物の名称はグラフ内に記載。
2)SARS-CoV-2感染を用量依存的に阻害する化合物の同定
次に、ヒト気道オルガノイドにおいて6化合物が用量依存的な抗ウイルス効果を示すかを確認しました(図2)。6化合物(10 μMあるいはそれ以下)を作用しても、細胞生存率は50%以上に維持されました。6化合物のうち、シクロヘキシミドとタプシガルギンを作用することによって、ヒト気道オルガノイドの上清中のウイルスゲノム量が化合物の用量依存的に減少しました。したがって、シクロヘキシミドとタプシガルギンは有望なCOVID-19治療薬候補として期待されます。
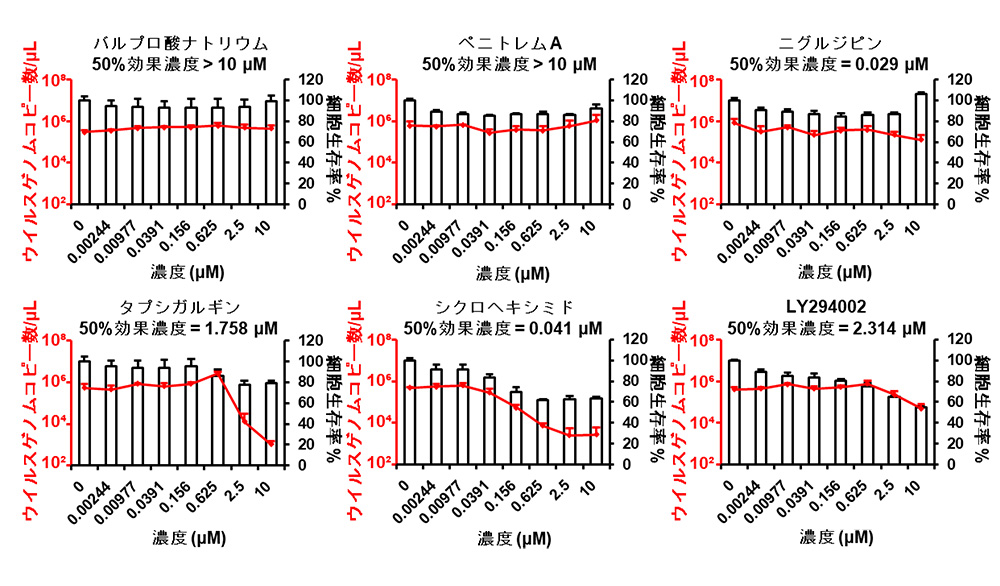
図2:6化合物を用いた二次スクリーニング
ヒト気道オルガノイドに6化合物を各濃度で作用させたときの培養上清中のウイルスゲノム量および細胞生存率への影響を評価。ウイルスゲノム量を50%に減少させたときの各化合物の作用濃度はグラフ内に記載。
3)シクロヘキシミドとタプシガルギンの抗ウイルス効果の評価
シクロヘキシミドとタプシガルギンの抗ウイルス効果をさらに検討しました。SARS-CoV-2に感染した気道オルガノイドにシクロヘキシミドあるいはタプシガルギンを作用させました。シクロヘキシミドおよびタプシガルギン作用によって、培養上清中のウイルスゲノム量(図3A)およびSARS-CoV-2 ヌクレオカプシド(N)注7)遺伝子発現量(図3B)が有意に減少しました。また、SARS-CoV-2 Nタンパク質の発現量が減少することも確認できました(図3C)。
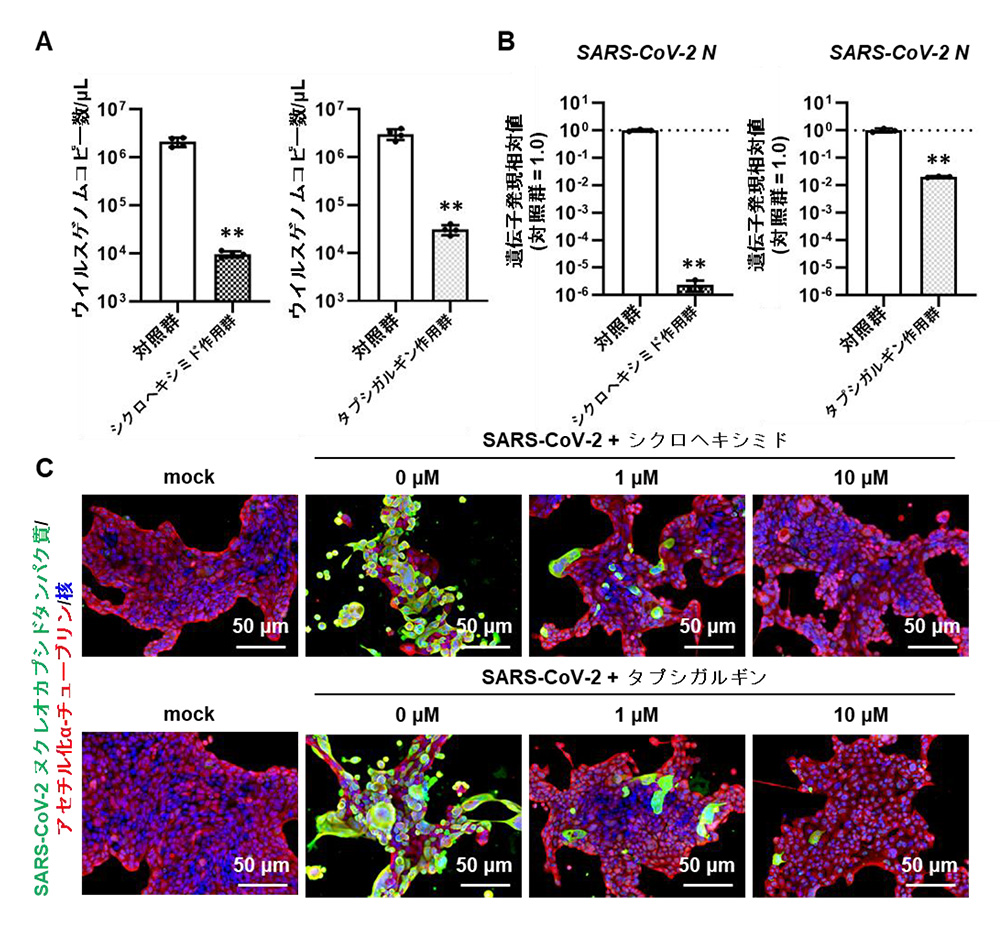
図3:シクロヘキシミドとタプシガルギンのSARS-CoV-2に対する抗ウイルス効果
シクロヘキシミドあるいはタプシガルギン作用時における
(A) 培養上清中のウイルスゲノムゲノム量
(B) 細胞内のSARS-CoV-2 N遺伝子発現量
(C) SARS-CoV-2 Nタンパク質発現量
**:p <0.01の有意差を示す。
4)シクロヘキシミドのSARS-CoV-2変異株および他のヒトコロナウイルスへの有効性評価
シクロヘキシミドはタプシガルギンよりも強い抗ウイルス効果が確認されたため、シクロヘキシミドに関してより詳細な検討を行うことにしました。シクロヘキシミドがSARS-CoV-2変異株および他のヒトコロナウイルスの感染効率を低下させるかを調べました。
シクロヘキシミドは、気道オルガノイドにおいて6 種類のSARS-CoV-2変異株(B.1.1.214、B.1.617.2、BA.1、BA.2、BA.2.3、BA.5注8))の感染効率を低下させました(図4A)。また、シクロヘキシミドは、iPS細胞由来肺オルガノイド注9)において他のヒトコロナウイルス(HCoV-229EとHCoV-OC43)の感染効率も低下させました(図4B)。以上のことから、シクロヘキシミドは、さまざまな SARS-CoV-2変異株およびヒトコロナウイルスに対して有効な治療薬候補であると考えられます。
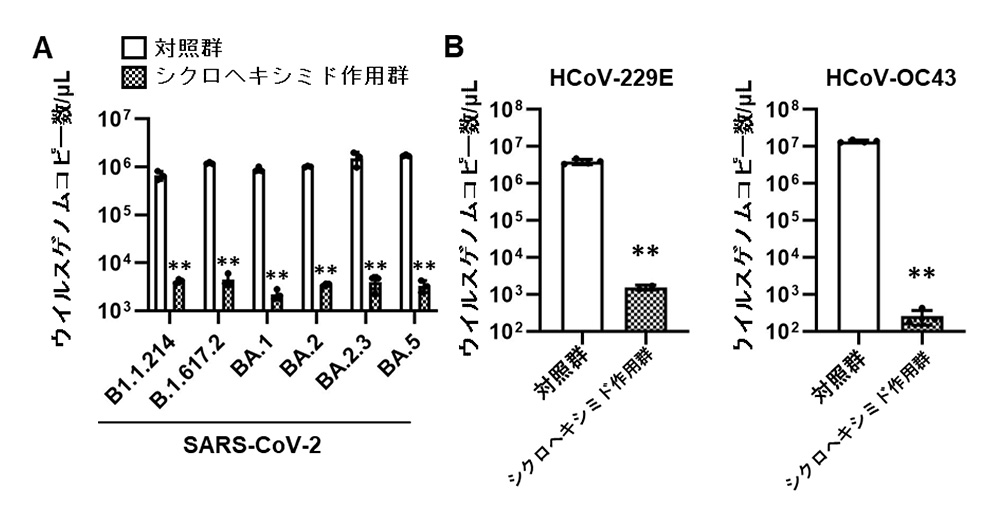
図4:シクロヘキシミドの各種SARS-CoV-2変異株およびヒトコロナウイルスに対する抗ウイルス効果
(A) シクロヘキシミド作用時における6種類のSARS-CoV-2変異株のウイルスゲノムコピー数の減少
(B) シクロヘキシミド作用時におけるヒトコロナウイルス(HCoV-229E, HCoV-OC43)のウイルスゲノムコピー数の減少
**:p <0.01の有意差を示す。
4. まとめと展望
本研究では、ヒト気道オルガノイドとオートファジー関連化合物ライブラリー(80化合物)を用いたスクリーニングを実施し、SARS-CoV-2感染を抑制する化合物としてシクロヘキシミドとタプシガルギンを同定しました。シクロヘキシミドは、6種類のSARS-CoV-2の変異株と、HCoV-229EおよびHCoV-OC43に対する抗ウイルス効果を示すことを見出しました。一方で、シクロヘキシミドはタンパク質合成阻害剤としての働きがあるために、動物実験で使用すると強い毒性が生じることも確認しています。今後、抗ウイルス効果を保持したまま、毒性を低減したシクロヘキシミド誘導体あるいは類縁化合物を開発できれば、有望な薬になると期待されます。今回、気道オルガノイドと化合物ライブラリーを用いた創薬スクリーニングは有用な手段であると示すことができたため、さまざまな化合物ライブラリーと組み合わせることで、より大規模なCOVID-19治療薬探索に役立つことを期待します。
5. 論文名と著者
- 論文名
Evaluation of broad anti-coronavirus activity of autophagy-related compounds using human airway organoids - ジャーナル名
Molecular Pharmaceutics - 著者
Rina Hashimoto1*, Tomokazu Tamura2*, Yukio Watanabe1*, Ayaka Sakamoto1, Naoko Yasuhara1, Hayato Ito2, Masahiro Nakano3,4, Hiromitsu Fuse1, Akira Ohta1, Takeshi Noda3,4, Yasufumi Matsumura5, Miki Nagao5, Takuya Yamamoto1,6,7, Takasuke Fukuhara2,8,9**, Kazuo Takayama1,9**
*筆頭著者 **責任著者 - 著者の所属機関
- 京都大学iPS細胞研究所(CiRA)
- 北海道大学大学院医学研究院微生物部門免疫学分野
- 京都大学医生物学研究所微細構造ウイルス学分野
- 京都大学大学院生命科学研究科微細構造ウイルス学分野
- 京都大学大学院医学研究科臨床病態検査学
- 理化学研究所革新知能統合研究センター iPS細胞連携医学的リスク回避チーム
- 京都大学高等研究院ヒト生物学高等研究拠点(WPI-ASHBi)
- 大阪大学微生物病研究所
- 日本医療研究開発機構革新的先端研究開発支援事業(AMED-CREST)
6. 本研究への支援
本研究は、下記機関より支援を受けて実施されました。
- 京都大学基金 iPS細胞研究基金
- 京都大学iPS細胞研究所山中伸弥研究室への新型コロナウイルス特別研究助成
- 公益財団法人 三菱財団
- 京都大学 ウイルス感染症・生命科学先端融合的共同研究拠点
- 日本学術振興会 科学研究費助成事業 基盤研究B
- 国立研究開発法人日本医療研究開発機構
(JP20fk0108533, JP21fk0108492, JP21gm1610005, JP21fk0108493, JP22fk0108617)
7. 用語説明
注1)気道オルガノイド
線毛細胞、クラブ細胞、ゴブレット細胞、神経内分泌細胞からなる気道様三次元構造体。SARS-CoV-2感染実験に使用することができ、感染細胞の特定、宿主細胞における応答、治療薬の評価などに利用できる。
注2)オートファジー
病原体や不要なタンパク質などをオートファゴソームという小胞に取り込み、分解・排除する細胞の機能。
注3)SARS-CoV-2
新型コロナウイルス(severe acute respiratory syndrome coronavirus 2)。新型コロナウイルス感染症(COVID-19)の原因ウイルス。さまざまな変異型が存在することが知られている。
注4)HCoV-229E
ヒトコロナウイルス(Human coronavirus)の一種。風邪の原因となるウイルス。
注5)HCoV-OC43
ヒトコロナウイルス(Human coronavirus)の一種。風邪の原因となるウイルス。
注6)新型コロナウイルス感染症(COVID-19)
新型コロナウイルス感染症の正式名称。CO=「corona」、VI=「virus」、D=「disease」。
注7)SARS-CoV-2ヌクレオカプシド(N)
SARS-CoV-2に最も多く存在するタンパク質であり、ウイルスの中身に存在する。
注8)B.1.1.214、B.1.617.2、BA.1、BA.2、BA.2.3、BA.5
SARS-CoV-2変異株の一種。B.1.1.214は2020年秋以降の第三波で確認された変異株。B.1.617.2は2021年夏に流行した変異株。B.1.617.2はデルタ株とも呼ばれる。BA.1、BA.2、BA2.3、BA.5は2021年末以降に流行した変異株。BA.1、BA.2、BA2.3、BA.5はオミクロン株とも呼ばれる。
注9)iPS細胞由来ヒト肺オルガノイド
iPS細胞より分化誘導した肺オルガノイド。気道と肺胞どちらの特徴も保有する。