2023-08-09 基礎生物学研究所
近年、生物組織内のメカニカルな力は、形態形成や細胞分化を駆動する上で重要な情報であることが分かってきました。しかし、生きた組織内で力を計測する手段は限られています。特に、3次元的な胚や組織の発生では、細胞の力の状態は時空間的に変化するため定量的な理解は十分にはされていません。したがって、形態形成やその数理シミュレーションにおいて、力の値に関する根拠が希薄であるという生命科学に特有の問題がありました。本研究では、分子動力学シミュレーションの分野で発展してきた粒子間の力(ポテンシャルエネルギー)を推定する方法から着想を得て、非平衡系である生物組織にも適用できる手法を検討し、顕微鏡観察等で得られる細胞の動きの画像情報から、生物組織内のメカニカルな力を推定する手法を開発しました。
本方法により、生きた組織内で細胞種によるメカニカルな性質の差異を定量的に評価することが可能となりました。さらに、本方法の実施に必要なデータが細胞核の追跡データのみという単純さゆえ、様々な生物種や組織に適用することが可能です。今後、固有の物理的性質をもった細胞の探索などへの発展性が期待できます。また、細胞を粒子として近似するモデルは、その実装や計算コストから大きな組織や臓器の数理シミュレーションに向いており、今回の研究はその基礎となるパラメータ値を取得する手段を与えます。
本研究は、基礎生物学研究所の小山宏史助教を中心として、同藤森俊彦教授、分子科学研究所/生命創成探究センターの奥村久士准教授、核融合科学研究所の伊藤篤史准教授、明治大学総合数理学部の中村和幸教授、生理学研究所の大谷哲久助教、生命創成探究センター/基礎生物学研究所の加藤輝特任助教との共同で行われ、2023年8月7日にPLOS Computational Biology誌に掲載されました。
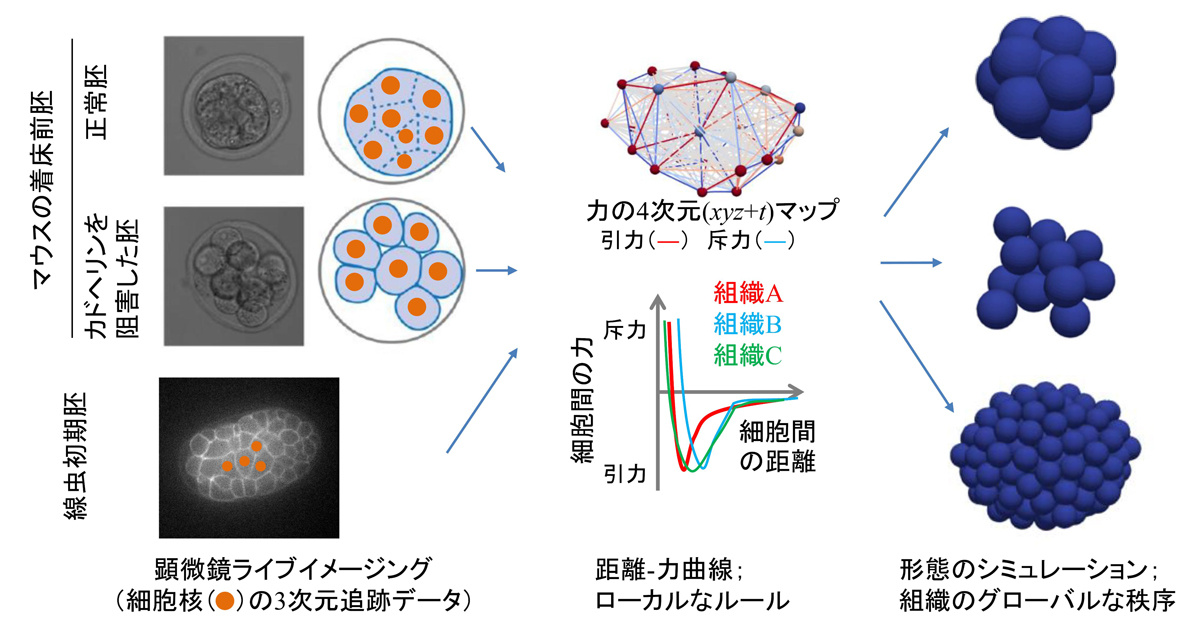
本研究の概念図
研究成果のポイント
- 多細胞組織において、共焦点顕微鏡などで得られた細胞の追跡データから細胞間の相互作用の力を推定する統計数理学的な方法を開発した。
- 3次元組織内の力の状態を、個々の細胞レベルの空間解像度と顕微鏡ライブイメージングの時間解像度で計測が可能となった。
- マウスや線虫の胚の割球では、細胞間の力は距離に依存した関数(距離-力曲線)という単純な法則で近似できた。
- マウスや線虫の胚の形態的な差異が、細胞間の力の相違とリンクして説明できることを示した。
【研究の背景】
多細胞生物では、個体、臓器、組織、胚に至るまで多様な形態を示し、その形態が生理的な機能と密接に関係している事例が多く知られています。ある形態をとるにはメカニカルな力が必ず関与しており、その力の源泉は主に細胞にあります。また、組織内の力の状態は細胞分化とも密接関係していることが知られています。このため、組織内の各細胞の力の状態を知ることは、形態形成や細胞分化を研究する上で基盤となる情報となります。
組織における力を計測する方法として、組織を破壊するなどの措置を伴う侵襲的なものがあります。しかし、胚や組織の発生では、細胞の力の状態は時間的に変化し、かつ、細胞種によってメカニカルな性質が異なるため、侵襲的な方法では全容が全くつかめませんでした。一方、非侵襲的な方法として、顕微鏡画像から力を統計数理学的に推定するという方法が研究されてきました。これに分類される方法には、力の単位は得られないという弱点がある一方で、時空間解像度の高い情報が得られるため、組織の全容や個別の細胞の情報を取得できるという長所があります。しかし、3次元組織の場合において、画像から力を推定する方法はこれまで提案されておらず、本研究ではこの問題の解決を目指しました。
また、技術開発を通して以下の生物学的な問題に取り組みました。先述した通り組織の力の源泉は細胞にあります。では、細胞の力というローカルな情報が、組織全体の形態というグローバルな秩序を決定する上でどの程度の寄与を果たしているのでしょうか?すなわち、細胞の力の性質と組織の形態が直接リンクしうるのかを本研究で検証しました。
【研究の成果】
1. 細胞間の相互作用の力の推定法の開発
画像から力を推定する方法では、何らかの理論モデルを仮定する必要があります。つまり、画像データに対して理論モデルをフィッティングすることでモデル中のパラメータ値を推定します。このように観測データに対して理論モデルを当てはめる手法は、天気予報などで用いられるデータ同化と呼ばれる統計数理学の分野で発展してきました。多細胞の理論モデルとしては、細胞の形態まで考慮した解像度の高いモデルが複数あります。しかし、モデルの解像度にフィットする観測データを取得することは、顕微鏡技術とそれに続く画像処理の問題で3次元組織では容易でないという現状があります。そこで本研究では、モデルと観測データの解像度をあえて低く抑えることで、両者をフィットさせる手段をとりました。すなわち、細胞を粒子として粗視化したモデルと、細胞の核の座標のみを考慮しました(図1左図)。細胞核の3次元情報は、様々な組織や生物種で続々と公開されており、比較的容易に取得できる情報とされています。
一方、粒子モデルを観測データにフィッティングさせるという手段は、原子・分子・プラズマ・コロイド科学の分野で発展しており、推定された粒子間の力・ポテンシャルエネルギーの値は分子動力学シミュレーションのパラメータ値として用いられます。これらの分野では、系が平衡状態にあるなどの前提のもとで推定法が構築されています。しかし、胚発生期などでは非平衡状態にあるなど前提が異なるため新たな方法の開発が必要でした。詳細は省きますが、正解が分かっている人工データに対して(ある種の教師ありデータ)、ベイズ推定の考えを取り入れた最適化問題を解くことで正しい力を推定できる方法を開発しました。
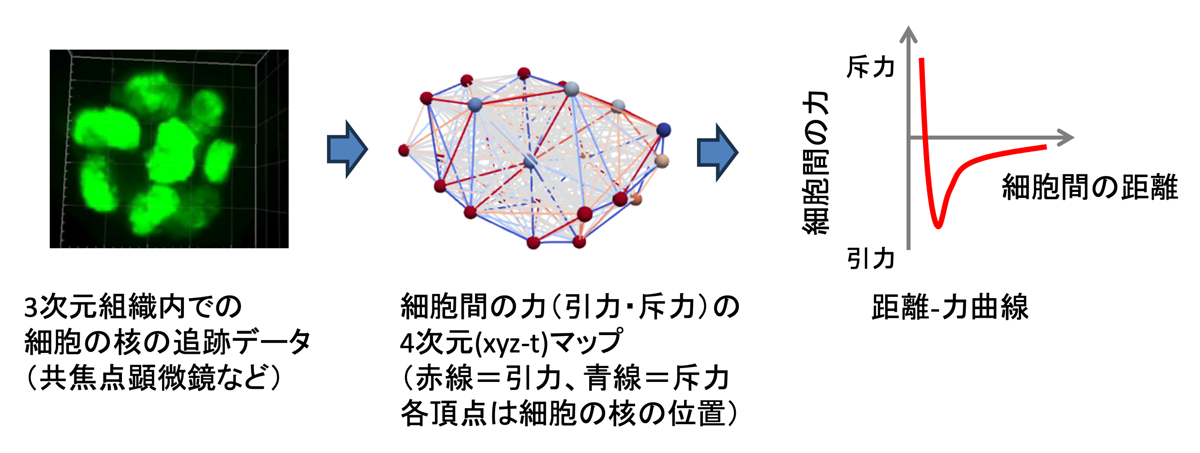 図1:細胞間の力の推定の概要
図1:細胞間の力の推定の概要
左図は、細胞核の共焦点顕微鏡画像の例です。細胞核を、ヒストンに緑色蛍光タンパク質を融合させたタンパク質を発現させることで可視化しました。中央の図では、細胞間の力の4次元マップの例で、線虫胚での推定結果を示しています。この図では一つのタイムポイントのスナップショットを示しています。右図では、細胞間の力の推定値を細胞間の距離に対してプロットして算出した距離-力曲線のイメージ図を示しています。
2. 実組織での力の推定
次に、開発した方法を実際の組織に適用しました。線虫の初期胚発生では、細胞核の追跡データが4細胞期から約350細胞期まで公開されています。このデータに対して本方法を適用することで、各細胞間の力(引力・斥力)の時系列変化を推定することに成功しました(図1中央図)。同様に、マウスの着床前胚に関して独自に細胞核の追跡データを取得し、各細胞間の力の時系列変化を推定しました。
上記で得られたデータは組織内の力の時空間分布という非常に膨大な情報を含有しているため、一見しただけでは有益な知識を簡単に発見することはできません。そこで、さらなる解析をすることで、細胞間の力が何らかの明確な法則に則って決定づけられているかを検証しました。一つの仮説が、細胞間の引力・斥力は、細胞間の距離の関数で表されるのではないかというものです。背景として、数理・理論研究の分野では、細胞間の距離に依存した引力・斥力を仮定した数理モデルが知られています(2体間の距離―力曲線、あるいは、2体間ポテンシャルエネルギーと言う)。この細胞の粒子モデルは、割球、上皮細胞、間質細胞など様々な細胞種への適用事例があります。しかし、現実の細胞は球形の粒子とはかけ離れた形態を示すこともしばしばあるので、細胞間の力を距離の関数で表すことに妥当性があるのかは、組織における実計測事例が存在しないため不明でした。
線虫およびマウス胚で推定された力の値を細胞間の距離に対してプロットしたところ、力の値が距離の関数として現れました(図1右図)。すなわち、距離が近い場合には斥力、より遠い場合には引力というプロファイルを示しました。近いときには細胞の体積等の効果により反発するため斥力となることは物理学的に合理的でした(図2)。さらに、より遠い場合には細胞間の接着力により近づこうとするので引力となるのも合理的でした(図2)。以上の結果は、現実の組織における細胞間の距離-力曲線に関する初めての実験的な計測事例です。
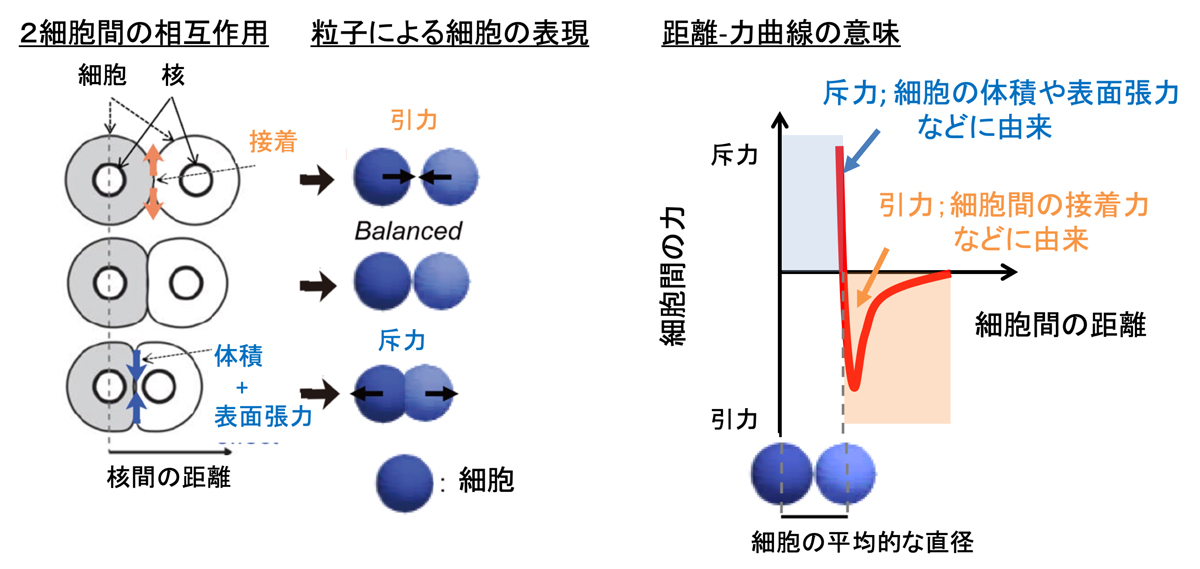 図2:細胞間の引力・斥力の意味
図2:細胞間の引力・斥力の意味
細胞間の引力・斥力は、細胞間の接着力、細胞の体積による排除効果などより微視的な要素の総和として現れると考えられています。細胞の核間の距離が近くなりすぎると体積の効果によって斥力が生じて遠ざかろうとし、ある程度距離が離れると細胞間の接着力により引力が生じて近づこうとすると予想されます。引力と斥力が釣り合う距離が細胞の平均的な直径とほぼ一致します。
3. 細胞間の力の定量的な差異と組織の形態とのリンク
上記のように、線虫やマウスの胚において細胞間の力が距離-力曲線として検出されることがわかりました。では、この曲線のプロファイルにどのような意味があるのでしょうか?組織の形態とリンクしている可能性を検証するために、推定された距離-力曲線に基づいた数理シミュレーションを実施しました。その結果、線虫胚から得られた距離-力曲線からは、実際の線虫胚で観察される楕円球型の組織が、マウスの桑実胚から得られた距離-力曲線からは、実際の桑実胚のような球型の組織が、それぞれ出現しやすいことが分かりました(図3)。つまり、細胞間の相互作用の力というローカルな法則が、組織全体の形態というグローバルな形態を決めるのに十分な情報を持っていることを示しています。
この考えをさらに検証するために攪乱実験を行いました。マウスの桑実胚のある時期には、カドヘリン等の細胞間接着分子の効果によって細胞同士が強固に密着し、球型になることが知られています。そこで、カドヘリンやアクトミオシンを薬剤で阻害することで、球型になれない胚を人為的に作成しました。正常な胚と薬剤で処理した胚のそれぞれから距離-力曲線を推定したところ、そのプロファイルに定量的な相違が検出されました(図3)。さらに、数理シミュレーションを実施したところ、薬剤処理した胚に由来する距離-力曲線からは、組織が球型になりにくいという結果が得られ、著者らの仮説を支持しました。また、距離-力曲線のプロファイルにおいて、形態の決定に重要な部分を同定することに成功しました。
以上から、①組織内での細胞間の相互作用の力は、細胞間の距離に応じた関数として表されること、②その関数の定量的な相違が組織の形態というグローバルな秩序を決定づけること、が明らかとなりました。
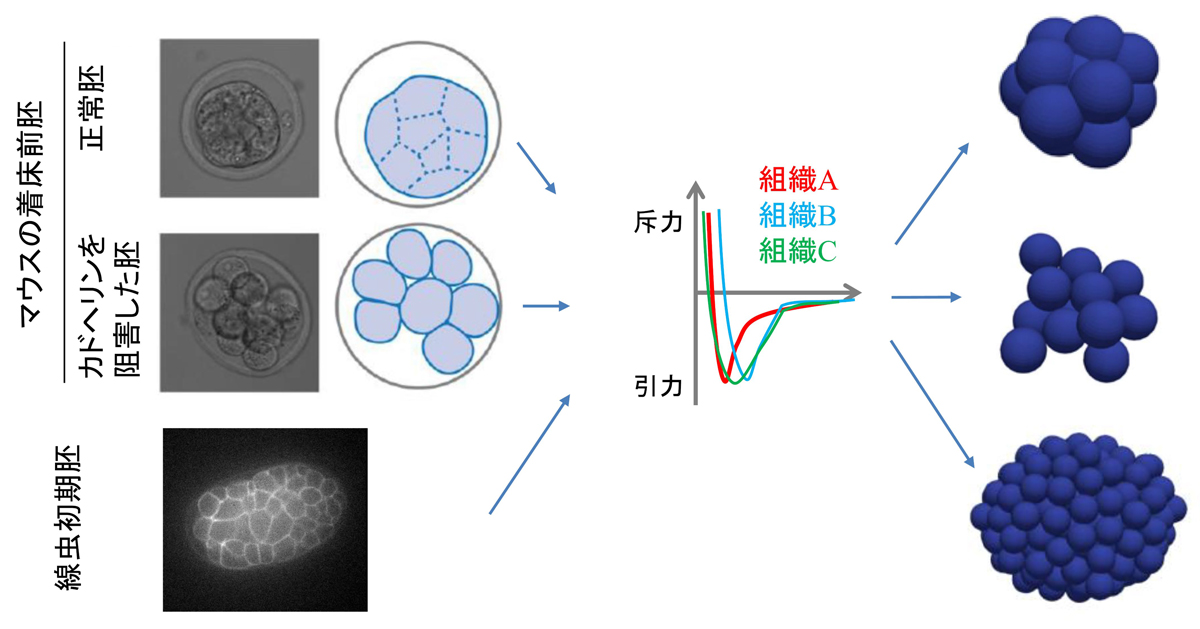 図3:距離-力曲線のプロファイルと組織の形態の関係
図3:距離-力曲線のプロファイルと組織の形態の関係
マウスの着床前胚について、正常胚とカドヘリンを阻害した胚の2種類の組織から距離-力曲線を推定しました。同様に、線虫初期胚でも推定しました。中央の距離-力曲線は模式図です。3種類の組織によって異なるプロファイルをもつ距離-力曲線が得られました。これらの距離-力曲線を使ってシミュレーションを実施した結果を右の列に示しています。上から、球型、いびつな形、卵型をそれぞれ示し、これらの形態は現実の組織の形態と類似していました。
【今後の展望】
近年、細胞や組織の力に基づいた数理シミュレーションが、発生や組織再生などの分野で実施されるようになりました。しかし、パラメータの値を実測するのが困難であるなど、工学・物理学などでは通常生じないような問題を抱えています。本研究で提示した推定法は、粒子モデルという単純さから、組織の大小や生物種に依らず適用できることが予想されます。様々な組織において、形ができあがる物理的なメカニズムの研究に貢献できると考えています。
また、マウス胚での阻害実験の結果に基づくと、ある遺伝子の発現量の相違によって細胞間の相互作用の力に定量的な相違が生じると予想されます。さらに、著者らはマウス胚の中で細胞種によって異なる距離-力曲線を示すことも報告しています。細胞分化では遺伝子発現の変化とともに細胞間の相互作用の力の変化を伴う事例が多いことを考慮すると、本研究の推定法は細胞分化過程や癌化過程の発見・判別に活用できる可能性があります。深層学習AIと組み合わせた判別法などが考えられます。
【発表雑誌】
雑誌名 PLOS Computational Biology
掲載日 2023年8月7日
論文タイトル: Effective mechanical potential of cell–cell interaction explains three-dimensional morphologies during early embryogenesis
著者:Hiroshi Koyama, Hisashi Okumura Atsushi M. Ito Kazuyuki Nakamura Tetsuhisa Otani, Kagayaki Kato, and Toshihiko Fujimori,
DOI:https://doi.org/10.1371/journal.pcbi.1011306
【研究グループ】
基礎生物学研究所 小山宏史助教、藤森俊彦教授
分子科学研究所/生命創成探究センター 奥村久士准教授
核融合科学研究所 伊藤篤史准教授
生理学研究所 大谷哲久助教
生命創成探究センター/基礎生物学研究所 加藤輝特任助教
明治大学 中村和幸教授
【研究サポート】
本研究成果は下記のサポートを受けて実施されました。
科学研究費補助金 17K15131、22H05168(新学術領域「動く細胞と秩序」)
自然科学研究機構 若手研究者による分野間連携研究プロジェクト
【本研究に関するお問い合わせ先】
基礎生物学研究所 初期発生研究部門
助教 小山 宏史
【報道担当】
基礎生物学研究所 広報室