2023-09-27 京都大学iPS細胞研究所
1. 要旨
藤田みさお教授(CiRA上廣倫理研究部門、京都大学高等研究院ヒト生物学高等研究拠点)、澤井努准教授(広島大学大学院、京都大学高等研究院ヒト生物学高等研究拠点 連携研究者)、赤塚京子特定研究員(CiRA上廣倫理研究部門)、八田太一講師(静岡社会健康医学大学大学院、元CiRA上廣倫理研究部門 特定助教)らの研究グループは、日本の一般市民と科学者を対象にヒトゲノム編集の利用に関する質問紙調査を実施しました。
この度、その成果を2報の論文にまとめ、2023年6月22日、8月17日付で「Frontiers in Genetics」誌で発表しました。

2. 背景
2012年に新たなゲノム編集技術として登場したCRISPR-Cas9は、既存の技術に比べ、効率的かつ正確に遺伝子を改変できる特徴を持ち、その応用可能性に高い期待が寄せられています。既に一部の動植物の品種改良のためにこの技術は使用されていますが、2015年に中国の研究グループが、研究の一環でCRISPR-Cas9を用いてヒト受精卵(ヒト胚)の遺伝子改変に成功して以降、生命倫理学分野ではヒトへの技術応用に関する倫理的課題について議論が重ねられてきました。
ヒト胚の遺伝子改変が可能になれば、不妊や遺伝性疾患、難治性疾患の原因解明や治療法開発に関する研究が進展するのみならず、ヒトの遺伝子の働きや初期発生に関する知見の獲得にも繋がることが期待できます。これらは研究目的での技術利用の話になりますが、一方で、同じ技術を用いて遺伝子改変したヒト胚を女性の子宮に移植すれば、遺伝子操作した子を誕生させることも技術的には可能です。実際、2018年に中国の科学者がHIVの父子感染を回避する目的で、男性側がHIVキャリアであるカップルの受精卵に遺伝子改変をし、双子の赤ちゃんを誕生させたことが国際的に大きなニュースとなりました。CRISPR-Cas9の安全性の確認や利用に伴う倫理的課題の検討が十分にされていない段階でのこのような技術利用に対しては、国を超えて批判や懸念の声が殺到しました。
今日でも多くの国や学術団体は、生殖を目的としたゲノム編集技術のヒトへの応用を禁止する声明を出していますが、一部には、技術的安全性が確立したあかつきには、治療法がなく、特定の遺伝子配列に起因する重篤疾患などを対象とした遺伝子改変を支持する声もあります。しかし、技術的に可能であるとしても、疾患治療にこの技術を利用してよいかどうか、またどのような疾患を対象とすべきかについては慎重に検討する必要があるでしょう。さらに、子孫の遺伝子改変が疾患治療にとどまらなくなる可能性を考慮することも重要です。たとえば、誕生後に癌や糖尿病などの疾患に罹患する確率を下げる目的での遺伝子改変や、性別や肌の色、体質や能力といった疾患とは無関係の形質や特性にかかわる遺伝子改変についてはどうでしょうか。技術的に安全であれば、目的を限定せず技術利用を容認できるでしょうか。あるいは、目的次第で技術の利用を認めるべきでしょうか。
今日、国内外の関連学術団体は、こうした問いを研究者や政策決定者だけでなく、一般の方の声を取り入れながら社会で広く議論していくことを推奨しています。こうした状況のなか、一般市民を対象にしたヒトゲノム編集の利用についての意識調査が欧米を中心に実施されてきていますが、日本人を対象とした調査は僅かであり、ゲノム編集技術をどのように捉えているのか、どのような技術利用であれば認められるのかについて、十分に明らかにされていませんでした。加えて、殆どの先行調査は、医療目的でのゲノム編集の利用に焦点化していたことから、精子・卵子やヒト胚を遺伝子操作する研究について一般の方がどのように考えているかについては調査されてきませんでした。しかし、臨床応用の実現には研究段階での技術利用が不可欠です。仮に、回答者がゲノム編集の臨床応用を容認したとしても、研究段階でのゲノム編集に倫理的懸念があるとすれば、それは本当の意味でこの技術の利用を支持しているとは言えないでしょう。
発表した2本の論文では、研究から臨床応用までを見据えたヒトゲノム編集の利用について、日本の一般市民と科学者(日本ゲノム編集学会会員)を対象に質問紙調査を実施し、両者を比較することによって、それぞれの意識の違いやその背景にある要因について考察をしました。
3. 研究手法
2019年5月にオンライン調査を通じて、4,424名の一般市民と98名の科学者(日本ゲノム編集学会会員)から回答を収集しました。質問紙は大きく分けて、研究目的でヒト胚や精子・卵子、体細胞にゲノム編集を行うことについて尋ねた質問(1)と医療目的で誕生前(精子・卵子や胚の段階)や誕生後の人にゲノム編集を行うことについて尋ねた質問(2)で構成され、回答者にはゲノム編集の基本的な説明を提示したうえで、どのような技術利用を認められるかについて回答してもらいました。
本調査では、先行研究との差別化をはかるために、対象と目的を切り離した上でゲノム編集の許容度を尋ねました。具体的には、最初に全ての回答者に対して、ゲノム編集を行う対象(精子・卵子、ヒト胚(余剰胚1/研究胚2)、体細胞)への技術利用について尋ね、「いかなる目的でも認められる」「目的次第で認められる」「いかなる目的でも認められない」の3つの選択肢から一つを選んでもらいました。そして、「目的次第で認められる」を選択した回答者にのみ、ゲノム編集をする具体的な目的(例:著しく寿命が短い病気の治療のため、不妊症の研究のため、など)を複数提示し、認められるものを全て選択してもらいました。
今回、このような質問の仕方をしたのは、目的にかかわらず特定の対象へのゲノム編集に反対する回答者と、目的によりゲノム編集の利用に反対する回答者を区別するためです。これにより、なぜ、回答者がゲノム編集を「認められない」と回答したのかについて、より多様な視点から考察することが可能となりました。
4. 結果
1)研究目的でのヒトゲノム編集の利用について
精子・卵子(Germ cells)、余剰胚(Surplus IVF embryos)、研究胚(Research embryos)、体細胞(Somatic cells)へのゲノム編集の利用について尋ねたところ、一般市民(Laypeople)の28.2%~36.9%が「いかなる目的でも認められない(Not acceptable for any purpose)」と回答しましたが、対象によってこの割合に大きな違いは認められませんでした。一方、研究者(Researchers)の場合、ゲノム編集を「いかなる目的でも認められない」と回答した人の割合は、精子・卵子、余剰胚、体細胞では5.1%~9.2%であったのに対し、研究胚では25.5%となりました【図1】。
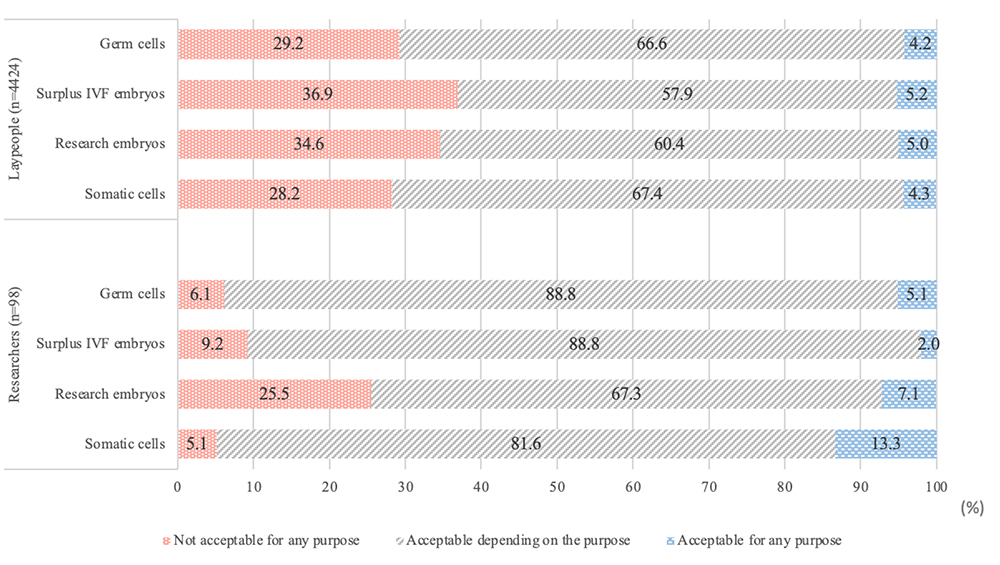
図1:研究目的でのゲノム編集の対象別許容度
次に、対象別許容度の質問で「目的次第で認められる(Acceptable depending on the purpose)」を選択した回答者に対して、具体的な研究目的を複数提示し、許容できるものを全て選んでもらいました。一般市民(Laypeople)では、不妊症(Infertility treatment)、難治性疾患(Intractable diseases)などに関する研究であれば50.4%~63.4%が、精子・卵子、余剰胚、研究胚、体細胞のゲノム編集を容認していましたが、目的がヒトの生物学的知見を得るという基礎研究(Basic research)になると、その割合は39.3%~42.8%と低くなりました。他方、研究者(Researchers)では、不妊症、難治性疾患、基礎研究については、73.6%~90.8%がゲノム編集を容認していましたが、慢性疾患研究(Chronic diseases)については60.9%~66.7%と、他の目的に比べて許容度は下がりました【図2】。
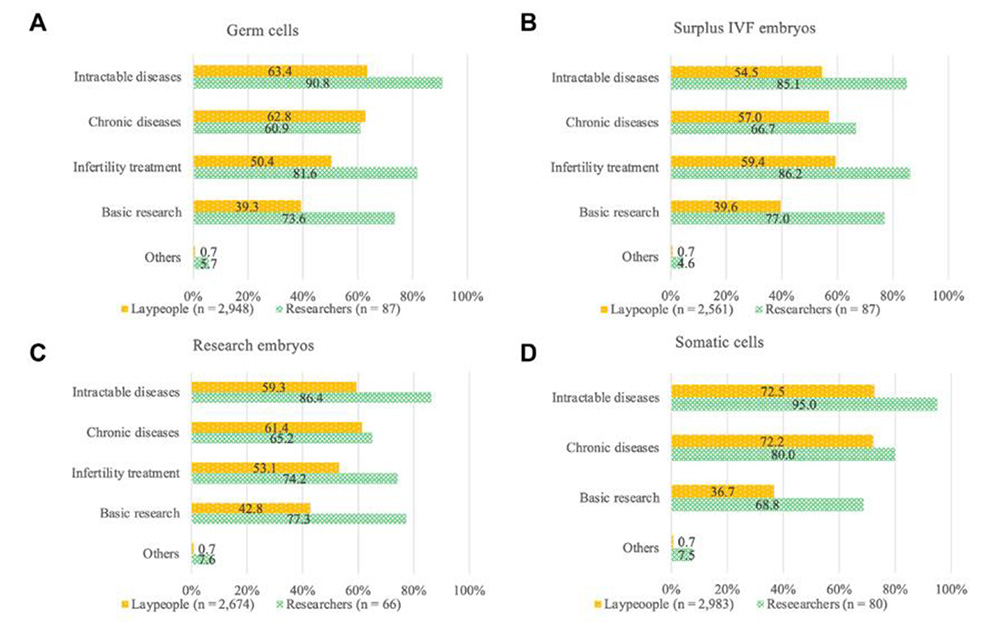
図2:研究目的でのゲノム編集の目的別許容度
(A. 精子・卵子、B. 余剰胚、C. 研究胚、D. 体細胞)
これらは結果の一部ですが、余剰胚と研究胚を区別して捉える傾向が研究者に顕著に見られることや、一般市民が疾患に関わる研究を許容しやすいことなどは、両者を比較することで得られた知見です。
2)医療目的でのゲノム編集の利用について
誕生前の段階(精子・卵子、胚)と誕生後(体細胞)に医療目的でゲノム編集を行うことについて尋ねました。なお、誕生前に実施するゲノム編集とは、生まれてくる子の遺伝形質を改変することを意味します。回答結果からは一般市民と研究者の間で回答の分布に差は認められませんでした。いずれも、回答者の半数近くが「目的次第で認められる(Acceptable depending on the purpose)」(一般市民49.3%、研究者56.1%)、4割以上が「いかなる目的でも認められない(Not acceptable for any purpose)」(一般市民45.8%、研究者40.8%)と回答し、「いかなる目的でも認められる(Acceptable for any purpose)」(一般市民5.0%、研究者3.1%)と回答したのは5%以下でした【図3】。
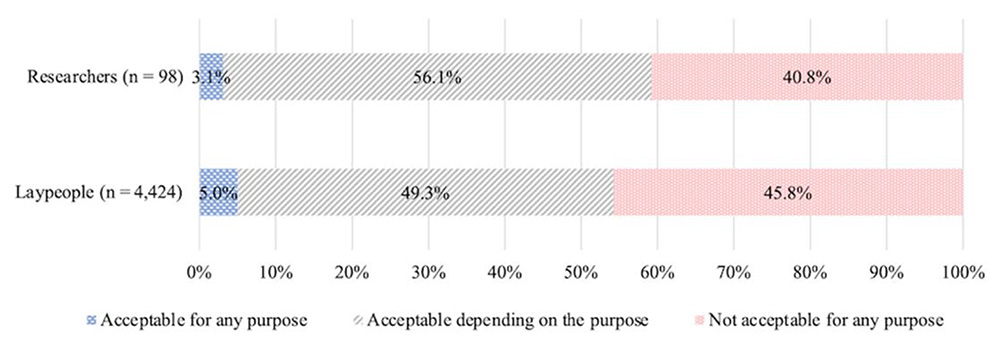
図3:医療目的で誕生前(精子・卵子、胚)に実施するゲノム編集の許容度
誕生後の人に実施するゲノム編集の利用について尋ねたところ、一般市民と研究者ともに「目的次第で認められる」の回答分布が高かった点は共通していましたが(一般市民63.6%、研究者89.8%)、「いかなる目的でも認められない」の回答分布は両者間で大きな差が見られました(一般市民32.6%、研究者3.1%)。ここからは、研究者の方が、一般市民よりも誕生後のゲノム編集を受け入れていることが読み取れます【図4】。
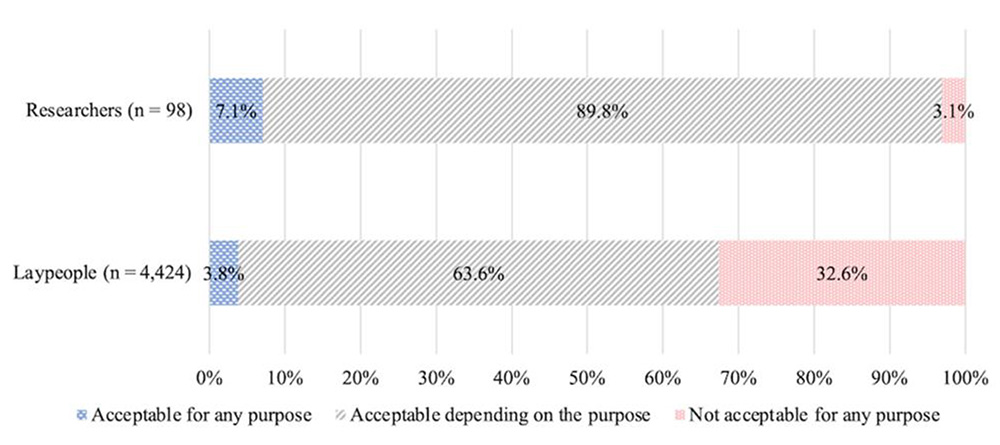
図4:医療目的で誕生後(体細胞)に実施するゲノム編集の許容度
次に、「目的次第で認められる」を選択した回答者に対して、医療目的でゲノム編集を実施する具体的な目的を提示し、認められるものを全て選んでもらいました。誕生前と誕生後のいずれにおいても、疾患の治療を目的とした利用に対する許容度が高い傾向にあるのに比べ、知性や体質、性格などの疾患以外の特性を改良するエンハンスメント目的での利用に対する許容度は顕著に低いことがわかりました。これらの傾向は一般市民と研究者に共通して見られました。一方で、疾患治療に関しては、一般市民に比べて研究者のほうがよりゲノム編集の利用を受け入れる傾向にあることがわかりました【図5、図6】。
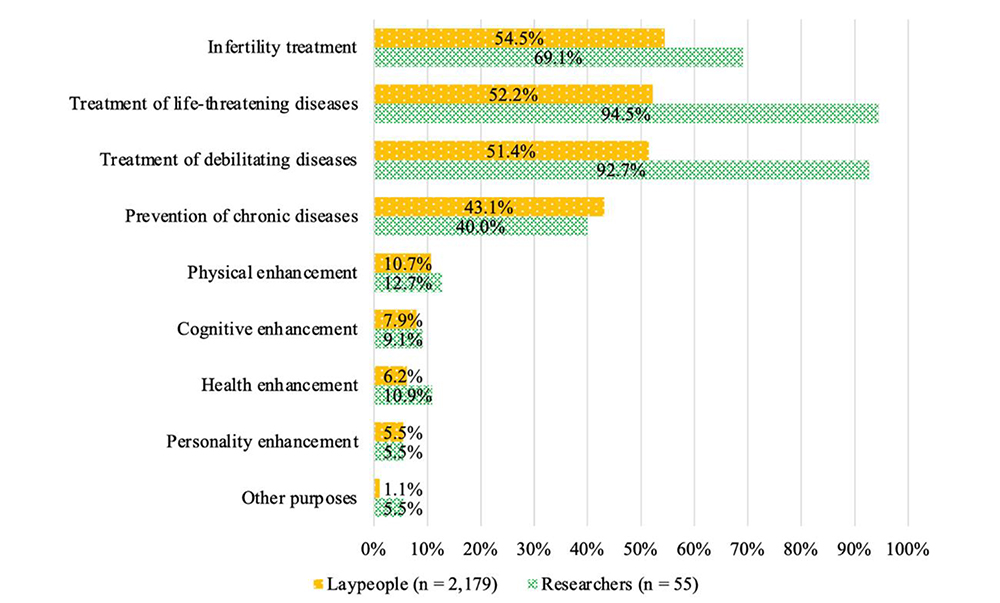
図5:医療目的で誕生前に実施するゲノム編集の目的別許容度
各項目は上から順に、不妊治療、生命を脅かす病気の治療、衰弱性疾患の治療、
慢性疾患の予防、体質改良、知性改良、健康増進、性格改善、その他。
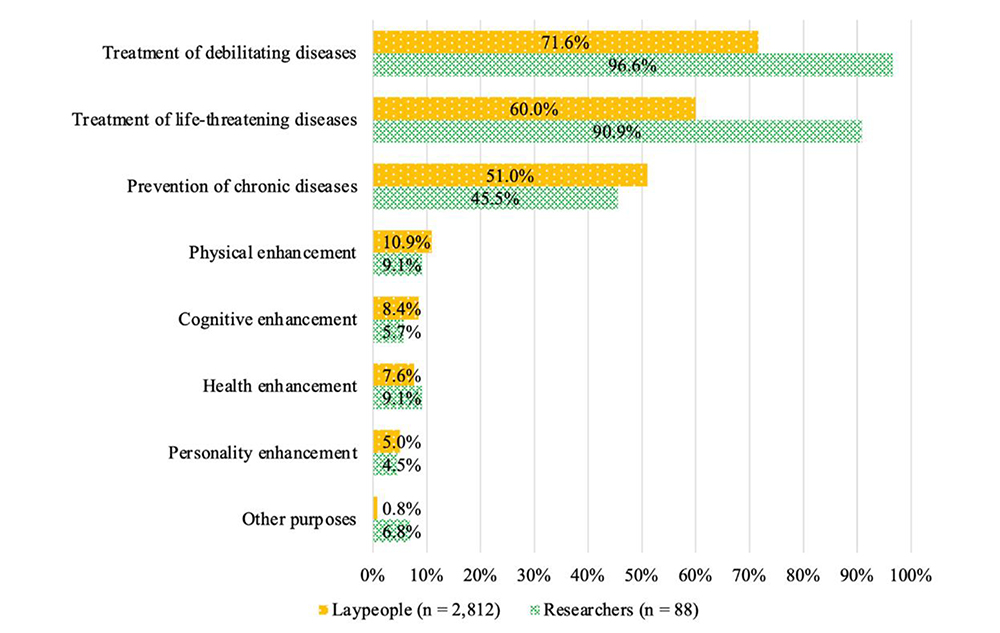 図6:医療目的で誕生後に実施するゲノム編集の目的別許容度
図6:医療目的で誕生後に実施するゲノム編集の目的別許容度
各項目は上から順に、衰弱性疾患の治療、生命を脅かす病気の治療、慢性疾患の予防、
体質改良、知性改良、健康増進、性格改善、その他。
以上をふまえると、疾患治療のゲノム編集は他の目的に比べて一般市民から理解を得やすいと考えられます。しかし、そもそも32.6〜45.8%の一般市民が医療目的でのゲノム編集を「いかなる目的でも認められない」と回答していた点を考慮すれば、現状では、疾患治療の目的であっても、一般市民の半数以上はゲノム編集の利用に抵抗を示していると言えるでしょう。
5. まとめ
本調査研究の成果は、研究目的でのヒトゲノム編集の利用に関する質問の結果をまとめた論文(1)と医療目的でのヒトゲノム編集の利用に関する質問の結果をまとめた論文(2)として報告されました。いずれにおいても、一般市民が研究者ほどにはゲノム編集技術の利用を受け入れられていない実態が明らかとなりました。この背景には、技術との距離感や知識量の差が影響しているとも考えられますが、そうしたものとは関係なく、専門家とそれ以外の人とでゲノム編集技術に対する評価が異なっている可能性もあります。今後、この技術の利用について社会で議論していくにあたり、専門家にとって自明的な価値観を議論の前提とするのではなく、多様なステイクホルダーの価値観に配慮した丁寧な議論の進め方を模索する必要があるでしょう。
6. 論文名と著者
【論文情報(1)】
- 論文名
Genome editing of human embryos for research purposes: Japanese lay and expert attitudes. - ジャーナル名
Frontiers in Genetics - 著者
Kyoko Akatsuka1, Taichi Hatta2, Tsutomu Sawai3,4, Misao Fujita1,4*
【論文情報(2)】
- 論文名
Human genome editing in clinical applications: Japanese lay and expert attitudes. - ジャーナル名
Frontiers in Genetics - 著者
Tsutomu Sawai3,4, Taichi Hatta2, Kyoko Akatsuka1, Misao Fujita1,4* - 著者の所属機関
- 京都大学iPS細胞研究所(CiRA)上廣倫理研究部門
- 静岡社会健康医学大学院大学
- 広島大学大学院 人間社会科学研究科
- 京都大学高等研究院 ヒト生物学高等研究拠点(WPI-ASHBi)
7. 本研究への支援
本研究は、下記機関より支援を受けて実施されました。
- 公益財団法人 上廣倫理財団
- 日本学術振興会 (JSPS)・文部科学省 科学研究費基金 若手研究(B)(17K13843)
- 日本学術振興会 (JSPS)・文部科学省 科学研究費基金 基盤研究(C)(18K10000, 21K10326)
- 文部科学省 世界トップレベル研究拠点プログラム(WPI)
- 日本医療研究開発機構(AMED)革新的先端研究開発支援事業(JP21gm1310011)
8. 用語説明
1. 当初は不妊治療のために作製したものの、生殖に利用する予定がなくなったヒト胚
2. 研究利用する目的で新たに作製したヒト胚