2024-01-11 国立がん研究センター
発表のポイント
- アジアでの大腸がんやその前がん病変の早期発見・治療を促進するため、日本、韓国、台湾、シンガポール、香港、タイの13施設で、大腸内視鏡検査を受ける大腸がん検診受診者を対象に、人工知能によるコンピュータ検出支援(CADe)を用いた大腸内視鏡検査の有効性を評価する多施設共同臨床試験を実施します。
- 本試験は、大腸がん検診における大腸内視鏡検査について、CADeを使用する検査法が、CADeを用いない通常の検査法よりも、病変を発見する割合が高いかどうかを検証します。
- 「アジアがん臨床試験ネットワーク構築に関する事業(ATLAS project)」と連動し、アジアでの新規検査法の開発に取り組みます。
概要
国立研究開発法人国立がん研究センター(理事長:中釜 斉、東京都中央区)中央病院(病院長:島田和明)は、大腸内視鏡検査での人工知能によるコンピュータ検出支援(CADe)注1の有効性をアジアで評価するため国内外13施設と共同で臨床試験(NCCH2217、研究略称:Project CAD)を開始しました。
大腸がんの治療を早期に行うためには、内視鏡検査時に前がん病変(ポリープ)や早期がんを見逃さないことが重要ですが、肉眼での認識が困難な病変や解剖学的死角、医師の技術差などにより一定頻度で見逃しが生じることが課題となっています。CADeは、人工知能(AI)を活用して前がん病変やがんを検査時にリアルタイムに検出し、検査を行う医師の診断を支援(補助)することができ、大腸内視鏡検査における病変発見の向上に寄与する可能性が期待されています。本試験では、薬事承認を得て製造販売されている医療機器を用いて大規模にCADeの有効性を評価し、日本のみならずアジアでの大腸がん検診における大腸内視鏡検査の質の向上を目指します。
本試験に参加する施設は、当院のほか国立がん研究センター東病院(所在地:千葉県柏市)、東京慈恵会医科大学附属病院(所在地:東京都港区)、東邦大学医療センター大森病院(所在地:東京都大田区)の国内4 施設と、海外(韓国、台湾、シンガポール、香港、タイ)9施設の合計13施設で、大腸内視鏡検査(便潜血検診、内視鏡検診両方を含む)を受ける受診者1,400人を対象に実施します。また、国立がん研究センター中央病院は2020年よりアジア地域での臨床研究・治験実施体制整備を目的とする「アジアがん臨床試験ネットワーク事業(Asian Clinical Trials Network for Cancers Project: ATLAS project) 注2」を開始しており、本試験は同事業とも連動し、アジア地域で国際共同試験を実施する体制構築と新規検査法の開発にも取り組みます。
背景
大腸がんは、日本を含めた多くの国において、がんによる死亡の主要な原因となっており、その早期発見や予防は非常に重要な課題です。大腸を調べる検査のうちで、大腸内視鏡検査は、大腸がんを早期発見できることに加えて、大腸がんの前段階である前がん病変(ポリープ)を発見し、取り除くことで、大腸がんになるリスクや大腸がんにより亡くなるリスクを低減できることが知られています。しかし、検査中に病変が見逃されてしまうことが一定の頻度で起こるとされており、大腸内視鏡検査の病変発見能をさらに向上させることは重要な課題となっています。
このような状況の中、近年、CADeが大腸内視鏡検査における病変発見能の向上に役に立つ可能性があるツールとして注目されており、大腸内視鏡検査においてCADeが有用であるという報告も増えています。しかし、日本を含めたアジアの大腸がん検診におけるその有用性は十分に証明されておらず、新たに検証する必要があります。
研究方法
本試験は、大腸がん検診における大腸内視鏡検査について、CADeを使用する検査法が、CADeを用いない通常の検査法よりも、病変を発見する割合が高いかどうかを検証します。また、本試験に用いるCADeは、当施設が企業と共同開発したCADeを含む薬事承認を得て製造販売されている医療機器で、通常の診療で使用される内視鏡装置・スコープから得られた画像に、大腸ポリープや大腸がんなどの病変の存在を示す印を内視鏡モニター上に表示することで、内視鏡検査を行う医師の支援を行います。そのため、用いられる内視鏡装置自体はすべて通常の診療で使用しているものと同じであり、特殊な内視鏡を使用することはありません。
研究名
人工知能によるコンピュータ検出支援を用いた大腸内視鏡検査の大腸がん検診における有効性評価:アジア多施設共同ランダム化比較試験(研究名称:Project CAD)

研究代表者
斎藤 豊(中央病院 内視鏡科 科長)
臨床研究実施計画・研究概要公開システム
jRCT番号:jRCT1032230396
本治験の詳細は、以下よりご確認ください。
臨床研究実施計画・研究概要公開システム
URL: https://jrct.niph.go.jp/latest-detail/jRCT1032230396(外部サイトにリンクします)
大腸内視鏡検査の方法
試験参加者には、「CADeを用いる大腸内視鏡検査(CADeグループ)」あるいは「CADeを用いない大腸内視鏡検査(従来法グループ)」のいずれかで大腸内視鏡検査を受けていただきます。検査法は、「無作為化割付」という方法により2分の1の確率でいずれかのグループに決定されます。どちらの検査法になっても不利益のリスクが最小限になるよう、日常診療において大腸がん検診受診者に対して大腸内視鏡検査を実施している医師が本試験でも大腸内視鏡検査を担当します。
試験参加者選択基準
- (1),(2)のいずれかの理由で全大腸内視鏡検査を受ける予定である。
(1) 大腸がん検診目的に最初から大腸内視鏡検査を受ける予定である。
(2) 便潜血検査を最初に行う大腸がん検診において便潜血陽性となり大腸内視鏡検査を受ける予定である。 - 登録時の年齢が50歳以上79歳以下である。
- ECOG Performance status注3が0または1である。
- 試験参加について受診者本人から文書で同意が得られている。
注:上記の選択基準に該当していてもこの試験に参加できないことがありますので、ご了承ください。
評価項目
主要評価項目は大腸腺腫発見割合(Adenoma detection rate:ADR)です。内視鏡検査1件当たりの大腸腺腫発見個数(Adenomas per colonoscopy:APC)やその他の病変の発見割合・個数、内視鏡検査時間、有害事象発生割などを副次的評価項目に設定しています。
予定登録数と研究期間
予定登録参加者数:1,400人
予定研究期間:3年(登録期間約2年、解析期間約1年)
研究開始日:2023年12月28日
研究の終了予定日:2026年12月31日
国内で使用される医療機器
- 内視鏡画像診断支援プログラムEndoBRAIN-EYE(製造販売業者:サイバネットシステム株式会社、製造販売元:オリンパス株式会社、承認番号:30200BZX00208000)
- 内視鏡検査支援プログラム EW10-EC02(CAD EYE)(製造販売業者:富士フイルム株式会社、承認番号:30200BZX00288000)
- WISE VISION 内視鏡画像解析AI(製造販売業者:日本電気株式会社、承認番号:30200BZX00382000)
研究参加施設一覧
日本
・国立がん研究センター中央病院
・国立がん研究センター東病院
・東京慈恵会医科大学附属病院
・東邦大学医療センター大森病院
韓国
・National Cancer Center
・Yonsei University Wonju College of Medicine
台湾
・National Taiwan University Hospital
・Fu Jen Catholic University Hospital
シンガポール
・National University Hospital, Singapore
・Singapore General Hospital
香港
・The Chinese University of Hong Kong
・CUHK Medical Centre
タイ
・Faculty of Medicine, Chulalongkorn University
研究支援企業一覧
- オリンパス株式会社
- 富士フイルム株式会社
- 日本電気株式会社
展望
本試験により、CADeを使用した大腸内視鏡検査の有効性が証明された場合は、CADeを使用することが大腸がん検診における大腸内視鏡検査の新たなスタンダードとなり、アジアの大腸がん検診における大腸内視鏡検査の質の向上や均てん化につながりし、大腸がん検診そのものの質の向上にもつながることが期待されます。
用語解説
*1 CADe
CADeは、Computer-Aided Detection(コンピュータ検出支援)を指します。人工知能(AI)を活用したソフトウェアで、内視鏡検査時に、大腸ポリープや大腸がんなどの病変の存在と位置を内視鏡モニター上にリアルタイムに表示することで、術者が病変を発見する支援を行います。
*2 ATLAS project
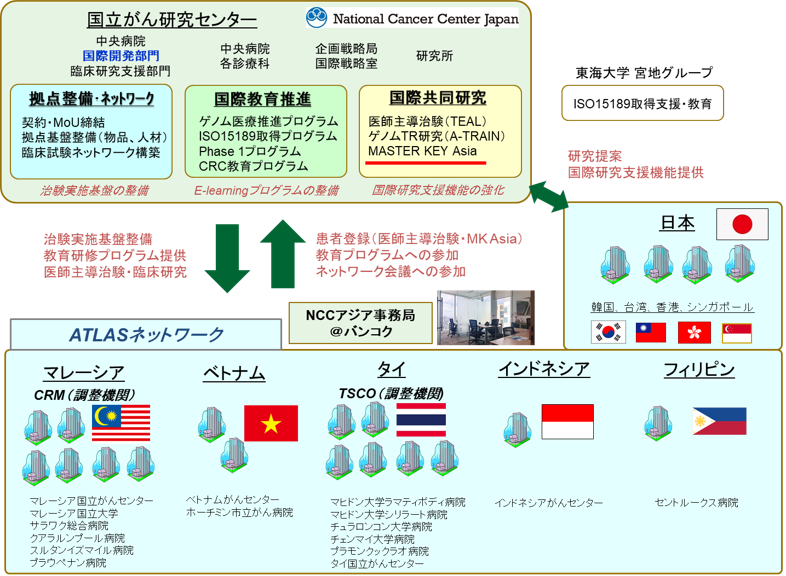
「ATLAS project:Asian clinical TriaLs network for cAncerS project」は、アジア地域でがん治療開発を今後積極的に推進しようとしているマレーシア、タイ、フィリピン、インドネシア、ベトナムと共に、国際共同試験のプラットフォームを日本主導で構築し、がんゲノム医療の導入と薬事承認申請のための医師主導治験/企業治験の実施を通じたアジア地域におけるがんの早期薬剤開発の発展を目指しています。また、アジア地域でのドラッグアクセスの改善とがんゲノム医療の本格的な導入を推進することでアジア全体での開発力を高め、アジア特有の課題をアジアで解決することを目指します。
日本にとってもアジア諸国と共同して治験を実施することにより、早期に試験を完了することができ、迅速な新規薬剤承認につながることが期待されます。最終的にはアジア地域での確固たる臨床試験ネットワークを構築し、アジアが世界の治療開発をリードしていくことを目指します(図1)。
2020年9月9日 プレスリリース
https://www.ncc.go.jp/jp/information/pr_release/2020/0909/index.html
図1 ATLASプロジェクト概要

*3 ECOG Performance status
米国の腫瘍学の団体の一つが設定する基準の一つ。(0:まったく問題なく活動できる。1:肉体的に激しい活動は制限されるが、歩行可能で、軽作業や座っての作業は行うことができる。)
問い合わせ先
研究に関する問い合わせ
国立研究開発法人国立がん研究センター
中央病院 内視鏡科/検診センター
関口 正宇
広報窓口
国立研究開発法人国立がん研究センター
企画戦略局 広報企画室