2024-04-19 東京大学
程 久美子(生物科学専攻 准教授/現:特任研究員)
高橋 朋子(埼玉大学 助教/兼:生物科学専攻 客員共同研究員)
米山 光俊(千葉大学 教授)
発表のポイント
- ウイルスが感染した細胞では、ウイルスから生体を防御するために、抗ウイルス性サイトカインであるI型インターフェロン(IFN)の分泌や細胞死といった抗ウイルス免疫応答が誘導されます。
- 本研究ではTRBPというタンパク質がウイルス感染により機能変換することで、ウイルス感染細胞の細胞死を促進するだけでなく、過剰なIFN分泌を抑制することを明らかにしました。
- この仕組みはウイルス感染細胞の免疫応答を制御する機構として機能していると考えられ、抗ウイルス治療や核酸医薬開発への応用が期待されます。
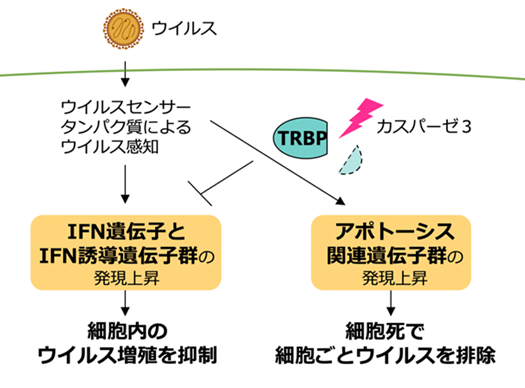
TRBPの切断によるウイルス感染細胞の免疫応答の制御
発表概要
東京大学大学院理学系研究科の高橋朋子客員共同研究員(兼:埼玉大学大学院理工学研究科助教)と程久美子准教授(研究当時、現:特任研究員)、千葉大学真菌医学研究センターの米山光俊教授らの研究グループは、RNAサイレンシングの制御因子であるTRBPがウイルス感染により機能変換することで、ウイルス感染細胞の抗ウイルス免疫応答が制御されることを明らかにしました。
ウイルスが細胞に感染すると、生体をウイルスから防御するために、抗ウイルス免疫応答が誘導されます。この免疫応答には、抗ウイルス性サイトカイン(注1)であるI型インターフェロン(IFN)の分泌や、アポトーシス(注2)と呼ばれるウイルス感染細胞の細胞死があります。IFNは細胞外に分泌されると、数百のIFN誘導遺伝子群(IFN-stimulated gene, ISG)と呼ばれるタンパク質の発現を誘導し、細胞を抗ウイルス状態にします。この応答はIFN応答とよばれ、細胞内のウイルス複製を抑制します。一方、ウイルス感染細胞のアポトーシスによる細胞死は、ウイルスが感染した細胞を細胞ごと生体から排除することで、生体内でのウイルス増殖を抑制します。ウイルス感染によるIFN応答と細胞死のバランスは、ウイルス増殖を効率よく抑制するために精密に制御されていると考えられますが、その仕組みは不明でした。本研究により明らかになったTRBPの機能変換がIFN応答と細胞死のバランスを制御する仕組みは、抗ウイルス治療や核酸医薬への応用が期待されます。
発表内容
TRBPは、マイクロRNAという20数塩基の小さなRNAが駆動する遺伝子発現制御機構において主要な機能をもつタンパク質です。この機構はRNAサイレンシング(注3)と呼ばれ、多様な遺伝子機能を制御しています。ヒトでは約2,000種類のマイクロRNAが存在しており、ひとつのマイクロRNAの欠損が癌などの重篤な疾患に繋がるなど、その機能の重要性は近年非常に注目されています。TRBPはマイクロRNA前駆体及びDicerというRNA切断酵素と相互作用することでマイクロRNAの成熟化(注4)を促進する重要な機能をもっています。
本研究ではまず、ヒト培養細胞にセンダイウイルスやニューカッスル病ウイルスなどが感染すると、TRBPが切断されることを明らかにしました。TRBPはウイルス感染により活性化したタンパク質切断酵素カスパーゼ3(注5)によって特定の部位で切断されました。またTRBPの切断は、ウイルスと同様の免疫応答を誘導する人工核酸Poly (I:C) (注6)または腫瘍壊死因子TNFαの処理によっても誘導されました。
切断されたTRBPがウイルス感染細胞においてどのような働きをするのかを調べたところ、TRBPは切断されることでDicerと相互作用しなくなり、マイクロRNAの成熟化を促進する機能を失うことが明らかとなりました。さらに、切断されたTRBPはIFN応答を制御するタンパク質と強く相互作用することも明らかになりました。
CRISPR/Casシステム(注7)を使って作製したTRBP欠損細胞に、切断されない変異型TRBPを発現させ、ウイルスを感染させました。すると、通常の切断されるTRBP発現細胞と比べて、切断されない変異型TRBP発現細胞ではウイルス感染による細胞死が減少したうえ、IFN量の増加が見られました。すなわち、TRBPの切断は、ウイルス感染細胞の細胞死を促進し、過剰なIFN分泌を抑制する働きがあると考えられます(図1)。
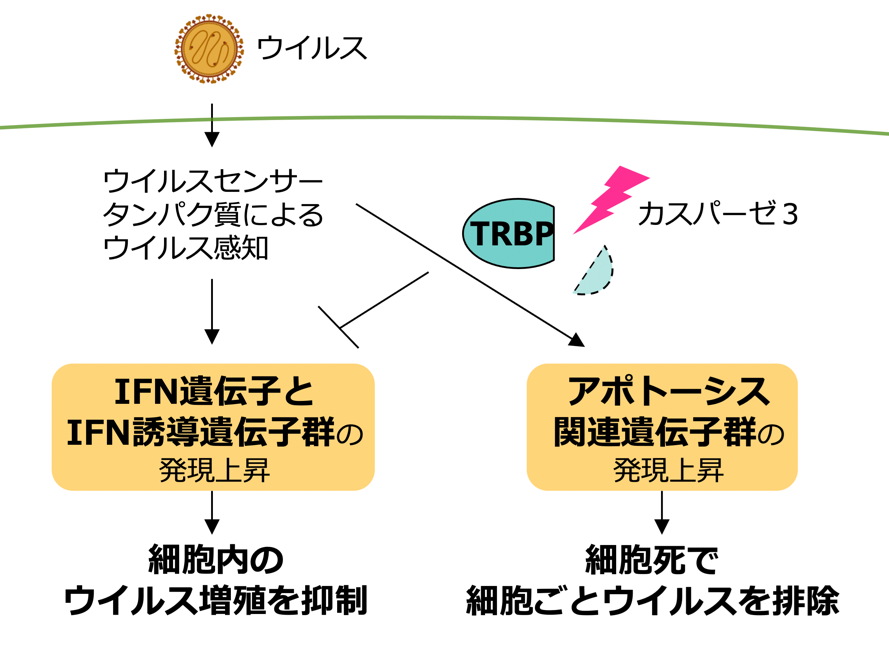
図1:TRBPの切断によるウイルス感染細胞の免疫応答の制御
ウイルス感染により活性化したカスパーゼ3によりTRBPが切断されると、ウイルス感染細胞の細胞死が促進され、過剰なIFN分泌が抑制される。
TRBPは、IFN応答をもたない無脊椎動物や植物では機能しておらず、IFN応答が抗ウイルス生体防御として重要な働きをもつ哺乳類でのみ機能しているタンパク質です。TRBPはウイルスが感染した哺乳類細胞において、IFN応答と細胞死のバランスを精密に制御するためのスイッチのような働きをしていると考えられます。本研究により明らかになった新しい免疫応答の仕組みは、抗ウイルス治療や近年臨床応用への期待が非常に高い核酸医薬(注8)への応用が期待されます。
<今後の展開>
mRNAワクチンを代表例として近年、核酸を用いた医薬品の応用が急速に進んでいます。マイクロRNAは疾患を治療するための医薬品としてだけでなく、疾患を早期に発見するためのバイオマーカーとしての応用も期待されています。本研究は、哺乳類で機能する抗ウイルス生体防御機構の分子メカニズムの解明にとどまらず、抗ウイルス治療や核酸医薬への応用が期待されます。
関連情報:
「プレスリリース①細胞内ウイルスセンサータンパク質による新しい生体防御の仕組みを発見」(2018/6/25)
「プレスリリース②マイクロRNAがウイルス感染細胞の細胞死を誘導する仕組みを発見」(2019/12/9)
論文情報
- 雑誌名
Nucleic Acids Research論文タイトル
Caspase-mediated processing of TRBP regulates apoptosis during viral infection著者
Keiko Shibata†, Harune Moriizumi†, Koji Onomoto, Yuka Kaneko, Takuya Miyakawa, Shuhei Zenno, Masaru Tanokura, Mitsutoshi Yoneyama, Tomoko Takahashi*, Kumiko Ui-Tei*
†筆頭著者 *責任著者DOI番号
10.1093/nar/gkae246
研究助成
本研究は、科研費「基盤研究B(課題番号:21310123, 研究代表者: 程久美子)」、「新学術領域研究(課題番号:21115004, 研究代表者: 程久美子)」「基盤研究B(課題番号:15H04319, 研究代表者: 程久美子)」「挑戦的萌芽研究(課題番号:16K14640, 研究代表者: 程久美子)」「若手研究B(課題番号:15K19124, 研究代表者: 高橋朋子)」「若手研究(課題番号:18K15178, 研究代表者: 高橋朋子)」、「公益財団法人セコム科学技術振興財団・挑戦的研究助成(研究代表者: 高橋朋子)」「公益財団法人内藤記念科学振興財団・内藤記念科学奨励金(研究代表者: 高橋朋子)」「公益財団法人武田科学振興財団・生命科学研究助成(研究代表者: 高橋朋子)」「公益財団法人MSD生命科学財団・研究助成感染症領域(研究代表者: 高橋朋子)」「公益財団法人キヤノン財団・善き未来をひらく科学技術(研究代表者: 高橋朋子)」「公益財団法人日立財団・倉田奨励金(研究代表者: 程久美子, 高橋朋子)」「千葉大学真菌医学研究センター共同利用・共同研究(課題番号:14-14, 15-16, 16-1, 17-15, 18-11, 19-1, 20-1, 21-05, 22-04, 23-04, 24-04)」の支援により実施されました。
用語解説
注1 サイトカイン
細胞から分泌されるタンパク質であり、細胞間相互作用に関与する生理活性物質の総称。
注2 アポトーシス
多細胞生物の細胞において能動的に起こる、プログラムされた細胞死で、システインプロテアーゼであるカスパーゼの活性化により誘導される。
注3 RNAサイレンシング
マイクロRNAやsmall interfering RNA (siRNA)という長さ20数塩基の短いRNAが、全長あるいは部分的に相補的な配列をもつ遺伝子のmRNAを切断したり、翻訳抑制して遺伝子発現を阻害する現象。マイクロRNAはヒトゲノムに約2,000種類コードされている。RNAサイレンシングには、TRBPだけでなく、Argonaute, Dicer, TNRC6などのタンパク質が重要な役割を担うことがわかっている。
注4 マイクロRNAの成熟化
マイクロRNAやsmall interfering RNA (siRNA)という長さ20数塩基の短いRNAが、全長あるいは部分的に相補的な配列をもつ遺伝子のmRNAを切断したり、翻訳抑制して遺伝子発現を阻害する現象。マイクロRNAはヒトゲノムに約2,000種類コードされている。RNAサイレンシングには、TRBPだけでなく、Argonaute, Dicer, TNRC6などのタンパク質が重要な役割を担うことがわかっている。
注5 カスパーゼ3
アポトーシスが誘導された細胞で活性化するタンパク質切断酵素で、特定のアミノ酸配列を認識して切断する。
注6 Poly (I:C)
ポリイノシンとポリシチジンで構成される人工合成二本鎖RNAで、ウイルスセンサータンパク質により認識され、ウイルスと同様の免疫応答を誘導する。
注7 CRISPR/Casシステム
近年開発されたゲノム編集技術であり、Casタンパク質とガイドRNAを用いて、特定の遺伝子の機能を欠損させることが可能。
注8 核酸医薬
DNAやRNAなどの核酸分子から作られる医薬品の総称で、タンパク質に翻訳されることなく直接生体に作用する。