2024-09-17 国立がん研究センター,兵庫医科大学
発表のポイント
- 国内外152施設が参加する研究プロジェクトCIRCULATE-Japan(サーキュレートジャパン)*1における世界最大規模の前向き研究の大腸がん肝転移手術例によるサブ解析においてリキッドバイオプシー*2の有用性が明らかになりました。
- 術後2-10週の間の血中循環腫瘍DNA*3(circulating tumor DNA [ctDNA])の結果が陽性であれば術後補助化学療法*4により再発リスクが低下しますが、陰性であれば術後補助化学療法による再発リスクが低下しないことがわかりました。
- 本研究の結果、術後のctDNAを測定することで、再発リスクに応じた術後補助化学療法の個別化に繋がることが期待されます。
概要
国立研究開発法人国立がん研究センター(理事長:中釜 斉、東京都中央区)東病院(病院長:土井 俊彦、千葉県柏市)の吉野 孝之 副院長、兵庫医科大学(学長:鈴木 敬一郎、兵庫県西宮市) 消化器外科学(下部消化管外科)の片岡 幸三 講師らの研究グループは、大腸がん術後にctDNAを検査する技術(リキッドバイオプシー)を用いて再発リスクをモニタリングするレジストリ研究(GALAXY試験*5)に登録された患者さんの中で、外科治療が行われた大腸がん肝転移患者さんに絞った解析を実施しました。
解析の結果、術後2-10週の間にctDNA陽性の大腸がん肝転移の患者さんは、陰性患者さんと比較して、術後の再発リスクが高いことがわかりました。また、術後2-10週にctDNA陽性の患者さんは、術後補助化学療法を受けることで、術後補助化学療法を受けなかった患者さんよりも再発リスクが低いものの、術後2-10週にctDNA陰性の患者さんは術後補助化学療法を受けても再発リスクは下がらないことがわかりました。
今まで大腸がん肝転移における術後補助化学療法が全生存期間を延長することを示した報告はありません。すでに、大腸がん術後のリキッドバイオプシーの有用性は報告されておりますが、大腸がん肝転移の患者さんにリキッドバイオプシーを行うことで、再発リスクに応じた術後補助化学療法の個別化が期待されます。
本研究成果は、科学雑誌「Annals of Oncology」で発表(ヨーロッパ時間2024年9月16日12時付)されました。
背景
大腸がん肝転移の患者さんに術後補助化学療法が有用かどうかは未だわかっておらず、術後の再発リスクに応じた術後補助化学療法の使用が期待されています。大腸がん術後のリキッドバイオプシーが術後の再発を予測する有用なバイオマーカーであることは国内外約150施設(台湾1施設を含む)の協力を得て行われた世界最大規模の前向き研究であるGALAXY試験の中間結果からすでに報告済みですが、リキッドバイオプシーが大腸がん肝転移の患者さんにおいても術後の個別化医療にどの程度有用かどうかはまだ明らかではありません。
以上の背景から、本研究は、GALAXY試験に登録された患者さんの中から、大腸がん肝転移に対して初回手術を実施した患者さんについて解析を行いました。米国Natera社が開発した高感度遺伝子解析技術「Signatera(シグナテラ)」アッセイを用いて、ctDNAの測定を術前および術後4週時点から定期的に血液を採取し、血液中のがん遺伝子異常の有無を調べました。2020年5月から2024年6月の間にGALAXY試験に登録された6061例中、大腸がん肝転移に対して肝切除を実施した患者さんで、十分な臨床情報とctDNAの結果が揃っている190例を対象に解析を行いました。
研究の方法・成果
大腸がん肝転移に対して初回手術を行った190例のうち、術後2-10週の間でctDNA陽性例と陰性例に分け、陽性例、陰性それぞれにおいて、術後補助化学療法を受けた患者さんと受けなかった患者さんで再発割合を比較しました。
術後2-10週の間にctDNA陽性であった61例では、術後補助化学療法を受けなかった患者さんでは無病生存割合の中央値1.45か月であったのに対し、術後補助化学療法を受けた患者さんでは12.9か月と再発リスクが低下することがわかりました(ハザード比*6 0.07、P<0.0001)(図1)。
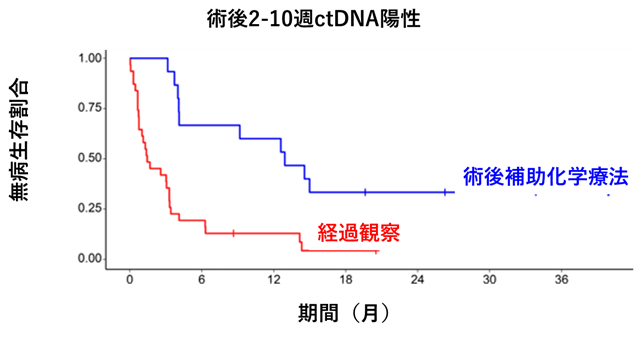
図1 術後ctDNA【陽性】例の術後補助化学療法群と経過観察群の無病生存割合の比較
一方、術後2-10週の間にctDNA陰性であった129例では、術後補助化学療法を受けなかった患者さんは24か月時点での無病生存割合が62.3%、術後補助化学療法を受けた患者さんは72.3%と統計学的な有意差は認められませんでした(ハザード比 0.68、P=0.371)(図2)。
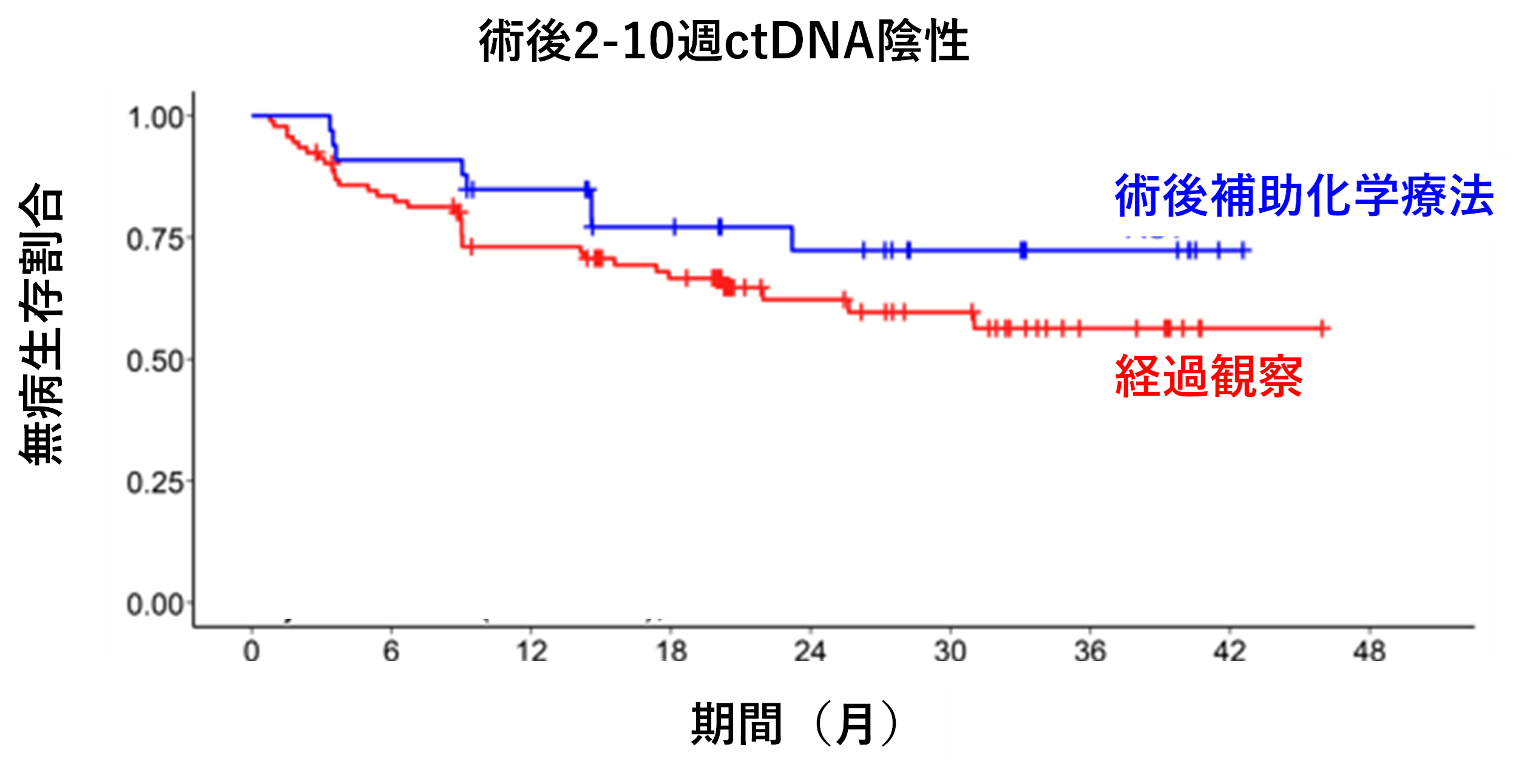
図2 術後ctDNA【陰性】例の術後補助化学療法群と経過観察群の無病生存割合の比較
さらに、ctDNA陽性例と陰性例で再発臓器を比較したところ、陽性例では陰性例と比較して肝転移再発が多い(73.6% vs. 33.3%, P=0.0004)のに対して、陰性例では陽性例と比較して肺転移再発が多く(61.9% vs.26.4%, P=0.0021)、統計学的に有意な差が見られました(図3)。
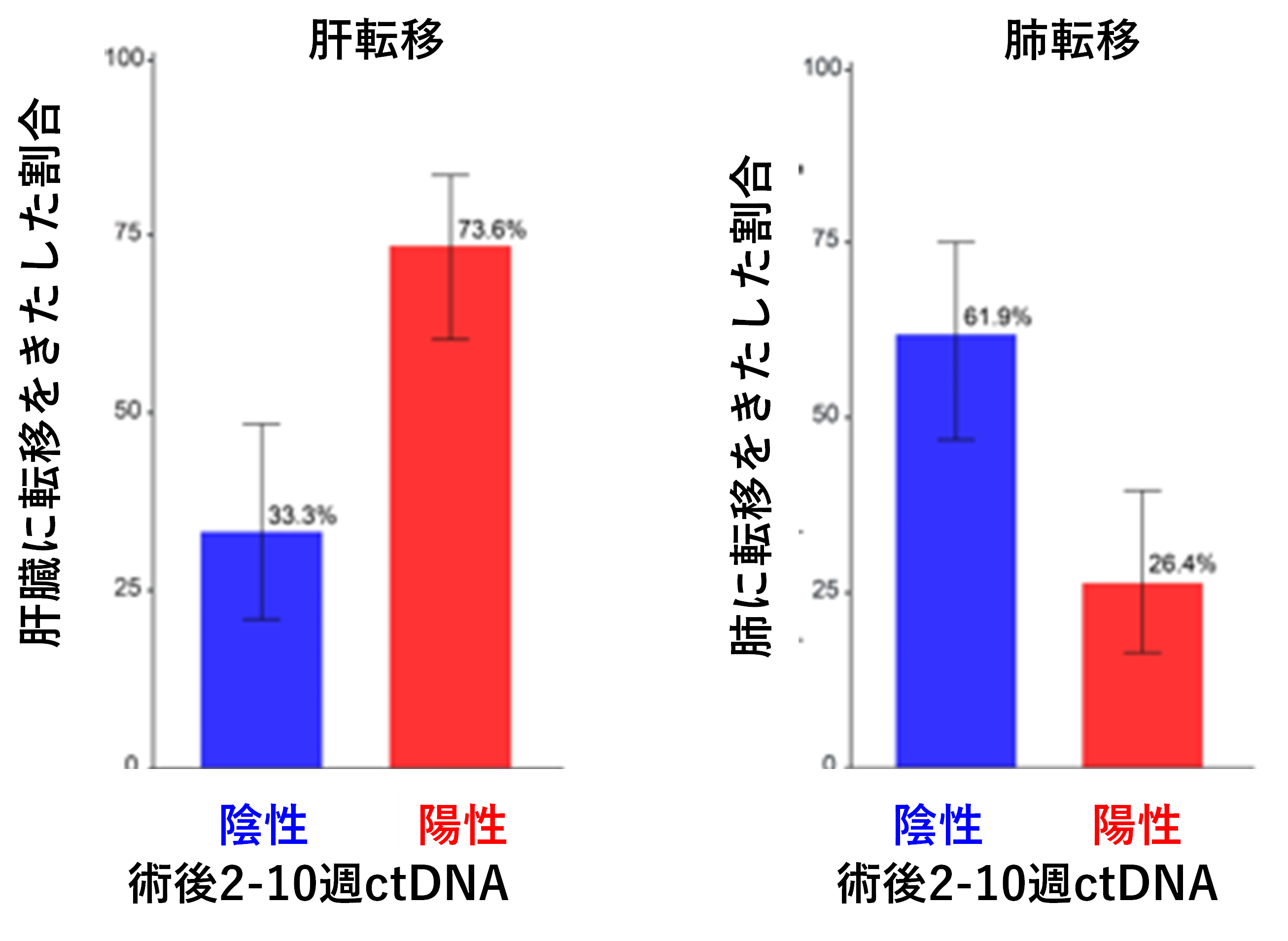
図3 術後ctDNA別の肝と肺に転移をきたした割合
以上の結果から、大腸がん肝転移の患者さんに対しては、術後2-10週の間のctDNAの陽性例では術後補助化学療法を行うことで再発リスクを低下させるが、陰性例では術後補助化学療法を行っても再発リスクが低下しない可能性が示されました。
また、陽性例と陰性例で再発臓器が異なることを念頭においた術後の画像検査が重要である可能性が示唆されました。
展望
大腸がん肝転移の患者さんに術後補助化学療法が有用かどうか、今まで数々の臨床試験が実施されてきましたが、術後補助化学療法が全生存期間を延長することを示した報告はありません。今後、より長期のフォローアップにより、全生存期間に関しても術後ctDNAと術後補助化学療法の関連が明らかになれば、再発リスクに応じた術後補助化学療法の個別化につながることが期待されます。一方、陰性の場合は肺転移再発が多いことから、肺転移に対するctDNAの感度が、肝転移のそれと比べて不十分である可能性が示唆されます。
しかしながら、本研究の結果のみで、術後2-10週の間にctDNA陰性である場合、術後補助化学療法が不要であるか結論づけることはできませんでした。解析された患者さんの数が十分でなく、また本研究において術後補助化学療法を行うかどうかは担当医によって判断されたため、ctDNA以外の臨床病理学的な背景等が術後後補助化学療法を受けた患者さんと受けなかった患者さんでは異なる可能性があるからです。本研究結果を検証するための更なる解析の結果が期待されます。
論文情報
雑誌名
Annals of Oncology
タイトル
Survival benefit of adjuvant chemotherapy based on molecular residual disease detection in resected colorectal liver metastases: Subgroup analysis from CIRCULATE-Japan GALAXY
著者
Kozo Kataoka, Keita Mori, Yoshiaki Nakamura, Jun Watanabe, Naoya Akazawa, Keiji Hirata, Mitsuru Yokota, Kentaro Kato, Masahito Kotaka, Kentaro Yamazaki, Yoshinori Kagawa, Saori Mishima, Koji Ando, Masaaki Miyo, Hiroki Yukami, George Laliotis, Shruti Sharma, Charuta C. Palsuledesai, Matthew Rabinowitz, Adham Jurdi, Minetta C. Liu, Alexey Aleshin, Daisuke Kotani, Hideaki Bando, Hiroya Taniguchi, Ichiro Takemasa, Takeshi Kato, Takayuki Yoshino, Eiji Oki,* (*は責任著者)
DOI
10.1016/j.annonc.2024.08.2240
掲載日
2024年9月16日12時(ヨーロッパ時間)
URL
https://www.annalsofoncology.org/article/S0923-7534(24)03763-3/fulltext(外部サイトにリンクします)
研究費
国立研究開発法人日本医療研究開発機構(AMED)
研究事業名:革新的がん医療実用化研究事業
研究課題名:SCRUM-Japanの基盤を活用した血液循環腫瘍DNAスクリーニングに基づくFGFR遺伝子異常を有する難治性の治癒切除不能な進行・再発固形がんに対する TAS-120 のバスケット型医師主導治験
研究代表者名:吉野 孝之
用語解説
*1 CIRCULATE-Japan(サーキュレートジャパン)

大腸がんの外科治療を受ける患者さんの術後再発リスクを最新のリキッドバイオプシー解析技術を用いて高精度に推定し、より適切な医療を提供することを目的としたプロジェクト。国内外152施設(うち海外1施設を含む)が参加する。大規模な医師主導国際共同臨床試験(GALAXY、VEGA、ALTAIR)から構成され、GALAXY試験は基幹となる試験となります。
◆参考プレスリリース
・2020年6月10日「リキッドバイオプシーによるがん個別化医療の実現を目指す新プロジェクト「CIRCULATE-Japan」始動-見えないがんを対象にした世界最大規模の医師主導国際共同臨床試験を開始-」
https://www.ncc.go.jp/jp/information/pr_release/2020/0610/index.html
*2 リキッドバイオプシー
患者さんの血液を用いてがんのゲノム異常を検出する検査。血液検査で繰り返し測定可能であるため、身体に負担が少なく、がんの再発をより早期に発見できることが期待される。
*3 血中循環腫瘍DNA
血液中にごく微量に存在するがん由来のDNA。
*4 術後補助化学療法
がんの手術後に行う抗がん剤治療。手術後にも残っている可能性がある目に見えない小さながん細胞をなくし、再発の可能性を減らすために行います。
*5 GALAXY試験
CIRCULATE-Japanプロジェクトの3つの医師主導国際共同臨床試験のうち基幹となる試験で、大腸がん手術前後に経時的にctDNAを解析し、再発や生存期間との関連を調べます。
◆参考プレスリリース
・2023年1月24日「リキッドバイオプシーが大腸がん術後の再発リスク測定に有用であることを確認
-世界最大規模の前向き研究により術後補助化学療法の個別化を目指す-」
https://www.ncc.go.jp/jp/information/pr_release/2023/0124/index.html
*6 ハザード比
時間当たりの再発リスクの比。
お問い合わせ先
研究に関するお問い合わせ
国立研究開発法人国立がん研究センター東病院
トランスレーショナルリサーチ支援室
束岡 広樹
学校法人兵庫医科大学
消化器外科学 下部消化管外科
講師 片岡 幸三
広報窓口
国立研究開発法人国立がん研究センター
企画戦略局 広報企画室(柏キャンパス)
学校法人兵庫医科大学
総務部 広報課