骨病変を制御する治療標的因子の候補として期待
2019-02-20 北海道大学,日本医療研究開発機構
ポイント
- 血液のがんである多発性骨髄腫細胞においてインターロイキン-34*1(IL-34)の発現を初めて同定。
- 多発性骨髄腫細胞が分泌するIL-34が、骨病変を促進する役割をもつことを解明。
- IL-34は、骨髄腫患者における骨病変を制御する新たな治療標的因子の候補として期待される。
概要
北海道大学遺伝子病制御研究所免疫生物分野の清野研一郎教授、同大学院医学研究院血液内科学教室の豊嶋崇徳教授らの研究グループは、血液のがんの一つである多発性骨髄腫細胞が分泌するIL-34が、骨病変を促進する役割をもつことを初めて解明しました。
多発性骨髄腫の主要な合併症として、痛みや骨折を伴う骨病変があげられます。骨病変に対しては、骨を溶かす細胞である破骨細胞を抑制する治療薬がいくつか開発されてきましたが、難治性の骨症状を訴える患者が依然として存在します。
本研究では、骨髄腫細胞から分泌されるIL-34が骨病変に関わる病理学的要因であることを初めて同定しました。マウスやヒトの骨髄腫細胞株、また骨髄腫の臨床検体を用いた実験では、IL-34があると骨病変を引き起こす破骨細胞の分化*2や活性化がさらに促進されることがわかりました。今後、骨髄腫患者における破骨細胞の病的な形成を制御するために、IL-34が新たな治療標的因子となる可能性があります。
なお、本研究成果は、米国東部時間2019年2月19日(火)公開のBlood Advances誌に掲載される予定です。
背景
多発性骨髄腫は、Bリンパ球から分化した形質細胞の腫瘍です。多発性骨髄腫には様々な合併症がありますが、中でも骨破壊性疾患は特に患者数が多い疾患です。これまでに骨を溶かす細胞である破骨細胞を抑制する治療薬がいくつか開発されてきましたが、難治性の骨症状を訴える患者が依然として存在します。そのため、多発性骨髄腫において骨破壊性疾患を引き起こす要因の解明が待たれています。
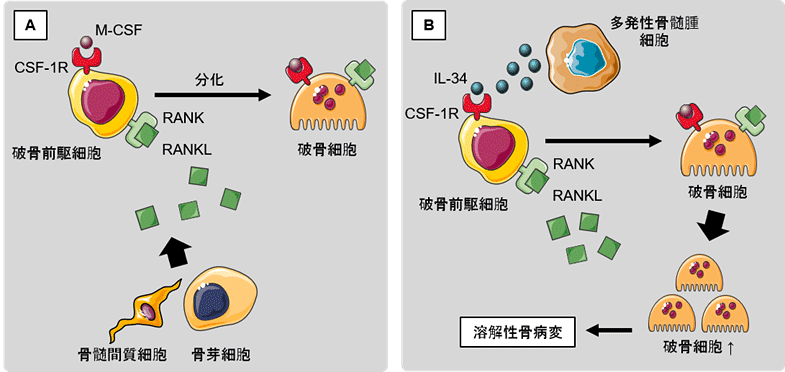
骨破壊性疾患を引き起こす破骨細胞の形成には、サイトカイン(細胞に変化を生じさせるタンパク質の一種)であるRANKLの存在と、CSF-1Rと呼ばれる糖タンパク質レセプター*3によるシグナルの活性化が必要です。CSF-1Rには、M-CSFとIL-34の2つのリガンド*4があります。IL-34は近年新たに発見され、M-CSFと共通のレセプターであるCSF-1Rに結合するサイトカインです。M-CSFと同様に免疫抑制性マクロファージへの分化や生存、増殖に関与し、in vitro(人工的な実験環境下)で破骨細胞の分化を誘導できることが明らかとなっています。本研究では、CSF-1RのリガンドとしてIL-34に着目し、多発性骨髄腫に伴う骨病変における役割を検討しました。
研究手法
本研究では、多発性骨髄腫細胞としてマウス多発性骨髄腫細胞株であるMOPC315.BMを用いました。骨髄腫細胞株でのIL-34の発現を、RT-PCRとELISAと呼ばれる手法により解析しました。また、多発性骨髄腫細胞は骨髄間質細胞(BMSC)と相互作用して破骨細胞を誘導するという報告から、これらの細胞を共培養し、破骨細胞活性化因子の発現を解析しました。
さらに、骨髄腫細胞株とBMSCを共培養した培地を用いて、骨破壊性疾患の原因となる破骨細胞を誘導できるか検証しました。加えて、IL-34の発現を抑制した骨髄腫細胞株を用いて、実際にマウスにおける骨病変を検証しました。最後に、ヒト多発性骨髄腫細胞株や臨床検体を用いて、IL-34の発現や破骨細胞の誘導性、骨病変との関連について検討しました。
研究成果
骨髄腫細胞株でのIL-34の発現を解析したところ、健常マウスの骨髄、末梢血、リンパ節、脾臓由来の形質細胞やB細胞と比較して非常に強い発現が認められました。この発現は炎症性サイトカイン刺激やBMSCとの共培養により、さらに上昇することがわかりました。次に、骨髄腫細胞株とBMSCを共培養した培地の上清(上澄み)を用いて、骨破壊性疾患の原因となる破骨細胞を誘導できるか検証したところ、IL-34発現を抑制していない骨髄腫細胞株の上清を用いた場合はTRAP染色陽性の破骨細胞が誘導されましたが、IL-34発現を抑制した骨髄腫細胞株の上清では破骨細胞は誘導されず、生細胞は存在しませんでした。
これらの結果から、多発性骨髄腫細胞のIL-34発現を抑制することで破骨細胞の形成が抑制され、骨病変が改善すると予想され、BALB/cマウスに、骨髄腫細胞株か、あるいは、IL-34発現を抑制した骨髄腫細胞株を尾静脈注射して骨病変や血中カルシウム濃度の変化を解析しました。すると、IL-34発現を抑制した骨髄腫細胞株を注入した場合は、マウスの骨病変は軽減し、血中カルシウム濃度も有意に低下しました。
次に、ヒト多発性骨髄腫細胞株や臨床検体を用いて、IL-34の発現や破骨細胞の誘導性、骨病変との関連について検討したところ、ヒト多発性骨髄腫細胞株において炎症性サイトカイン刺激によるIL-34の発現上昇が認められました。骨髄腫患者(合計15人)の臨床検体におけるIL-34の発現を解析し、発現が強いもの、中程度のもの、発現していないものの3グループに分類しました。他の2グループと異なり、IL-34の発現が強かった骨髄患者は100%の確率で骨病変があり、正常単球から破骨細胞への誘導性が強いという結果が得られました。これらの検体で抗IL-34阻害抗体により破骨細胞の誘導性が軽減されたことから、骨髄腫細胞に分泌されるIL-34が骨病変を促進すると考えられました。
今後への期待
本研究によって、多発性骨髄腫細胞とBMSCの相互作用によりIL-34を含む破骨細胞活性化因子が産生され、破骨細胞が誘導されることが明らかとなりました。さらに、多発性骨髄腫細胞のIL-34発現を抑制することによって、マウスの骨病変が軽減されました。したがって、IL-34をターゲットとした治療は、多発性骨髄腫に伴う骨破壊性疾患を改善する可能性があります。今後、多発性骨髄腫由来IL-34による骨破壊性疾患への影響に関する研究が進み、IL-34を治療標的とした治療法が確立されることが期待されます。
研究費
本研究は、国立研究開発法人日本医療研究開発機構(AMED)の革新的がん医療実用化研究事業「IL-34を基軸としたがん微小環境分子基盤の理解とその臨床的特性に基づいた新しい治療法の開発」(研究開発代表者:清野研一郎)、共同利用・共同研究拠点特別共同研究(研究代表者:豊嶋崇徳)、独立行政法人日本学術振興会科学研究費助成事業若手研究(研究開発代表者:Muhammad Baghdadi)、公益信託日本白血病研究基金(研究開発代表者:清野研一郎)の支援を受けて行われました。
論文情報
- 論文名
- A role for IL-34 in osteolytic disease of multiple myeloma(多発性骨髄腫の骨病変におけるIL-34の役割)
- 著者名
- Muhammad Baghdadi1,石川 浩三1,中西 沙耶香1,村田 智己1,梅山 悠伊1,小林 拓斗1,亀田 洋輔1,遠藤 拓1,和田 はるか1,Bjarne Bogen2,山本 聡3,山口 圭介3,笠原 郁美3,岩崎 博4,高畑 むつみ4,井端 淳4,高橋 秀一郎5,後藤 秀樹5,豊嶋 崇徳5,清野 研一郎1
(1北海道大学遺伝子病制御研究所免疫生物分野,2ノルウェイ オスロ大学インフルエンザワクチン研究KG Jebsenセンター,3市立札幌病院血液内科,4札幌厚生病院血液内科,5北海道大学大学院医学研究院血液内科学教室) - 雑誌名
- Blood Advances(米国血液学会の専門誌)
- 公表日
- 日本時間2019年2月20日(水)午前2時(米国東部時間2019年2月19日(火)正午)(オンライン公開)
参考図
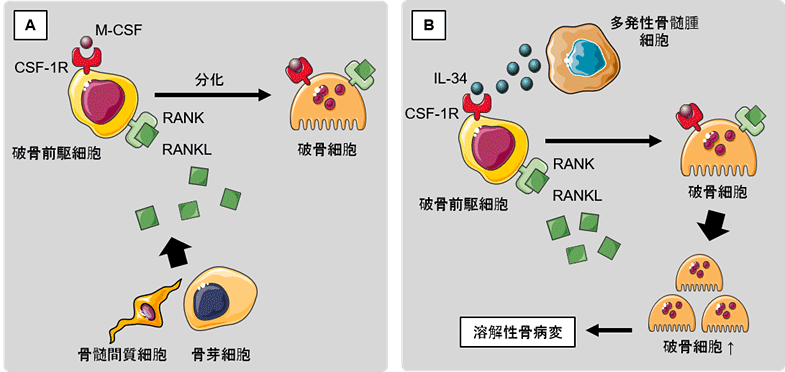
(A)
正常な状態では、RANKLの存在下で、破骨前駆細胞(破骨細胞に分化する前の細胞)に発現するCSF1RとM-CSFが結合することにより、破骨細胞への分化が促進される。
(B)
多発性骨髄腫患者では、RANKLの存在下で、多発性骨髄腫細胞から多量に発現しているIL-34がM-CSFが存在しなくてもCSF1Rと結合し、破骨細胞への分化を誘導する。よって、破骨細胞の働きが過剰に亢進する状態となる。
用語解説
- *1 インターロイキン-34(IL-34)
- インターロイキンとは白血球から分泌されるタンパク質で、細胞同士の連絡を担うもの。30種類以上が知られており、IL-34は34番目に同定された。
- *2 分化
- 特殊化されていない細胞が、より特殊な機能をもった細胞に変化するプロセスのこと。
- *3 レセプター
- 外界からの何らかの刺激を受け取り、情報として利用できるように変換する仕組みを持った、細胞における構造のこと。
- *4 リガンド
- 特定のレセプターに特異的に結合し、レセプターを活性化させる物質のこと。
お問い合わせ先
研究内容に関すること
北海道大学遺伝子病制御研究所免疫生物分野 教授 清野 研一郎(せいの けんいちろう)
URL:https://seinolab.wixsite.com/seinolab/home-1
配信元
北海道大学総務企画部広報課
AMEDに関すること
国立研究開発法人日本医療研究開発機構(AMED)戦略推進部 がん研究課