2020-03-31 京都大学
亀井謙一郎 物質-細胞統合システム拠点(iCeMS=アイセムス)准教授、Rodi Abdalkader 同特定助教は、微細加工技術を駆使して、ヒトの角膜構造を細胞培養系で再現するデバイスの開発に成功しました。
透明な組織である目の角膜が病気になると、濁るなどの視覚障害が起き、時には失明などの可能性があります。そのような病気を治療するために、点眼液などの治療薬が開発されていますが、ウサギなどの実験動物とは、ヒトへの効能や毒性が予想できませんでした。これは実験動物との種間差だけでなく、目のまばたきの頻度にも違いがあるためでした。
そこで本研究では、マイクロメートルほどの非常に小さいものを加工できる微細加工技術を応用した「マイクロ流体デバイス」に着目しました。このデバイスを用いることによって、ヒトの体の中における血管網や組織を再現することができます。このデバイスにヒト由来の角膜上皮細胞を培養し、更に、細胞培養液を行き来させることによって、まばたきも再現した「ヒト角膜モデル」の開発に成功しました。
本研究成果は、新しい角膜治療薬の開発に貢献できるだけでなく、動物代替法として、実験動物を削減することが期待されます。
本研究成果は、2020年3月11日に、国際学術誌「Lab on a Chip」のオンライン版に掲載されました。

図:本研究のイメージ図(イラスト:高宮泉水 iCeMS特定助教)
書誌情報
【DOI】 https://doi.org/10.1039/C9LC01256G
Rodi Abdalkadera and Ken-ichiro Kamei (2020). Multi-corneal barrier-on-a-chip to recapitulate eye blinking shear stress forces. Lab on a Chip
詳しい研究内容について
角膜・オン・チップの開発に成功~「まばたき」も再現~
・生体外ヒトモデル「角膜・オン・チッカの開発に成功
.まばたきの再現による人工角膜の高機能化
・多検体同時評価が可認に
京都大学物質-細胞統合システム拠点(iCeMS=アイセムス)の亀井謙一郎(かめい・けんいちろう)准教授、Rodi Abdalkader(ルディ・アブドアルカーディル)特定助教は、微細加工技術を駆使して、ヒトの角膜構造を細胞培養系で再現するデバイスの開発に成功しました。この研究結果は、点眼液開発や、それに必要な動物実験の代替法として期待されます。
透明な組織である目の角膜が病気になると、濁るなどの視覚障害が起き、時には失明などの可能性があります。そのような病気を治療するために、点眼液などの治療薬が開発されていますが、ウサギなどの実験動物とは、ヒトへの効能や毒性が予想できませんでした。これは実験動物との種間差だけでなく、目のまばたきの頻度にも違いがあるためでした。
そこで今回の研究では、マイクロメートルほどの非常に小さいものを加工できる微細加工技術を応用した「マイクロ流体デバイス※1」に着目しました。このデバイスを用いることによって、ヒトの体の中における血管網や組織を再現することができます。このデバイスにヒト由来の角膜上皮細胞を培養し、更に、細胞培養液を行き来させることによって、まばたきも再現した「ヒト角膜モデル」の開発に成功しました。
本研究で得られた成果は、新しい角膜治療薬の開発に貢献できるだけでなく、動物代替法として、実験動物を削減することが期待されます。
本成果は 2020 年 3 月 11 日に英科学誌「Lab on a Chip(ラボ・オン・チップ)」にオンラインで公開されました。
1.背景
私たちの生活には多くの「薬」があリ、健康に生活するためには欠かせないものとなっています。しかし、新しい薬の開発は重要な局面を迎えています:というのも、一つの新しい薬を開発するために、数百億円以上の巨額の費用と10年以上の長い年月を必要とするからです。また、この薬品開発は全てが成功するわけではなく、非常に低い成功率も課題となっています。
その中でも目薬は、目の乾燥や充血の改善だけでなく、目の炎症や眼病などを治癒するために開発されています。目薬開発時には薬効・安全性・毒性評価などが行われますが、ウサギなどの実験動物を使用しているため、正確な評価ができませんでした。特にウサギの 「まばたき」は1時間に10~12回で す が 、 ヒトは1時間に10開回と大きな違いがあり、これが種間差の要因の一つとなっています。 そこで、ヒトの「目」を再現できる新しい試 験法の開発が急務となっています。
近年、培養系におけるヒトの臓器モデルとして、微細加工技術を基にしたマイクロ流体デバイスを用いた「Organ ona Chip(組織チップ)*2 が注目されています(図1)。これは、デバイス内に組織構造を模倣したモデルを作成する技術であり、従来の細胞培養プレートなどでは再現できなかった組織機能を発現することができます。2016年の世界経済フォーラムにおいても、次世代バッテリーや自動操縦車などと同様に「Top 10 Emerging Technologies」に選択されており、その重要性は増しています。
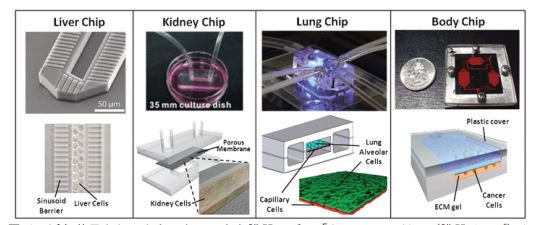
図 1 近年着目されるようになってきた臓器モデル「Organ on a Chip(臓器チップ)」
(出典:Huh et al., Lab Chip, 2012, 12, 2156)
2.研究内容と成果
そこで本研究では、角膜における薬剤透過試験や毒性試験を行うことが可能な生体外ヒトモデルを開発するために(図2)、ヒト角膜上皮細胞をマイク口流体デバイスに導入した新しい実験系、「角膜・オン・チップ」の開発に取り組みました(図3,4)。
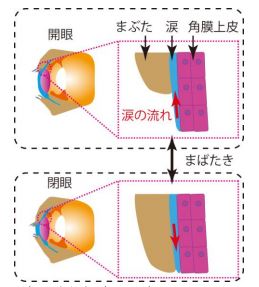
図 2 本研究で再現したヒト角膜構造とまばたき時の涙の動き
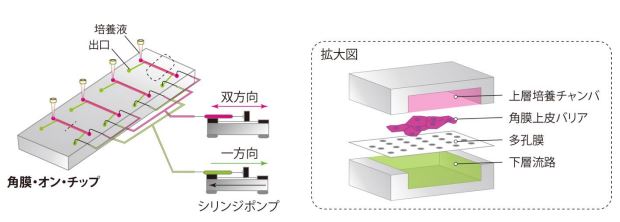
図 3 本研究で開発した「角膜・オン・チップ」の概念図

図 4 角膜・オン・チップ
私たちがこのチップを開発するにあたって、①薬剤の角膜上皮透過性試験、②まばたきによる角膜上皮細胞へのずリ応力*3印加、③ずリ応力による角膜上皮の高機能化、を目指しました。まず、このチップを構成する材料として、生体適合性が高く、ガス・光透過性も高いPolydimethylsiloxane(PDMS)*4 を使用しました。また、マイク口流体デバイス内に多孔膜を設置し、その上で角膜上皮細胞を培養することで、角膜上皮細胞による膜形成と薬剤透過性の評価を可能にしました。更に、まばたきにおけるずり応力を再現するために、双方向に駆動可能なシリンジポンプを使用しました。

図 5 角膜・オン・チップ内で培養した角膜上皮細胞における ZO-1 タンパク質(緑)の発現。角膜が機能するために ZO-1 が必要。従来法(トランスウェル)と比較しても、発現量の増加が確認できる。左図のスケールバーは 50 µm、右図のスケールバーは 100µm。
作成したチップ内で培養したヒト角膜上皮細胞IHC[-T)における膜機能としての評価を免疫細胞染色により確認しました(図5)。膜機能として必要なZO-1タンパク質が培養後7日目で強<発現していることが確認でき、また、従来のトランスウェルを用いた培養と比較しても、その発現が強くなることが確認できました。
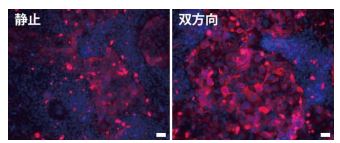
図 6 角膜・オン・チップ内で培養した角膜上皮細胞における CK-19 タンパク質(赤)の発現。角膜が成熟するために CK-19 が必要。静止培養と比較し、双方向のずり応力を印加すると、CK-19 の発現が増加していることが確認できる。スケールバーは 50 µm。
次に、双方向のずり応力が角膜上皮細胞の成熟化に与える影響について、免疫細胞染色により確認しました(図6)。角膜成熟化マーカーであるCK-19タンパク質が、双方向のずり応力を印加することによって、発現が強化されることが確認できました。
これらの結果から、本研究で開発した「角膜・オン・チップ」は、角膜をよリ機能的な状態で培養できることを確認しました。
3.今後の展開
本研究では、角膜構造だけでなくまばたきの動きも再現した生体外ヒトモデル「角膜・オン・チッカの開発に成功しました。このチップは、従来の動物実験では困難であった点眼液の薬効・安全性・毒性のヒトへの影響を予測する新規方法として期待されます。
また、動物実験代替法としても期待でき、実験動物の削減にも繋がリます。近年、世界中において動物愛護・倫理的な観点から実験動物の使用を抑制、場合によっては禁止、という動きになっています。例えばEUでは、化粧品開発時における実験動物の使用は既に禁止されています。本研究のように、実験動物を使用せず、ヒトのモデル化を可能とする技術の開発が熱望されています。
4.用語解説
※1マイク□流体釣くイス:微細加工技術を応用して作製されたデバイス。化学物質の合成や分離などで利用されるだけでなく、微小空間における物理現象を研究するためにも使用される。近年では、極微量のサンプルなどから遺伝子増幅・解析が可能なデバイスなども開発されている。
※2組織チップ:マイク口流体デバイスを基に、生体外における組織の再構築と生理機能の再現を目的としたチップ。創薬への応用が期待されている。
※3ずリ応力:立体のある一面に平行にすべらせるようにかかる応力のこと。
※4Po-yd.methyl引oxane(PDMs):マイク口流体デノくイスを作成するために使用されるシリコンゴム材料:ガス透過性、光透過性に優れ、生体適合性にもあるため、細胞培養実験基材に良く使用される。
5.研究ブ口ジェクトについて
本研究は、日本学術振興会科学研究費補助金(基盤研究(凶研究代表亀井謙一郎、課題番号17HO208り、及び日本医療研究開発機構く課題番号1793766力の支援を受けて行われました。
6.論文タイトル・著者
”Multi-corneal barriers-on-a-chip to recapitulate eye blinking shear stress forces”
(参考訳:目のまばたきによるずり応力も再現したマルチ・角膜・オン・チップ)
著者:Rodi Abdalkader and Ken-ichiro Kamei
Lab on a Chip DOI: 10.1039/C9LC01256G