2018-05-22 国立循環器病研究センター,大阪大学,洛和会音羽病院
国立循環器病研究センター(大阪府吹田市、理事長:小川久雄、略称:国循)研究所分子病態部の柳本広二疾患分子研究室長、画像診断医学部の飯田秀博元部長、病院脳神経外科の高橋淳部長らの研究グループは、独自に開発したマウス脳梗塞モデルと最新の7テスラ小動物用MRIを用いて、これまでで最も早期に虚血性脳卒中(注1)発症後の不可逆的組織変化(脳組織が壊死した箇所)の検出に成功しました。本研究は、大阪大学医学部および洛和会音羽病院との共同研究の成果として、専門誌「Molecular Neurobiology」に2018年5月22日に掲載されました。
背景
脳梗塞は発症すると後遺症が残る可能性が高く、最重度の要介護5の原因疾患の第1位です(厚生労働省「平成28年国民生活基礎調査」より)。死亡の回避や後遺症の軽減のためには、発症後早期に血管の詰まりを解消し血流を再開させること(再灌流療法)が必要です。現在わが国で承認されている再灌流療法には、血栓を溶かすアルテプラーゼ静注療法(以下「t-PA静注療法」)と特殊な機器で血栓を取り除く血管内治療があります。
t-PA静注療法により急激に血流量が増加することから、脳組織が壊死してしまうと傷ついた血管から出血するリスクが高まります。現在のところ脳組織の壊死を早期に検出する画像診断法は確立されていないことから、t-PA使用基準は過去の臨床経験から全世界一律で「虚血性脳卒中発症後4.5時間以内」(以下「本基準」)とされています。
本基準は最重症の症例から類推したものですが、脳組織の壊死が始まっているかどうかを正確に判断する方法があればより安全かつ積極的にt-PA使用が可能になると考えられ、脳組織の壊死の出現を早期に察知できる新たな画像診断法の確立が望まれています。
研究手法と成果
急性期脳梗塞の画像診断にはMRI(注2)が用いられます。MRIは条件を変えることで様々な画像を撮影することが可能になります。柳本室長らのグループは、新たに開発した計算手法を「Essential Diffusion Coefficient: EDC法」と名付け、従来の撮影方法であるT2強調画像(注3)やADCマップ(注4)の画像と比較しました。MRIの指標として臨床の場で用いられているADCとは、「見かけの拡散係数」との意味を持ち、新たに開発したEDCは、「本質的な拡散係数」の意味を持ちます。EDCは、細胞外に生じる血管性浮腫の影響をさらに排除した、より純粋な細胞性変化の指標です。撮影対象は国循が独自に開発した脳梗塞モデルマウス「3-VO(注5)」で、虚血性脳卒中発生直後より10時間連続撮像を行い、その間に得られた様々な脳領域でのMRIシグナル変化を、発症から24時間後に取りだした3-VOマウスの脳の組織診断の結果と比較しました(図1)。
その結果、T2強調画像やADCマップなど従来の撮影・計算方法では脳組織の壊死の始まり(不可逆的となった組織の変化)を捉えることができませんでしたが、EDC法では虚血発症後5時間15分後に虚血状態の強い箇所における急激な細胞性浮腫の増強を捉えることができました。(図2)虚血状態発症から24時間後に取りだした脳と比較すると、顕著な細胞性浮腫(MRI/EDC所見)を示した部分と壊死が発生した部分は一致していました。また、発症から壊死が開始するまでの時間も、t-PAの使用限度である4.5時間を超え、6時間後までに行われた、「遅れたt-PA静注療法」が、出血性合併症を適正使用の場合の2倍以上に増加させるとの臨床経験から得られた事実に一致していました。以上のことから、EDC法により壊死の有無や発生の瞬間を高精度に判断できることが明らかになりました。
今後の展望・課題
今回開発および精度の検証を行ったEDC法では、問診による推定発症時刻よりも実際の発症時刻が早く、推定発症時刻から4.5時間以内であってもt-PA静注療法の適用で出血リスクが高まるケースや、虚血の程度が軽く脳組織の傷害が見られないケースなどを正確に判別できます。これにより、t-PA静注療法の適用について患者ごとのより柔軟な治療方針決定に寄与できると期待されます。EDC法は現在あるMRIの機器で応用可能であるため、今後は企業との共同研究を呼び掛け、全てのMRIで簡易にEDC値を求めることのできるマッピングソフトの開発および実臨床での精度の確認を目指します。
(注1)虚血性脳卒中
脳血管の狭窄や血栓の生成等により、脳の血流が途絶えて(虚血)身体症状の現れる状態のこと。この状態を経て脳組織が死に至り、壊死(CT検査や組織診断で確定できる不可逆的な組織損傷)が生じると「脳梗塞」と診断される。不可逆的な組織損傷が生じると、t-PA静注療法後の出血性合併症が生じやすくなる。
(注2)MRI(Magnetic Resonance Imaging:磁気共鳴画像)
強い磁力をあてることでヒトの体内の分子の並び方が微妙に変化することを利用した、画像診断の方法。分子の変化をコンピューターで計算し、画像化(断層写真)する。
(注3)T2強調画像
水、脂肪組織、液性成分、嚢胞などは白く、腫瘍はやや白く、脳は灰色に見える画像。脳卒中の画像診断においては、脳組織の壊死が起こる時には水が細胞の内外にたまる現象が起こるが、そのうち細胞の外に移動した水(血管性浮腫)を確認するために用いる。
(注4)拡散強調画像(DWI)
水の拡散運動を画像化したもの。臨床では、虚血性脳卒中の「急性期、虚血性変化」の指標。この撮像法の開発によって虚血性脳卒中急性期の診断力が飛躍的に向上した。ただし、「虚血性変化(DWIで白くなる部位)」の組織学的意義は様々で、血管性浮腫、細胞性浮腫の他、温度、イオン勾配(粘度)等の影響を受けることが知られている。また、本検査法による陽性結果は一過性に終わることもある。
(注5)ADCマッピング(ADCとは、見かけ上の拡散係数、の意味)
(注4)とは異なり、DWIに基づいた(ADCと呼ばれる)計算結果をイメージ化した画像。血管性浮腫の要素を含むT2(横緩和時間)の影響を排除しているため、細胞性浮腫への特異性がDWIよりも高まっている。ただし、画像上での明と暗が細胞性浮腫と相反する血管性浮腫の影響は依然受けており、虚血性脳卒中の急性期に得られる陽性結果が、その後に消失することがあり、これを用いた脳梗塞の早期診断法は確立していない。
(注6)3-VO(3血管閉塞)マウス
他の脳梗塞の病態再現モデルで多く見られる「発症後の死亡率」が極めて低く、大小ばらつきの少ない皮質型脳梗塞を全例に出現させることを可能としたオリジナルモデル。脳皮質内の側副血行(血管吻合)によって、臨床上最も問題となる、積極的な治療が可能な「中等度の虚血レベル(ペナンブラ領域)」が確実に含まれる。以下のサイトから、3-VOマウスの顕微鏡下手術動画を確認できる。
下は上のQRコードです。

(図1)撮影した画像と実際の脳の状態の比較
発症24時間後のマウス脳の断面(左画像)では、壊死した部分は白く、壊死を免れた部分は赤くなっている。右画像は虚血性ストレス後の急性期に撮られたT2信号強調画像(血管性浮腫の部位が白く描出されている)。
左に示した発症24時間後の脳を用いた組織学的診断によって、以下のことが確認され、それによって各ROIが定義された。
1(ROI-1)は、虚血性ストレスが最も強く、虚血発症直後に殆どの細胞が死滅する領域
2(ROI-2)は、虚血性ストレスが中等度で、24時間以内に大多数の細胞が死滅する領域。
3(ROI-3)は、虚血性ストレスが軽度で、24時間後には大多数の細胞が生存する領域。
4(ROI-4)は、虚血性ストレスがかからなかった、無傷の領域。
※ROI(関心領域)測定法:特定の解剖学的部位に特化した分析方法。

(図2)局所脳虚血発症後急性期の、脳の各領域の組織生存率とEDCとの関係
壊死した、もしくは壊死に向かう領域(ROI-1,2:▼:虚血性ストレスが強く、死後の壊死性変化に向かう細胞の多い領域)のEDCは、虚血発症5.25時間後に殆ど壊死のない領域(ROI-3:○:虚血性ストレスが軽く、細胞死を免れる細胞の多い領域)に比べて急激に低下し、以降は低値持続となる。この組織生存率が急激に低下するタイミング・場所で脳組織の壊死が起こったと考えられる。
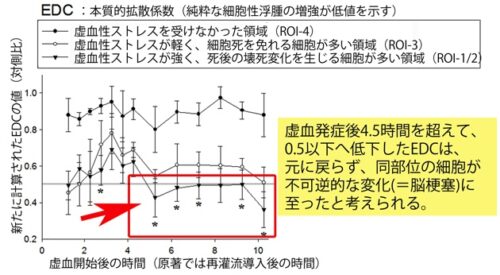
注:壊死とは死後の細胞崩壊であり、虚血によって生じた壊死組織の検出によって、初めて脳梗塞と診断されます。細胞膜が脆弱となり、壊れやすくなった壊死組織が生じた後のt-PA静注療法の導入は、出血性合併症の危険性が高まること(脳出血のリスクが3%から7%へ急増する)が知られていますが、現状では急性期の壊死性変化を、それが生じた時点で捉えることができず、従って、t-PA静注療法の導入が一律に4.5時間以内と定められています。しかしながら、本基準を過ぎても尚、壊死組織が生じていない、従って、t-PA静注療法を比較的安全に導入できる症例が存在する、と考えられています。