2021-06-25 京都大学iPS細胞研究所
ポイント
- ブラウ症候群患者さんのマクロファージでは、IFNγ刺激依存的な自己炎症反応が起きることを示した。
- 抗TNF抗体治療によりこの異常が改善されることを明らかにした。
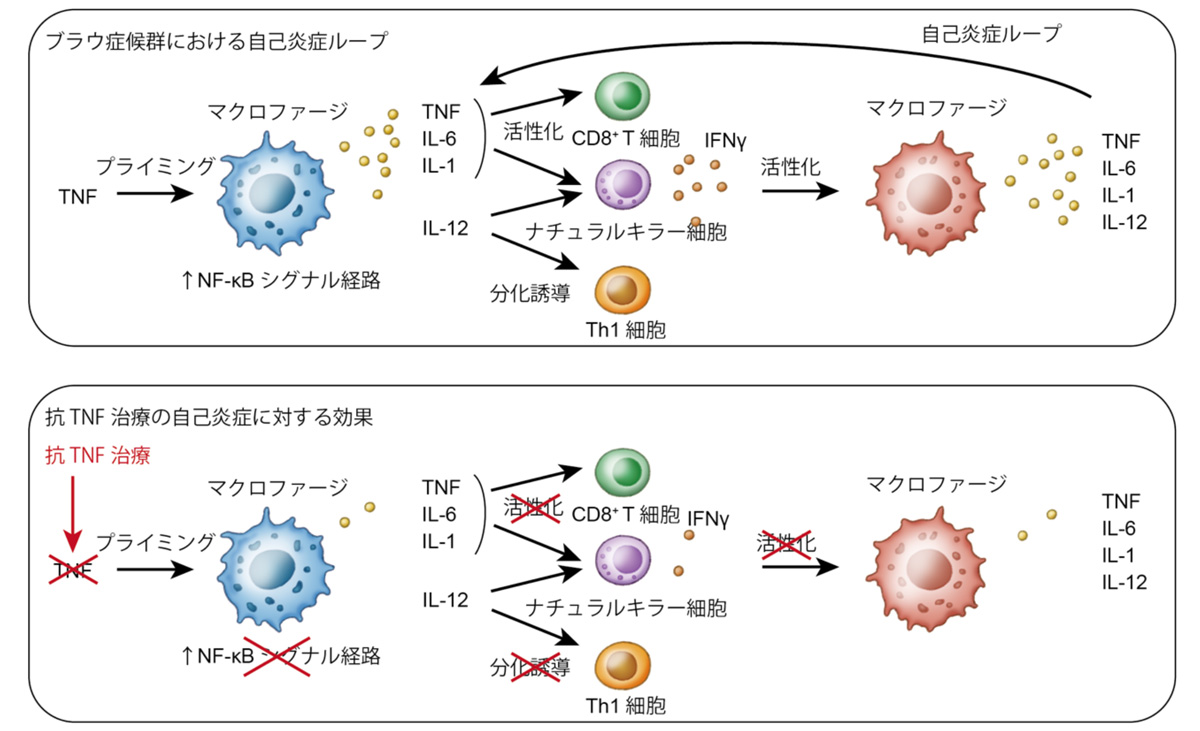
図1:ブラウ症候群における自己炎症反応の概要及び抗TNF治療の効果
1. 要旨
北川瑶子研究員(CiRA臨床応用研究部門)、川崎ゆり研究員(CiRA臨床応用研究部門)、齋藤潤准教授(CiRA臨床応用研究部門)らの研究グループは、ブラウ症候群患者さんの末梢リンパ球およびヒトiPS細胞を用いて、自己炎症反応注1)が起きるメカニズム及び抗TNF抗体治療の有効性を明らかにしました。
この研究は、鹿児島大学病院、関西医科大学、京都大学大学院医学研究科及びCiRA齋藤潤研究室の共同研究の成果です。
この研究成果は2021年6月25日に米国科学誌「Journal of Allergy and Clinical Immunology」にオンライン公開されました。
2. 研究の背景
指定難病であるブラウ症候群は、NOD2遺伝子の変異により引き起こされる単発性の自己炎症性疾患です。 典型的な患者さんでは、4歳までに皮膚病変が発症し、その後、眼や関節にも病変が現れます。 これらの病変が進行すると、失明や関節拘縮などの重篤な合併症を引き起こし、患者さんの生活の質を著しく悪化させることになります。 ブラウ症候群の治療法として、これまで副腎皮質ステロイドなどの非特異的な免疫抑制療法が使われてきましたが、その効果は限定的であり、重篤な合併症のリスクも生じます。 近年、TNF、IL-6、IL-1などのサイトカイン注2)を標的とした抗体治療が試されており、特に抗TNF抗体は長期的な有効性が報告されています。 しかし、その薬理学的メカニズムは不明であり、細胞表現型を調べ、有効性を評価する必要がありました。
そこで、齋藤潤研究グループはブラウ症候群患者さんのマクロファージにおける表現型異常を定義し、抗TNF治療によりこの異常が修正されるかを検証しました。
3. 研究結果
CiRA齋藤潤研究室では、以前にブラウ症候群患者さんのiPS細胞から誘導したミエロイド細胞株を用いて、IFNγ注3)刺激がブラウ症候群で観察される炎症性サイトカインの過剰産生に寄与することを明らかにしました(CiRAニュース 2017年6月5日)。 この研究に引き続き、本研究ではブラウ症候群患者さんの末梢血単球に由来するマクロファージの特徴を調べました。その結果、未治療のブラウ症候群患者さん由来のマクロファージでは、IFNγ刺激がサイトカインの異常発現の前提条件であることを確認しました。また、未刺激の状態ですでにNF-κBシグナル経路注4)が活性化していることがIFNγ刺激依存的なサイトカイン産生異常に寄与する可能性が考えられました。
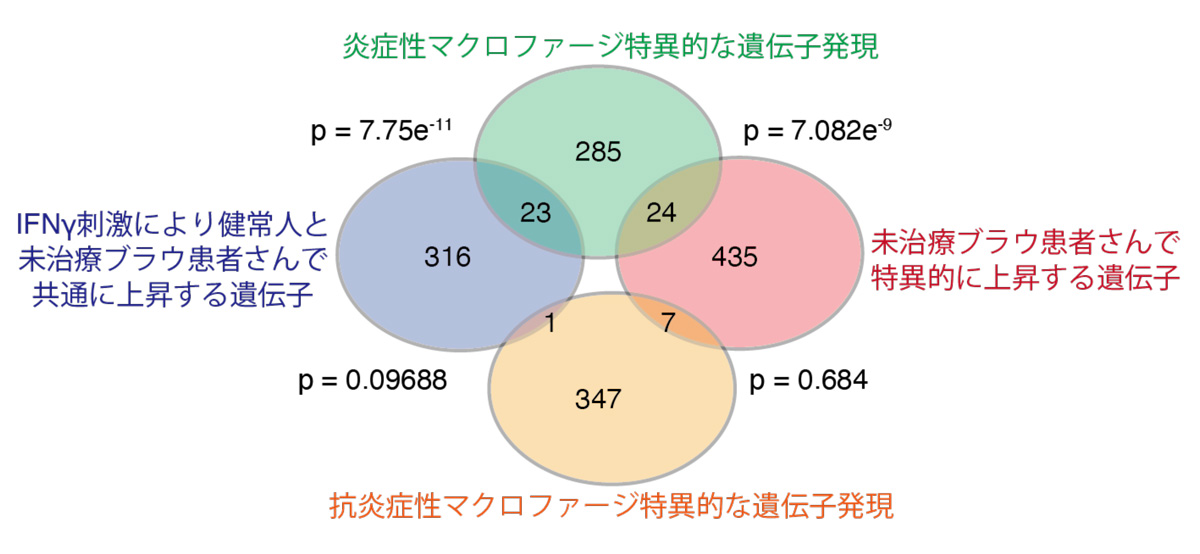
図2:IFNγ刺激により発現上昇する遺伝子と炎症性マクロファージ特異的に発現する遺伝子の重複
一方、抗TNF治療により、上記のブラウ症候群に伴う異常が修正されることが明らかになりました。トランスクリプトーム解析注5)では、抗TNF治療を受けたブラウ症候群患者さんのマクロファージは健常人由来のマクロファージと似たプロファイルを示しました。
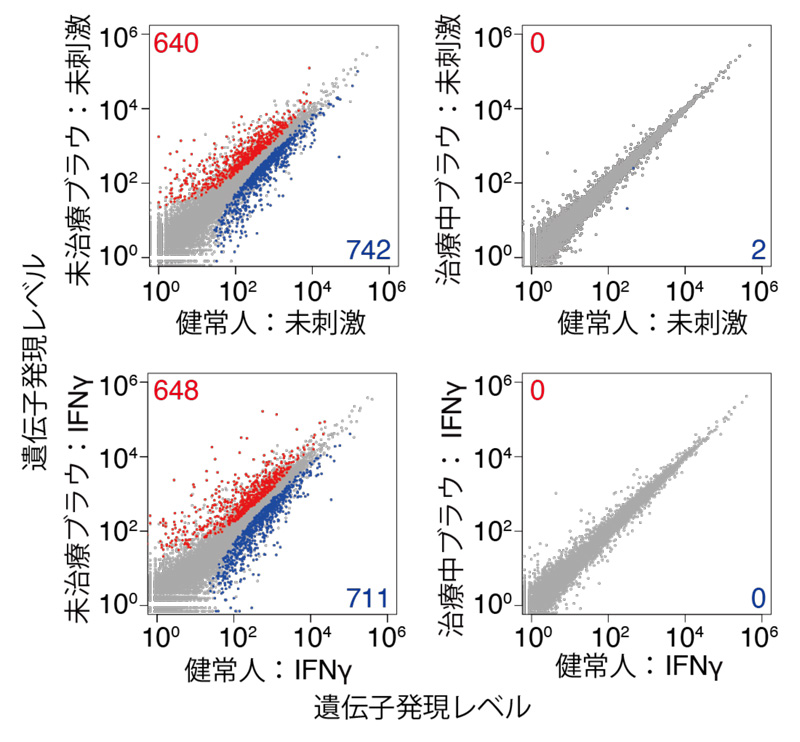
図3:健常人、未治療のブラウ症候群患者さん、抗TNF治療を受けたブラウ症候群患者さんのマクロファージのトランスクリプトーム比較
赤と青の数字は、二つの群間で発現量が異なる遺伝子の数を示す。
さらに、同一の環境下で分化させたマクロファージのプロファイルを比較するため、健常人及びブラウ患者さん由来iPS細胞からマクロファージを分化させ、表現型を調べたところ、IFNγ依存的なサイトカイン産生異常が認められました。そこで、未治療、治療中の患者さん末梢血由来マクロファージとiPS細胞由来マクロファージの遺伝子を比較したところ、どちらもIFNγ刺激に対して類似した応答を示すことがわかりました(図4)。さらに解析を進めると、IFNγ刺激に対して過剰なサイトカイン産生が起こる場合には共通して、刺激前にNF-κBシグナル経路が活性化していることがわかりました。これらの結果により、マクロファージがTNFなどの炎症性サイトカインに事前にさらされ、NF-κBシグナル経路が活性化することが、ブラウ症候群の症状を引き起こす一つの要因であると考えられます
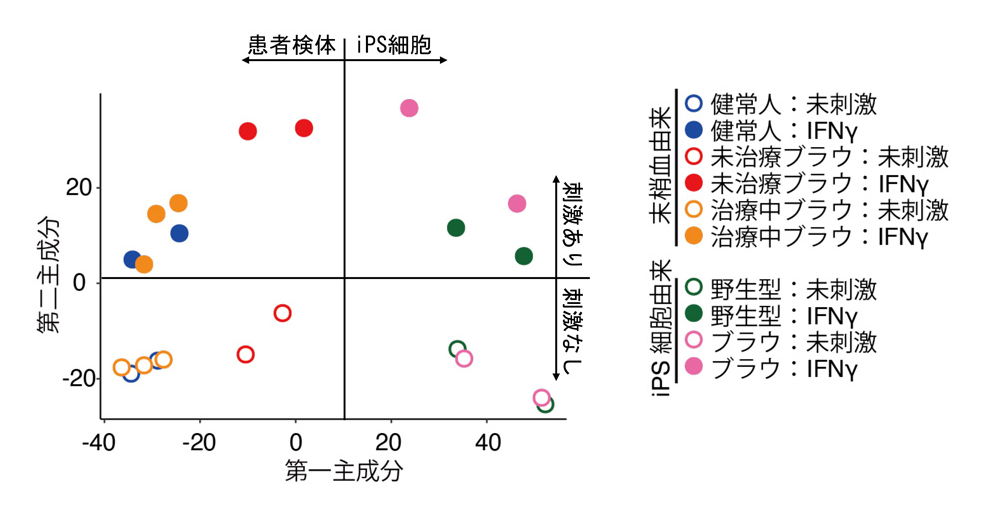
図4:末梢血由来マクロファージとiPS細胞由来マクロファージにおける遺伝子発現の主成分解析
遺伝子発現のばらつきを、グラフで表したもの。患者検体、iPS細胞ともに、IFNγ刺激を加えると、遺伝子発現が第二主成分方向に変動している。
4. まとめ
本研究では、ブラウ症候群患者さんの末梢血由来マクロファージ及び疾患特異的iPS細胞を用い、自己炎症反応の誘導にNF-κBシグナル経路の活性化とIFNγ刺激が重要であることを示しました。また、近年有効な治療法として使用されている抗TNF抗体は、マクロファージにおけるNF-κBシグナル経路の活性化を抑えることで、炎症反応を惹起するいき値を下げ、IFNγ刺激存在下でも自己炎症ループの誘導を防ぐと考えられました。本研究により、ブラウ症候群の自己炎症のメカニズムの深い理解が可能になったほか、抗TNF療法の妥当性を証明することが出来ました。従って、この成果は、ブラウ症候群の治療法選択や今後の新規治療薬開発に役立つと期待されます。
5. 論文名と著者
- 論文名
Anti-TNF treatment corrects IFNγ-dependent proinflammatory signatures in Blau syndrome patient-derived macrophages - ジャーナル名
Journal of Allergy and Clinical Immunology - 著者
Yohko Kitagawa1*, Yuri Kawasaki1*, Yuichi Yamasaki2, Naotomo Kambe3,4, Syuji Takei2, and Megumu K. Saito1†
*共同第一著者
†責任著者 - 著者の所属機関
- 京都大学iPS細胞研究所臨床応用研究部門
- 鹿児島大学病院小児科
- 関西医科大学皮膚科
- 京都大学大学院医学研究科皮膚科学
6. 本研究への支援
本研究は、下記機関より資金的支援を受けて実施されました。
- AMED再生医療実現ネットワークプログラム
- AMED疾患特異的iPS細胞の利活用促進・難病研究加速プログラム
- AMED難治性疾患実用化研究事業
- 日本学術振興会 科学研究費 特別研究員奨励費
- 日本学術振興会 科学研究費 基盤C
7. 用語説明
注1)自己炎症反応
外来病原体からの刺激がない状態で起こる炎症反応。通常、免疫システムは外来病原体に反応して炎症を起こすことで病原体を排除するが、何らかの異常で自己の体内物質に反応したり、ブラウ症候群のように遺伝子変異のため刺激がない状態で炎症が起ったりすることがある。
注2)サイトカイン
免疫細胞が出す液性因子。他の免疫細胞を活性化させ、炎症を増強する働きを持つものもある。
注3)IFNγ
炎症性サイトカインの一種。主にリンパ球から産生され、マクロファージを活性化させる。
注4)NF-κBシグナル経路
炎症反応を誘導するシグナル経路の一種。マクロファージにおいてはTNFなどの炎症性サイトカインの産生に関与する。
注5)トランスクリプトーム解析
細胞内の遺伝子の発現状況を網羅的に把握するための分子解析。