微量試料計測で凝集たんぱく質の分子構造の違いを同定可能に
2021-07-27 東京工業大学,理化学研究所,科学技術振興機構
ポイント
- アルツハイマー病の主原因の1つとされる、42残基のアミロイドβたんぱく質(Aβ42)凝集体の分子構造の違いを高感度で検出する固体NMR計測法を開発
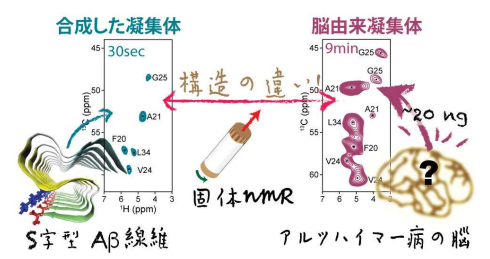
- 固体NMRスペクトルを分子指紋として使い、極微量の脳由来Aβ42凝集体と、試験管で作成したAβ42凝集体から両者の分子構造が異なることを確認
- アルツハイマー患者由来のAβ42凝集体に対する構造のスクリーニングや、抗体医薬への応用を期待
東京工業大学 生命理工学院 生命理工学系の石井 佳誉 教授(理化学研究所(理研) 生命機能科学研究(BDR)センター兼任)と理研BDRの山崎俊夫ユニットリーダー、小林 直宏 上級研究員らの国際共同研究グループは、アルツハイマー病の主原因の1つとされる42残基のアミロイドβたんぱく質(Aβ42)凝集体について、高磁場固体NMR法を用いて分子構造の違いを高感度で検出する方法を開発した。
これまでの研究で、試験管内で作成した繊維状Aβ42凝集体の構造は知られているものの、アルツハイマー病患者の脳内に蓄積する繊維状Aβ42凝集体の実際の構造はよく分かっていなかった。今回、国際共同研究グループは、アルツハイマー病患者の脳より得られた微量の凝集体試料を増幅することで、高磁場固体NMR法のスペクトル解析を短時間かつ高感度で行うことに成功した。このNMRスペクトルを分子指紋として使った比較により、脳由来の試料は、人工の繊維状Aβ42凝集体とは構造が大きく異なることを明らかにした。これは、脳由来のAβ42凝集体の分子構造が、試験管内で作成したAβ42凝集体の標準的な分子構造とは全く異なることを示す有力な証拠だといえる。
この成果から、アルツハイマー患者に由来するAβ42凝集体の分子構造のスクリーニングにNMR法を用いることが可能であり、それが脳内のAβ42凝集体の構造と機能の理解につながると期待できる。また将来的には、脳内のAβ42凝集体の3次構造決定や、抗体医薬の結合部位の同定などへの応用も考えられる。この高感度固体NMR法は現在JST 未来社会創造事業で開発中の1.3GHz超高磁場NMR装置の先端利用技術として開発された計測法であり、本装置と組み合わせることで、解析感度をさらに大幅に上げることも可能となる。
本研究は、米国化学会誌「Journal of the American Chemical Society」のオンライン版に近日中に掲載される。
本研究は、科学技術振興機構(JST) 未来社会創造事業 大規模プロジェクト型「高温超電導線材接合技術の超高磁場NMRと鉄道き電線への社会実装(研究代表者:前田 秀明)」、科学研究費助成事業(学術研究助成基金助成金) 国際共同研究加速基金(帰国発展研究)「次世代の高磁場生体固体NMR法の開発とアミロイドとリガンド相互作用の構造生物学(研究代表者:石井 佳誉)」、米国National Institutes of Health(NIH、国立衛生研究所), NIGMS U01 Grant「Structures and Propagation of Pathologically Relevant Amyloids in Alzheimer’s(研究代表者:石井佳誉)」、NIH, NIA R01 Grantと Alzheimer’s Association Zenith Fellows Award(研究代表者:S. C. Meredith)およびNIH, NIGMS T32 Training Grant(研究代表者:M. R. Clark)による支援を受けて行われた。
<論文タイトル>
- “Sensitivity-Enhanced Solid-state NMR Detection of Structural Differences and Unique Polymorphs in Pico- to Nanomolar Amounts of Brain-derived and Synthetic 42-residue Amyloid-b Fibrils”
- DOI:10.1021/jacs.1c03346
<お問い合わせ先>
<研究に関すること>
石井 佳誉(イシイ ヨシタカ)
東京工業大学 生命理工学院 生命理工学系 教授
山崎 俊夫(ヤマザキ トシオ)
理化学研究所 生命機能科学研究センター 構造NMR技術研究ユニット ユニットリーダー
小林 直宏(コバヤシ ナオヒロ)
理化学研究所 生命機能科学研究センター 先端NMR開発・応用研究チーム 上級研究員
<報道担当>
東京工業大学 総務部 広報課
理化学研究所 広報室 報道担当
科学技術振興機構 広報課