2021-11-29 大阪大学
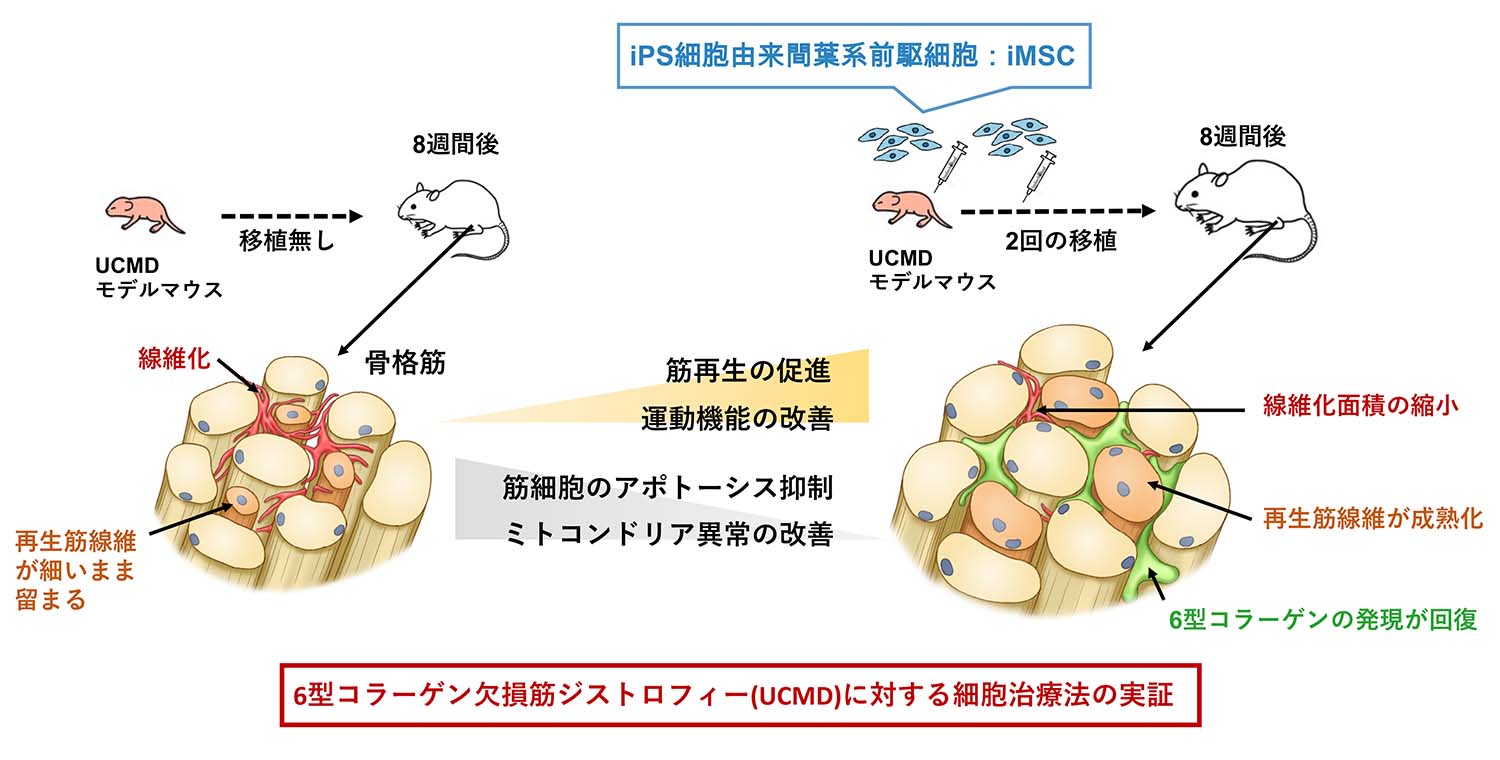
 図:アルファ線治療薬アスタチン(TAH-1005)を用いた治療のイメージ
図:アルファ線治療薬アスタチン(TAH-1005)を用いた治療のイメージ
研究成果のポイント
- 治療効果の高いアルファ線を体内から照射する新たながん治療薬(アスタチン※1)の安定製造に成功
- 従来の治療では効果不十分である難治性の甲状腺がん患者を対象とした医師主導治験を開始
- 外来での注射1回で高い治療効果が得られ、負担の少ない革新的治療になることが期待される
概要
大阪大学 大学院医学系研究科の渡部直史助教(核医学)らの研究グループは、難治性分化型甲状腺がんに対するアスタチン化ナトリウム([211At]NaAt)注射液の医師主導治験※2を開始します。
これまで、主に放射性ヨウ素(131I)※3を用いたベータ線治療が行われてきましたが、多くの転移を伴う患者さんでは十分な治療効果が得られないことがありました。一方、アスタチンはヨウ素によく似た性質を示す元素であるとともに、アルファ線と呼ばれるエネルギーの高い放射線を放出するため、より高い治療効果が期待されます。研究グループはこれまでの非臨床試験において、アスタチン化ナトリウム([211At]NaAt)注射液(治験成分記号:TAH-1005)の有効性と安全性を十分に検証しました。そのうえで、理化学研究所RIビームファクトリーで製造したアスタチン(原料)をもとに、大阪大学医学部附属病院において治験薬としての安定製造(院内製造)に成功しました。
この度、同病院の治験審査委員会等の承認、医薬品医療機器総合機構(PMDA) ※4の治験計画届出調査を経て、患者さんに対する医師主導治験を開始できることになりました。今後、治験の中でアルファ線治療薬アスタチンの安全性や薬物動態を確認すると共に、医薬品としての実用化を目指して、有効性の検証を行っていきます。
治験実施までの背景
甲状腺がんの多くが分化型甲状腺がん※6と呼ばれ、ベータ線を放出するヨウ素を取り込む性質を有しています。現在、分化型甲状腺がんの多発転移に対する治療では、専用の病室に入院して、放射性ヨウ素(131I)を用いたベータ線治療が実施されています。しかし、繰り返しの治療を行っても十分な治療効果が得られない場合があること、医療機関にとってコストや人材面から専用病室の維持が難しいという問題がありました。また、放射性ヨウ素(131I)は周囲の被ばくを避けるために専用病室には1人で入院する必要がありますが、最近は介助が必要なご高齢の患者さんも増えていることから、外来で安全に実施可能な治療法が求められていました。アスタチンから放出されるアルファ線は飛距離が短く体外に出ないことから、外来治療として実施可能であることを厚生労働省の科学研究班において検証し、既に日本核医学会の承認が得られています。
大阪大学では、医薬品としての実用化を目指し、多くの分野が連携して、アスタチンに関する多くの前臨床研究を実施してきました。既に非臨床研究において、アスタチン(211At)が従来の放射性ヨウ素(131I)に比べて、大きな治療効果を持っていることが示されています。また治験開始にあたっては、PMDAとの対面助言に基づいて、甲状腺がんの治療薬としての安全性を確認するための毒性評価試験を実施し、治験開始の準備を進めてきました。さらに大阪大学医学部附属病院 核医学診療科内の治験薬GMP(Good Manufacturing Practice)※7製造施設において、アルファ線治療薬アスタチンを治験薬として安定的に製造する体制を確立し、2021年8月に院内短寿命放射性薬剤安全管理委員会での承認を得ました。一方、アスタチンは短寿命であるため、原料の国内製造が必須です。理化学研究所では、重イオン加速器施設「RIビームファクトリー」の加速器(サイクロトロン)※8を用いて、治験に必要とされるアスタチンを大量製造する技術開発を行い、大阪大学医学部附属病院へのアスタチン原料の安定供給を実現しました。
治験の概要
本医師主導治験は、放射性ヨウ素(131I)等の標準治療にて十分な治療効果が得られない難治性の分化型甲状腺がん患者を対象として、アルファ線治療薬アスタチンを投与した後の安全性、薬物動態、有効性を確認するための第Ⅰ相治験になります。今回、TAH-1005は世界で初めてヒトに投与されます。抗がん剤の治験であることから、患者さんを対象に低用量から開始して、徐々に用量を増量していくデザインとなっています。2021年11月から2024年3月までの間で実施され、予定症例数は最大16例です。
本研究が社会に与える影響・意義
本治験を含めてアスタチンの開発が順調に進み、アルファ線治療薬アスタチン(TAH-1005)が医薬品として承認された際には患者さん、医療機関の双方にとって負担の少ない外来治療となることが見込まれます。また、アスタチンは様々な分子や抗体に標識することが可能であり、今後様々ながん種に対する治療薬としての展開が期待されます。さらにアスタチンの製造には加速器(サイクロトロン)が必要となりますが、標的アルファ線がん治療に使えることが実証されれば、加速器技術のさらなる発展も期待されます。
治験責任医師のコメント
<渡部直史助教>
アスタチンを用いた非臨床研究の成果が得られた後、1日でも早く治療薬として患者さんに届けたいという思いで、治験の準備を進めて参りました。これまで本当に多くの関係者の皆様から多大なるご支援を頂いたことで、無事に治験開始まで至ることができました。この場を借りて、心より感謝を申し上げたいと思います。またここからが本当のスタート地点でもありますので、治験の実施にあたっては患者さんの安全面に十分に配慮しつつ、順調に進むように引き続き尽力したいと思います。
用語説明
※1 アスタチン
元素記号:At。211Atはアルファ線(α線)を放出する放射性同位体であり、加速器を用いて製造される(半減期 7.2時間)。ヨウ素とよく似た性質を示し、分化型甲状腺がんに集積する。
※2 医師主導治験
国から医薬品として認めてもらうために、安全性と有効性を確認する試験を「治験」といい、医師自ら企画・立案して行う治験のことを「医師主導治験」という。
※3 放射性ヨウ素(131I)
ベータ線(β線)と呼ばれる放射線を放出するヨウ素の放射性同位体であり、保険診療で甲状腺がんや甲状腺機能亢進症の治療に用いられている(半減期 8日)。高用量の治療では専用の病室に入院が必要となるが、全国的に治療病室が不足している。
※4 医薬品医療機器総合機構(PMDA)
医薬品の品質、有効性および安全性について、治験開始前の相談から承認までを一貫した体制で指導・審査する独立行政法人。
※5 NaIシンポーター
ナトリウム/ヨウ素共輸送体と呼ばれ、甲状腺や分化型甲状腺がんに存在し、細胞内にヨウ素を取り込む仕組みのこと。アスタチンもヨウ素と同じようにNaIシンポーターを介して、取り込まれる。
※6 分化型甲状腺がん
甲状腺がんの中でも正常の甲状腺細胞と同様にヨウ素を取り込む性質を有するがんであり、乳頭がん、濾胞がんなどを指す。
※7 治験薬GMP(Good Manufacturing Practice)
治験薬を製造する際に遵守すべき製造・品質管理の方法や構造設備に関する条件について、国が定めた基準。
※8 加速器(サイクロトロン)
プラスの電荷を持った粒子を電磁力で秒速4万kmまで加速させ、ターゲットに照射することで、新たな原子を製造する装置。
特記事項
アスタチンの非臨床研究は、科学技術振興機構(JST)産学共創プラットフォーム共同研究推進プログラム(OPERA QiSS)の一環として、大阪大学核物理研究センター(センター長:中野貴志)、同放射線科学基盤機構(機構長:小川哲生)、同理学研究科(研究科長:深瀬浩一)の協力を得て、実施されました。また、非臨床試験は日本医療研究開発機構(AMED)創薬支援推進事業・創薬総合支援事業(創薬ブースター)、治験の準備は、AMED橋渡し研究事業(preC・大阪大学拠点)、AMED臨床研究・治験推進研究事業(Step1)の支援を受けて進められました。2021-2023年度はAMED臨床研究・治験推進研究事業(Step2)の支援を受けて、治験を実施します。さらに、治験薬の製造にあたっては、理化学研究所 仁科加速器科学研究センター(センター長:櫻井博儀)の重イオン加速器施設「RIビームファクトリー」のAVFサイクロトロンを用いて、アスタチン(原料)の大量生成を行い(製造担当:羽場宏光、王洋、殷小杰、南部明弘、重河優大、佐藤望)、その供給を受けた上で、院内製造を行っています(担当:仲定宏、大江一弘、白神宜史)。
本治験は大阪大学医学部附属病院 核医学診療科(科長:加藤弘樹)において、糖尿病・内分泌・代謝内科(科長:下村伊一郎)、耳鼻咽喉科・頭頸部外科(科長:猪原秀典)、乳腺・内分泌外科(科長:島津研三)、放射線部(部長:富山憲幸)の協力の下で、未来医療開発部からの支援を受けて、実施されます。
本件について、11月29日に大阪大学(吹田キャンパス)およびオンライン同時配信にて記者発表を行いました。