2021-12-02 東京大学
発表者
- 酒井 寿郎
- (東京大学先端科学技術研究センター 代謝医学分野 教授/東北大学大学院医学系研究科 分子代謝生理学分野 教授)
- 松村 欣宏
- (東京大学先端科学技術研究センター 代謝医学分野 准教授)
2.発表のポイント
- 体の中には脂肪細胞になる前の前駆脂肪細胞が存在し、前駆脂肪細胞から脂肪細胞が「できる・できない」を決めるエピゲノム(注1)の仕組みを解明しました。
- タンパク質複合体(注2)の「いつ・どこに・どのように」あるかが、脂肪を蓄える遺伝子の働きを調節していることが明らかとなりました。
- 本研究成果は生活習慣病の予防や新規治療法につながることが期待されます。
3.発表概要
脂肪組織の中にある白色脂肪細胞(注3)は栄養分を脂肪として蓄え、空腹時にはこれを分解して栄養分を血液中に供給することで飢えから体を守るはたらきがあります。しかし栄養の過剰により摂取と消費のエネルギーバランスが崩れると肥満を発症します。脂肪組織の中には脂肪細胞になる以前の前駆脂肪細胞が存在します。栄養分を過剰に取ると、脂肪細胞は大きくなり、また前駆脂肪細胞から脂肪細胞ができます。遺伝子の発現は、ゲノム上の遠く離れた場所にあるエンハンサーと呼ばれる遺伝子制御部位によって調節されます。脂肪を蓄える遺伝子のエンハンサーは、前駆脂肪細胞では準備状態、脂肪細胞では活性化状態になっています。しかし、準備状態に止める仕組み、活性化状態に変化する仕組みは明らかではありませんでした。
東京大学先端科学技術研究センター/東北大学大学院医学系研究科の酒井寿郎教授、東京大学先端科学技術研究センターの松村欣宏准教授、東北大学大学院医学系研究科の伊藤亮助教、東京大学大学院医学系研究科の矢島あゆむ大学院生(研究当時)らの研究グループは、前駆脂肪細胞のエピゲノム・プロテオミクス解析(注4)を行い、新規のタンパク質複合体が「いつ・どこに・どのように」存在するかが、脂肪を蓄える遺伝子のエンハンサー(注5)の状態を決めることを解明しました。細胞分裂後期に、エンハンサー上で、タンパク質複合体の中の特定のタンパク質が分解されると、エンハンサーが準備状態から活性化状態に変わり、前駆脂肪細胞から脂肪細胞ができることがわかりました(図1)。
本研究成果は生活習慣病の予防や新規治療法につながることが期待されます。
本研究は、文部科学省 科学研究費 基盤研究「環境因子とエピゲノム記憶による生活習慣病発症の解明」、国立研究開発法人 日本医療研究開発機構 革新的先端研究開発支援事業(AMED-CREST)「健康・医療の向上に向けた早期ライフステージにおける生命現象の解明」研究開発領域における研究開発課題「生活習慣病予防に働く早期ライフステージの生活環境記憶の解明」等の支援のもとで行われたものです。
本研究成果は2021年12月2日に国際科学誌『Nature Communications』オンライン版に掲載されました。
4.発表内容
脂肪組織中の白色脂肪細胞は栄養分を脂肪として蓄え、空腹時には脂肪を分解して飢えから体を守り、また摂食制御や二次成長に重要なホルモンを分泌する重要な細胞です。栄養摂取と消費のエネルギーバランスが崩れると肥満を伴うメタボリックシンドロームが発症します。脂肪組織中には脂肪細胞になる以前の前駆脂肪細胞も存在します。栄養を過剰摂取すると、脂肪細胞が肥大化し、また前駆脂肪細胞から成熟した脂肪細胞ができ、余分な栄養分を脂肪として蓄えるようになります。肥満を伴うメタボリックシンドロームを予防する上で、前駆脂肪細胞からどのような仕組みで脂肪細胞ができるかを理解することは重要です。遺伝子の発現は、遺伝子の近くにあるプロモーター(注6)と、離れた場所にあるエンハンサーとよばれる制御部位によって調節されます。プロモーターは遺伝子を発現させる機能を持ち、エンハンサーは遺伝子の発現を高める機能を持ちます。脂肪を蓄える遺伝子のエンハンサーは、前駆脂肪細胞では準備状態、脂肪細胞では活性化状態になっています。しかし、前駆脂肪細胞においてエンハンサーを準備状態に止める仕組み、活性化状態に変化する仕組みは明らかではありませんでした。
ゲノムDNAはヒストンとよばれるタンパク質により巻き取られたクロマチン(注7)構造をとって、細胞の中の核に収納されています。ヒストンのメチル化やアセチル化(注8)といった後天的に書き変えられる遺伝情報(エピゲノム)によって、クロマチンの構造や遺伝子の働きが変わります。活性化状態のエンハンサーのクロマチンでは、ヒストンH3の27番目のリジンがアセチル化(H3K27ac、注9)されています。一方、準備状態のエンハンサーのクロマチンでは、H3K27acが低く保たれています。クロマチンの上では、エピゲノムH3K27acを書き込むヒストンアセチル化酵素(注10)と、H3K27acを消すヒストン脱アセチル化酵素(注11)がせめぎ合い、エンハンサーの働きを調節しています。
研究グループは前駆脂肪細胞から脂肪細胞ができるのを抑えるタンパク質SETD5に着目し、エピゲノムH3K27acおよびSETD5がゲノム上の遺伝子配列のどこに存在するかを、次世代シークエンサー(注12)を用いて解析しました。さらにSETD5が他のどのようなタンパク質と相互作用するかを、質量分析装置(注13)を用いて網羅的に解析しました。その結果、SETD5はヒストン脱アセチル化酵素、核内受容体コリプレッサー(注14)、転写因子(注15)とタンパク質複合体をつくり、脂肪細胞分化のマスターレギュレーター(注16)と呼ばれるCebpaとPparg遺伝子のエンハンサーに結合し、準備状態を保っていることがわかりました。また、細胞分裂後期には、後期促進複合体(注17)と呼ばれる別のタンパク質複合体の働きによりSETD5が分解されると、エピゲノムH3K27acが書き込まれ、エンハンサーの働きが活性化し、前駆脂肪細胞から脂肪細胞ができることもわかりました。前駆脂肪細胞が細胞分裂するタイミングで、タンパク質複合体が変わることで、エンハンサーのエピゲノムが書き換わり、脂肪細胞ができると考えられます。
今回の研究では、タンパク質SETD5が脂肪を蓄える働きをもつ白色脂肪細胞の「できる・できない」を決めていることが明らかになりましたが、同様のしくみが脂肪を燃焼する働きを持つベージュ脂肪細胞(注18)などにもある可能性があります。脂肪細胞はエネルギー代謝の調節に重要な役割を持っていることから、本研究成果は、生活習慣病の予防や新規治療法の開発において役立つことが期待されます。
5.発表雑誌
- 雑誌名:
- Nature Communications
- 論文タイトル:
- Spatiotemporal dynamics of SETD5-containing NCoR-HDAC3 complex determines enhancer activation for adipogenesis
- 著者:
- Yoshihiro Matsumura*,#, Ryo Ito*, Ayumu Yajima*, Rei Yamaguchi, Toshiya Tanaka, Takeshi Kawamura, Kenta Magoori, Yohei Abe, Aoi Uchida, Takeshi Yoneshiro, Hiroyuki Hirakawa, Ji Zhang, Makoto Arai, Chaoran Yang, Ge Yang, Hiroki Takahashi, Hitomi Fujihashi, Ryo Nakaki, Shogo Yamamoto, Satoshi Ota, Shuichi Tsutsumi, Shin-ichi Inoue, Hiroshi Kimura, Youichiro Wada, Tatsuhiko Kodama, Takeshi Inagaki, Timothy F. Osborne, Hiroyuki Aburatani, Koichi Node, Juro Sakai# (*筆頭著者、 #責任著者)
- DOI番号:
- 10.1038/s41467-021-27321-5
6.用語解説
(注1)エピゲノム:ゲノムの塩基配列以外の後天的に書き換えられる遺伝情報をさす。具体的にはDNAのメチル化、ヒストンのメチル化やアセチル化など。
(注2)タンパク質複合体:二つ以上のタンパク質からなる複合体。タンパク質-タンパク質相互作用によって作られる。
(注3)白色脂肪細胞:栄養分を脂肪として蓄える脂肪細胞。空腹時には脂肪を分解して栄養分を血液中に供給する。
(注4)エピゲノム・プロテオミクス解析:エピゲノム解析は、細胞の中のDNAのメチル化、ヒストンのメチル化やアセチル化などを調べる手法。プロテオミクス解析は、細胞の中の多様な種類のタンパク質を網羅的に調べる手法。
(注5)エンハンサー:遺伝子の発現を強める機能をもつ制御部位。遺伝子から離れたところに存在する。
(注6)プロモーター:遺伝子を発現させる機能をもつ制御部位。遺伝子の近くに存在する。
(注7)クロマチン:ゲノムDNAとタンパク質の複合体。ゲノムDNAはヒストンタンパク質により巻き取られたクロマチン構造をとり、細胞の中の核に収納される。
(注8)ヒストンのメチル化やアセチル化:後天的に書き換わるヒストンタンパク質の化学変化。ヒストンのメチル化は遺伝子の働きを促進、抑制のどちらにも働く。ヒストンのアセチル化は遺伝子の働きを活発にする。
(注9)ヒストンH3の27番目のリジンのアセチル化(H3K27ac):ヒストンH3タンパク質の27番目のリジンのアセチル化。遺伝子の働きを活発にするエピゲノム。
(注10)ヒストンアセチル化酵素:ヒストンタンパク質をアセチル化する酵素。エピゲノムH3K27acを書き込み、遺伝子の働きを活発にする。
(注11)ヒストン脱アセチル化酵素:ヒストンタンパク質を脱アセチル化する酵素。エピゲノムH3K27acを消し、遺伝子の働きを抑える。
(注12)次世代シークエンサー:数千万のDNA断片の塩基配列を同時に決定することができる解析装置。従来のシークエンサーに比べ大幅に速く、安価に塩基配列を決定できる。
(注13)質量分析装置:分子をイオン化し、その質量を分析する装置。一度に複数のタンパク質の質量を測定し、同定することができる。
(注14)核内受容体コリプレッサー:ヒストン脱アセチル化酵素の働きを活発にする働きをもつタンパク質。遺伝子の働きを抑える。
(注15)転写因子:特定のDNA配列を認識し、結合することができるタンパク質。他のタンパク質と相互作用することで、遺伝子の発現を強めたり、弱めたりする。ここではC/EBPβとC/EBPδタンパク質をさす。C/EBPβとC/EBPδタンパク質は、脂肪細胞分化の初期に働く。
(注16)脂肪細胞分化のマスターレギュレーター:脂肪細胞の分化を制御する転写因子。CebpaとPparg遺伝子からできるC/EBPαとPPARγタンパク質をさす。C/EBPαとPPARγタンパク質は、脂肪細胞分化の後期に働き、脂肪を蓄える遺伝子の働きを活発にする。
(注17)後期促進複合体:細胞分裂後期に、タンパク質に分解の目印であるユビキチンをつける酵素として働く。ユビキチンがついたタンパク質は、プロテアソームと呼ばれる別のタンパク質複合体によって分解される。
(注18)ベージュ脂肪細胞:脂肪を消費し、熱を産生する働き持つ脂肪細胞。肥満や糖尿病を予防する働きがある。
7.添付資料
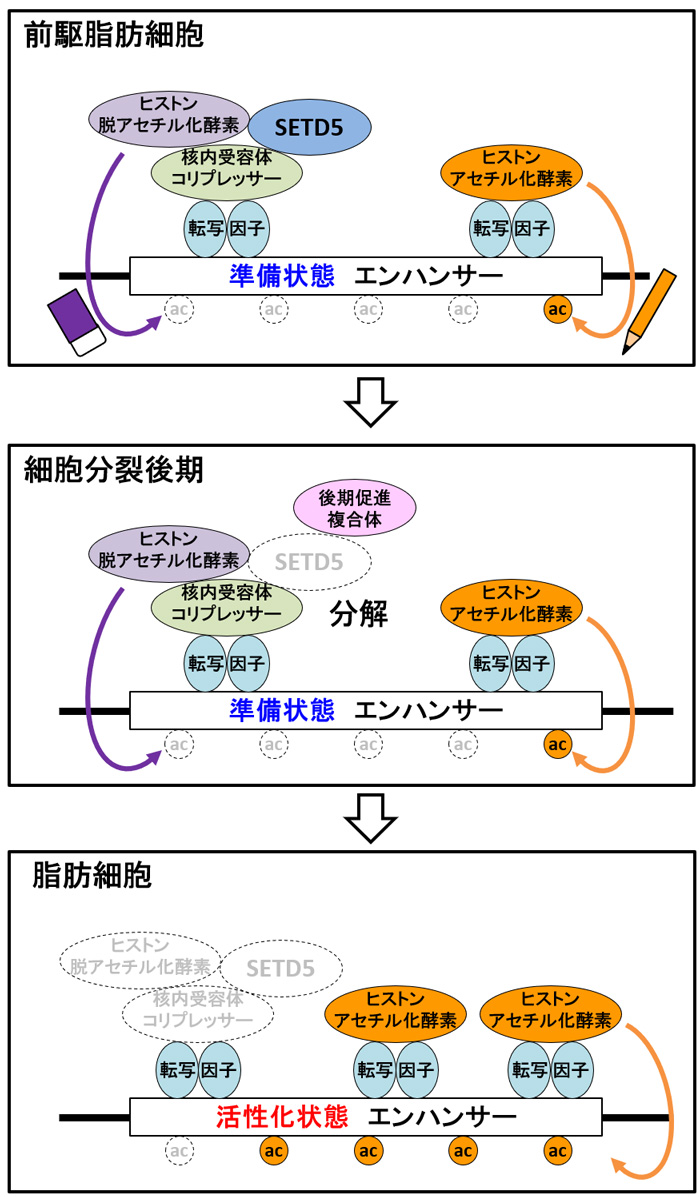
図1.脂肪細胞が「できる・できない」を決めるエピゲノムのしくみ。
図の中の丸で囲った『ac』はヒストンH3の27番目のリジンのアセチル化(H3K27ac)を表している。図の中の転写因子は、C/EBPβとC/EBPδを指す。SETD5を含むタンパク質複合体が「いつ・どこに・どのように」存在するかが、脂肪を蓄える遺伝子のエンハンサーの働きを調節する。