2022-05-13 日本医療研究開発機構
日本医療研究開発機構(AMED)が「次世代がん医療創生研究事業(P-CREATE)」と「産学連携医療イノベーション創出プログラム(ACT-M)」で支援した、国立がん研究センター、庄内地域産業振興センター、住友ファーマ株式会社(旧社名 大日本住友製薬株式会社)の研究チームが、急性白血病治療薬として創製した新薬候補化合物について、日本および北米で実施中の急性白血病を対象とした本新薬候補化合物のフェーズ1/2試験の最初の患者さんへの投与を開始しました。
なお、本内容については上記機関より、2022年3月31日に下記のプレスリリースが行われております。
AMEDは、今後とも日本国内にける新規薬剤開発の支援を広く行ってまいります。
国立研究開発法人国立がん研究センター(所在地:東京都中央区、理事長:中釜 斉、以下「国立がん研究センター」)、公益財団法人庄内地域産業振興センター(本部:山形県鶴岡市、理事長:皆川 治、以下「庄内地域産業振興センター」)、大日本住友製薬株式会社(本社:大阪府大阪市、代表取締役社長:野村 博、以下「大日本住友製薬」)は、新薬候補化合物DSP-5336(開発コード、以下「本剤」)のバイオマーカー候補の選別や適応症の検討等に関する共同研究を実施しています。このたび、大日本住友製薬が日本および北米で実施中の急性白血病を対象とした本剤のフェーズ1/2試験の最初の患者さんへの投与を開始しましたので、お知らせします。
発表のポイント
- 急性白血病に関する基礎研究成果をもとに開発された新規薬剤候補の臨床試験(フェーズ1/2)において患者さんへの投与が開始されました。
- MLL遺伝子およびNPM1遺伝子変異を有する急性白血病の新規薬剤開発を目指します。
国立がん研究センター、庄内地域産業振興センター、大日本住友製薬株式会社は、新薬候補化合物DSP-5336(開発コード、以下「本剤」)のバイオマーカー候補の選別や適応症の検討等に関する共同研究を実施しています。このたび、大日本住友製薬が日本および北米で実施中の急性白血病を対象とした本剤のフェーズ1/2試験の最初の患者さんへの投与を開始しましたので、お知らせします。
急性白血病の治療は現在でも化学療法が主体であり、治癒が期待できない予後不良群が存在します。特にMLL(mixed-lineage leukemia)遺伝子の染色体転座が見られるMLL転座白血病患者の5年生存率は20%以下と極めて不良であり、革新的な分子標的療法の開発が強く望まれています。
庄内地域産業振興センター/国立がん研究センター・鶴岡連携研究拠点がんメタボロミクス研究室の横山 明彦チームリーダーの研究チームは、MLL染色体転座の結果生み出されるMLL融合タンパクがMENINタンパクと結合することで急性白血病を発症するメカニズムを世界に先駆けて発見しました。その研究成果に基づき、国立大学法人京都大学(本部:京都府京都市、総長:湊 長博)と大日本住友製薬との協働研究プロジェクト「DSKプロジェクト」を通してMLLタンパクとMENINタンパクとの結合を選択的かつ強力に阻害する本剤を創製しました。さらに、本剤の非臨床試験(以下「本研究*」)において、国立がん研究センター研究所造血器腫瘍研究分野の北林 一生分野長の研究チームと横山チームにより、これまでに国立がん研究センターが蓄積してきた臨床検体や様々なマウス白血病モデルを用いて、本剤の多様な白血病への抗腫瘍作用が示されました。
今後、大日本住友製薬は、MLL転座白血病およびNPM1遺伝子変異白血病を予定適応症として本剤の開発を進める予定です。
国立がん研究センターおよび庄内地域産業振興センターのがん研究の実績と、大日本住友製薬の創薬研究において蓄積された知見との融合による共同研究の成果を通じて、いまだ十分な治療法のない予後不良の急性白血病に対して革新的な治療薬を提供することを目指します。
*本研究は、国立研究開発法人日本医療研究開発機構(AMED)の医療分野研究成果展開事業「産学連携医療イノベーション創出プログラム(ACT-M)」の支援を受け実施しています。また、国立がん研究センターでは、関連する血液がんの研究に関し、国立研究開発法人日本医療研究開発機構(AMED)の「次世代がん医療創生研究事業(P-CREATE)」 の支援を受けています。
ご参考
急性骨髄性白血病について
血液がんの一種である急性骨髄性白血病は、血液細胞の供給源である骨髄で分化・成熟能が障害された骨髄系細胞(白血病細胞)が異常増殖することで引き起こされます。白血病細胞の異常増殖により、正常な造血機能が阻害されることから適切な治療がなされない場合は、短期間で致死的な症状を呈する重篤な疾患です。日本における年間罹患数は7,000人程度であり、近年では白血病細胞の染色体核型・遺伝子変異解析に基づいた詳細な病型分類が行われ治療戦略に役立てられています。急性骨髄性白血病に対する基本的な治療戦略は強力な抗がん剤治療(化学療法)ですが、一部の病型における治療抵抗性や高齢者患者さんにおける適応の難しさなどから、充分な治療選択肢が存在していない状態です。
MLL転座白血病およびNPM1変異白血病について
MLL転座白血病は、何らかの原因により11番染色体に座位するMLL遺伝子が損傷し、転座を起こすことで異なる染色体座に存在する遺伝子と結合し、MLL融合遺伝子を生じることで発症します。MLL遺伝子は80以上の遺伝子と融合することが知られており、これらMLL融合遺伝子を有する白血病の大半は極めて予後不良であることが知られています。特に乳児白血病に多く見られ、本来比較的治りやすいはずである乳児白血病の治療予後を大きく引き下げている遺伝子異常です。MLL転座白血病の5年生存率は20%程度であり、標準療法である化学療法剤にも抵抗性を示すことから革新的な新薬の創出が期待されています。
NPM1変異白血病では、核内リン酸化タンパク質をコードするヌクレオホスミン(NPM1)遺伝子に変異が生じ、その機能に異常をきたすことで白血病発症に至ります。NPM1変異は、急性骨髄性白血病の予後不良因子ではありませんが、他の遺伝子変異(FLT3変異、IDH1/2変異、TP53変異など)と共存するケースが多く、その遺伝子変異の組み合わせにより予後中程度および不良の白血病となります。また、共存する遺伝子変異を標的とした分子標的薬などが有効なケースもありますが、NPM1遺伝子変異を標的とした承認薬はいまだにありません。
開発の経緯について
本剤は、20年以上に及ぶMLL転座白血病の基礎研究成果の積み上げにより開発につながりました。
横山と北林らは1998年頃からMLLタンパク質の性質の解明に取り組み始めました。横山は以来一貫してMLL白血病研究を継続し、米国留学中に正常なMLLタンパク質とMLL融合タンパク質の両方がMENINというタンパク質と結合することを見出しました(Yokoyama et al., 2004)(図1A)。また、MENINと結合できなくなるように構造を変化させたMLL融合タンパク質は白血病を引き起こさないことを実験的に示しました(Yokoyama et al., 2005)。さらに、MLLはMENINと結合することでLEDGFという別のタンパク質と結合し、標的遺伝子領域を認識することを見出しました(Yokoyama et al. 2008)。これにより、白血病を引き起こす関連遺伝子の発現は、MLL融合タンパク質がMENINと結合して複合体を形成し特定の遺伝子領域に結合することで活性化されるということが解明されました。
これらの成果から、MLLとMENINの結合を阻害する化合物がMLL融合タンパク質を無力化するであろうという推論の分子基盤が明らかになりました(図1B)。アカデミア、製薬企業がMENIN-MLL結合阻害剤の開発に乗り出し、現在では複数の企業による開発競争に至っています。本剤は、横山が京都大学在職中にDSKプロジェクトに参加し、大日本住友製薬と共同で開発しました。その後、AMED ACT-M研究費の支援を受け、横山は国立がん研究センター鶴岡連携研究拠点にてマウス病態モデルを用いた薬効評価を行い、北林が国立がん研究センター研究所・造血器腫瘍分野においてヒト臨床材料を用いた薬効評価を行いました。その結果MLL転座白血病以外のNPM変異白血病などでも本薬剤が薬効を示すことが確認され、臨床試験の開始に至りました。本剤の開発は基礎研究により明らかにされた分子メカニズムの理解を基盤として創薬に至った一例であり、基礎医学研究の重要性を示すものです。
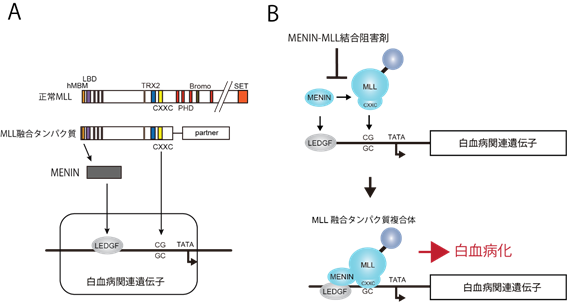
図1 MENIN-MLL結合阻害剤の作用機序A. 正常MLLとMLL融合タンパク質の構造。MLLタンパク質はMENINを介してLEDGFと結合し、CXXCドメインを介してCG配列と結合する。
MLL融合タンパク質は二つの分子間結合を介して遺伝子領域と結合します。一つはMLL融合タンパク質に含まれるCXXCドメインという構造が遺伝子発現調節領域にあるCGというDNA配列に結合する分子間結合です。もう一つは、MLL融合タンパク質がMENINというタンパク質と結合し(Yokoyama et al. 2004 Yokoyama et al. 2005)、MENINの構造を介してLEDGFというタンパク質に結合する分子間結合です。重要な点は、MLLはMENINと複合体を形成することで初めてLEDGFと結合できるようになるということです(Yokoyama and Cleary, 2008)。この二つの分子間結合によって、MLL融合タンパク質複合体は、安定して白血病関連遺伝子の遺伝子発現調節領域に結合し、遺伝子発現を活性化することができるようになります(Okuda et al. 2014)。
B. MENIN-MLL結合阻害剤の作用機序。MENIN-MLL結合阻害剤はMLL融合タンパク質とMENINの結合を阻害することで、MLL融合タンパク質による白血病関連遺伝子の異常な遺伝子発現を妨げ、白血病細胞を無害な細胞に変化させる。
DSKプロジェクトについて
大日本住友製薬と京都大学の産学連携プロジェクトとして2011年3月から2021年3月まで、日本初のオープンイノベーション拠点である京都大学の「メディカルイノベーションセンター」を中心に、大日本住友製薬の研究所の研究チームと協働で独創的な抗がん剤、診断・治療法の創出を目指してきました。2021年4月からは産学連携講座として、研究活動を継続しています。
国立がん研究センター研究所について
国立がん研究センター研究所は、国内最大級のがん研究施設で、極めて独創的な基礎研究から、実際の治療薬・診断薬の開発研究まで、中央病院(東京都)、東病院(千葉県)と連携し幅広く対応しています。
これまで、多様なシークエンサー群と独自のバイオインフォマティクス開発によるがんゲノム解析で多くの成果を上げ、その発見を基にした薬剤開発、病院と連携した臨床試験へとつなげています。また、がんゲノム医療の要素技術開発にも注力しており、我が国初のがん遺伝子パネル検査を開発し保険収載を実現しただけでなく、造血器悪性腫瘍や小児がんの遺伝子パネル検査法の開発にも取り組んでいます。さらに、バイオリソースの拡充においては、既に400種類以上の患者腫瘍組織移植(patient-derived xenograft)マウスや2 万種類以上の新鮮凍結腫瘍組織バイオバンクが整備されており、これらを有効に活用して国内外のアカデミア・企業と共同研究を展開しています。詳しくは、国立がん研究センター研究所のホームページ をご覧ください。
庄内地域産業振興センターについて
庄内地域産業振興センターは、地場産業の育成及び発展を支援することによって、活力ある地域経済社会の形成、地域住民の生活向上に貢献することを目的として、1987年に設立された公益法人で、国立がん研究センター・鶴岡連携研究拠点がんメタボロミクス研究室の事業実施機関となっています。詳しくは、庄内地域産業振興センターのホームページ をご覧ください。
大日本住友製薬について
大日本住友製薬は、人々の健康で豊かな生活のために、研究開発を基盤とした新たな価値の創造により、広く社会に貢献することを企業理念としています。この理念を実現するため、また、日本はもちろん世界の方々に革新的で有用な医薬品をお届けするため、新薬の研究開発に全力を注いでいます。詳しくは、大日本住友製薬のホームページ をご覧ください。
参考文献
Okuda, H., Kawaguchi, M., Kanai, A., Matsui, H., Kawamura, T., Inaba, T., Kitabayashi, I., and Yokoyama, A. (2014). MLL fusion proteins link transcriptional coactivators to previously active CpG-rich promoters. Nucleic Acids Res42, 4241-4256.
Yokoyama, A., and Cleary, M. L. (2008). Menin critically links MLL proteins with LEDGF on cancer-associated target genes. Cancer cell 14, 36-46.
Yokoyama, A., Somervaille, T. C., Smith, K. S., Rozenblatt-Rosen, O., Meyerson, M., and Cleary, M. L. (2005). The menin tumor suppressor protein is an essential oncogenic cofactor for MLL-associated leukemogenesis. Cell 123, 207-218.
Yokoyama, A., Wang, Z., Wysocka, J., Sanyal, M., Aufiero, D. J., Kitabayashi, I., Herr, W., and Cleary, M. L. (2004). Leukemia proto-oncoprotein MLL forms a SET1-like histone methyltransferase complex with menin to regulate Hox gene expression. Mol Cell Biol 24, 5639-5649.
お問い合わせ先
本件に関するお問い合わせ先
国立研究開発法人国立がん研究センター 企画戦略局広報企画室
公益財団法人庄内地域産業振興センター
国立がん研究センター・鶴岡連携研究拠点 がんメタボロミクス研究室
大日本住友製薬株式会社 コーポレートコミュニケーション部
AMED事業に関するお問い合わせ先
「産学連携医療イノベーション創出プログラム(ACT-M)」について
日本医療研究開発機構 実用化推進部 研究成果展開推進課
「次世代がん医療創生研究事業(P-CREATE)」について
日本医療研究開発機構 創薬事業部 医薬品研究開発課