2022-09-20 東京大学
1.発表者
金子 雄大(東京大学大学院工学系研究科先端学際工学専攻 博士後期課程)
加藤 洋人(東京大学大学院医学系研究科 准教授)
杉山 暁(東京大学アイソトープ総合センター 助教)
山次 健三(東京大学大学院薬学系研究科 助教)
児玉 龍彦(東京大学名誉教授/東京大学先端科学技術研究センター がん・代謝プロジェクトリーダー(特任研究員))
塚越 雅信(サヴィッド・セラピューティックス株式会社 代表取締役社長)
2.発表のポイント
- がんの光免疫治療において、再発腫瘍を完全に消失させる新しい光活性化物質Ax-SiPcを用いた新しい光免疫・抗体ミメティクス治療薬FL2を開発した。
- 乳がんを再発させたマウスに本治療薬を用いて実験したところ、腫瘍が完全に消失した。
- FL2と腫瘍免疫療法を併用することで、がんを手術せずに治す画期的な治療法の確立につながる可能性がある。
3.発表概要
光免疫治療は切除の難しい進行がんでも、手術なしに近赤外線の照射によって活性化したがん細胞を殺すことができます。しかし近赤外線は人体内で届く範囲が限られており、治療後の再発が課題となっていました。東京大学アイソトープ総合センター杉山暁助教らの研究グループは、抗体ミメティクス治療薬(注1)とAx-SiPc(注2)を結合させた効果の高い光免疫製剤「FL2」の開発に成功しました。
これまで、マウスにヒト乳がん細胞を移植し成長させ、FL2治療を1回行った場合、肉眼的には腫瘍が消えたように見えても、病理検査ではがん細胞の一部が残存し、5割が再発していました。本研究では、再発腫瘍が大きくなったあと2回目の治療を行った場合、腫瘍が完全に消失し、その瘢痕組織に免疫系の細胞が集簇していることを、病理検査により発見しました。
FL2反復投与は光が到達できる皮膚腫瘍の根治に効果的であり、腫瘍免疫の活性化に有効な可能性があります。今後、光免疫治療とネオアンチゲン(注3)へのRNAワクチンを用いた腫瘍免疫治療を併用した実験を発展させることで、より広範な進行がんの治療につながることが期待されます。
本研究成果は、2022年9月20日(火)(日本時間)に「Cancer Science」にオンライン掲載されました。
4.発表内容
近年、早期がんの治療成績は向上している一方、再発と転移を伴う進行がんの死亡者は増加し、有効な治療法の開発が切望されています。がんの主な治療方法である、手術療法(外科的切除や内視鏡的切除など)、化学療法、放射線治療は、がん細胞のみでなく、周囲の正常組織や臓器にも傷害を与えてしまいます。このため、正常細胞・組織への傷害は副作用として患者の体に大きな負担を強いることになっています。このようなことから、正常細胞や組織を傷つけることなく、がん細胞のみにダメージを与える治療法の開発が求められています。近年、この理論に基づいた新しいがん治療法として、近赤外光を使用した光免疫治療法の開発が進められ、切除の難しい進行がんの患者の生活の質を保ちながら実施できる治療として期待されています。
光免疫療法は、腫瘍細胞を認識する抗体に光で活性化される化合物(光増感剤)を結合させた薬を使用します。薬の活性化には、腫瘍細胞局所に集まった光増感剤に効率よくエネルギーを与えるために、体の深部に到達できる近赤外光(690nm)を使用します。光照射によりエネルギーを受け取った光増感剤は化学反応を起こし、細胞表面付近で細胞を傷害する物質(一重項酸素(注4))を発生させます。これにより、光増感剤が集積した腫瘍細胞のみを殺すことで、周囲の正常細胞、組織へのダメージをなくした新しいがんの治療法として開発が進められています。
本研究グループは、人工的に合成された、製造しやすく腫瘍細胞表面に存在する抗原特異的に結合する抗体ミメティクス薬剤と、人工的に設計された、光を当てると一重項酸素を従来薬より多く作るAx-SiPcを結合させた治療薬「FL2」を開発しました。「FL2」はヒト乳がん細胞に発現しているHER2分子(注5)に特異的に結合します。このため、マウス体内へ投与された「FL2」はマウスへ移植されたヒト乳がん細胞へ集積します。
今回、ヒト乳がん細胞を移植した腫瘍塊(大きさ平均417±88 mm3)を持つ10匹のマウスに対し、「FL2」の投与を行い、光照射による治療を行いました。1回目の治療後、全てのマウスで急激に腫瘍塊の大きさが減少し、治療後15日後の大きさの平均は約40 mm3となりました。しかし、治療30日後、半分の5匹に肉眼的再発が認められました。これら5匹のマウスの再発した腫瘍塊の大きさは治療63日後に平均381±296 mm3となったため、1回目と同じ手法で2回目の治療を行い、全例で肉眼的に腫瘍の消失を確認しました。さらに1回目の治療後約90日、2回目の治療後約30日目に、10匹全てのマウスの剖検を行い、病理学的にも腫瘍細胞が完全に消失し、治療部分は正常な皮膚の状態へと回復していることを明らかにしました。
また、治療によりがん細胞が受けた影響を確認するため、光照射10日後で治癒途中の治療部位の病理学的な解析を行いました。そこでは、全ての腫瘍細胞は凝固壊死しており、壊死した腫瘍細胞の周りには免疫系の細胞が集まってきていることを確認しました。光免疫療法では光増感剤が集積したがん細胞のみが、光照射により特異的に壊死に至っていることを明らかにしました。
光免疫療法により腫瘍免疫を誘導し、進行がんの根治の率を高められれば、増加している進行がんの根治に新たな可能性を与えることになります。現在は転移しやすいマウスの腫瘍を用い、光免疫治療と、コロナ禍で高い有効性の証明された修飾RNA(注6)を用いたがんのネオアンチゲンへのワクチンの併用療法の効果を検討中です。今後、FL2を用いた皮膚の悪性腫瘍への臨床開発を進めることで、進行がんに対する新たな治療法の誕生につながることが期待されます。
本研究は、東大発ベンチャーであるサヴィッド・セラピューティックス株式会社の支援を受けて実施されました。
5.発表雑誌
- 雑誌名:
- 「Cancer Science」
- 論文タイトル:
- Pathological Complete Remission of Relapsed Tumor by Photo-ActivatingAntibody–Mimetic Drug Conjugate Treatment
- 著者:
- Kaneko Yudai, Yamatsugu Kenzo, Yamashita Takefumi, Takahashi Kazuki, Tanaka Toshiya, Aki Sho, Tatsumi Toshifumi, Kawamura Takeshi, Miura Mai, Ishii Masazumi, Ohkubo Kei, Osawa Tsuyoshi, Kodama Tatsuhiko, Ishikawa Shumpei, Tsukagoshi Masanobu, Chansler Michael, Sugiyama Akira*, Kanai Motomu*, Katoh Hiroto*
- DOI 番号:
- 10.1111/cas.15565
6.問い合わせ先
東京大学アイソトープ総合センター RI防護・環境保全部門 助教 杉山 暁(すぎやま あきら)
7.用語解説
(注1)抗体ミメティクス
抗体ミメティクスは、分子量の大きな抗体を模倣しつつ、分子量を小さくし、結合特異性を増すように人工的に設計されたタンパク質です。抗がん剤や抗ウィルス剤、イメージング用検査薬として開発が進められています。
(注2)Ax-SiPc
Ax-SiPcは、近赤外線の照射で活性化されがん細胞など殺すシリコン・フタロシアニン化合物で垂直方向のリンカーの結合部位を持つ新規化合物、Axially Substituted Silicon Phthalocyanineの略称。リンカーまたはリンカー先の化合物を介して抗体や抗体もどきの人工合成タンパク質に結合できます。
(注3)ネオアンチゲン
ネオアンチゲンは、がん細胞の体細胞変異に由来する変異タンパク質です。がんの遺伝子変異により新たに生じた抗原(アンチゲン)であり、正常組織では発現しておらず、腫瘍関連抗原に比べてよりがん特異的であると考えられています。そのため、正常組織に対する傷害性が低く、がん特異的な免疫原性が高く、新たな免疫療法のターゲットとして期待されています。
(注4)一重項酸素
一重項酸素は、光増感分子が基底状態の酸素と反応することで生成されます。酸素の存在下での光増感分子の光照射と、これに続く基底状態の酸素と励起三重項状態の光増感剤の反応で、一重項状態の酸素の生成が行われます。
(注5)HER2
HER2は上皮成長因子受容体2(human epidermal receptor 2)と呼ばれる細胞の増殖などに関係しているタンパク質です。HER2陽性乳がんなどの治療薬の分子標的とされています。
(注6)修飾RNA
修飾RNAは、生体内でタンパク質を作らせるために免疫回避する仕組みを組み込んだ人工的に作ったメッセンジャーRNAです。通常生体外から入ってきたメッセンジャーRNAは、免疫反応によりすぐに分解されてしまいます。しかし体内に存在する通常のメッセンジャーRNAでは核酸化合物の一つがウリジンであるのに対して、治療薬やワクチンとして開発されているmRNAはウリジンの代わりに修飾核酸(シュードウリジンやその他の誘導体)を使うことで免疫回避することができます。
8.添付資料
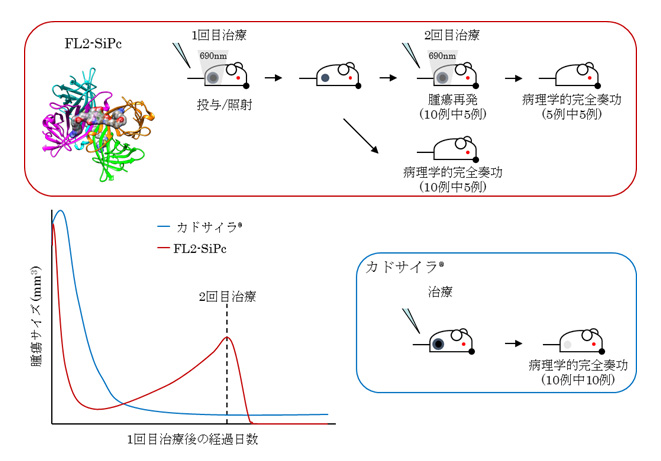
図:光活性型抗体ミメティクス製剤(FL2-SiPc)による治療と経過
FL2-SiPcによる治療はHER2陽性ゼノグラフトモデルマウスの腫瘍を急速に減少させるが、複数例で腫瘍の再発が見られた。再発例におけるFL2-SiPeの再治療は腫瘍を急速に減らし、病理学的完全奏功へと導いた。