遺伝性の希少かつ重篤な疾患の日常診療における発見と管理は、ゲノム解読によって改善される可能性があることが、新しい研究によって明らかになりました。 The detection and management in routine care of inherited rare and serious conditions can be improved by genome sequencing, according to a new study.
2022-12-19 エディンバラ大学
スコットランド・ゲノム・パートナーシップ(SGP)として知られるこのプロジェクトの成果は、医療政策や資金調達の決定に活用されるだろうと、専門家は述べている。
全ゲノム配列決定では、個人の遺伝子の全塩基配列を読み取り、通常のパターンとは異なる変異体を特定する。
科学者たちは、これらの遺伝子と病気の原因となることが知られている遺伝子とを比較し、どの変異体がその人の症状の鍵を握っているのかを特定するために、この変異体のショートリストを調べます。
スコットランドでは、人口の8%が希少疾患に罹患しており、そのうち約80%が遺伝的な原因によるものであると推定されています。
発達障害や学習障害、長期的な健康に影響を与える多くの症状の原因となる15万以上の遺伝子異常が知られていますが、多くの人が診断されていません。
SGPのメンバーとして、エジンバラ大学の科学者は、過去の遺伝子検査で遺伝的原因が特定されなかった希少疾患を持つスコットランド人とその家族から得た1,000人分のゲノムの塩基配列を決定しました。
このデータは、健康や病気において遺伝子が果たす役割を配列して研究するGenomics Englandのイニシアチブである「10万人ゲノムプロジェクト」の一環として、処理と保存のために送られました。
NHSスコットランドの遺伝科学者と医師は、分析されたデータを解釈し、参加者に有用な結果を伝えました。これまでに参加者の23%で遺伝子診断が判明しています。
<関連情報>
- https://www.ed.ac.uk/news/2022/genome-project-sheds-light-on-rare-diseases-in-sco
- https://www.nature.com/articles/s41431-022-01226-3
公的医療保険制度における希少な遺伝性疾患に対する遺伝子パネルベースのゲノムシークエンシング:今後の検査への示唆 Genome sequencing with gene panel-based analysis for rare inherited conditions in a publicly funded healthcare system: implications for future testing
Lynne J. Hocking,Claire Andrews,Christine Armstrong,Morad Ansari,David Baty,Jonathan Berg,Therese Bradley,Caroline Clark,Austin Diamond,Jill Doherty,Anne Lampe,Ruth McGowan,David J. Moore,Dawn O’Sullivan,Andrew Purvis,Javier Santoyo-Lopez,Paul Westwood,Michael Abbott,Nicola Williams,Scottish Genomes Partnership,Timothy J. Aitman & Zosia Miedzybrodzka
European Journal of Human Genetics Published:06 December 2022
DOI:https://doi.org/10.1038/s41431-022-01226-3
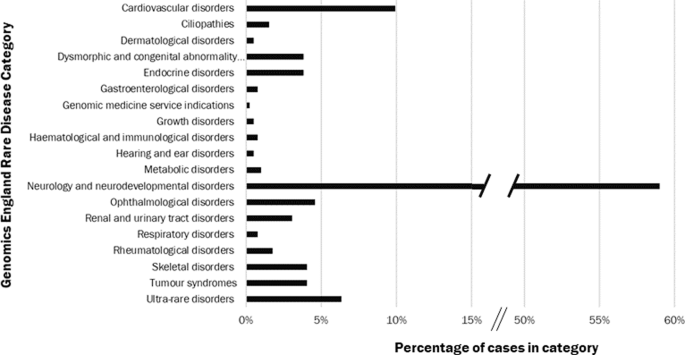
Abstract
NHS genetics centres in Scotland sought to investigate the Genomics England 100,000 Genomes Project diagnostic utility to evaluate genome sequencing for in rare, inherited conditions. Four regional services recruited 999 individuals from 394 families in 200 rare phenotype categories, with negative historic genetic testing. Genome sequencing was performed at Edinburgh Genomics, and phenotype and sequence data were transferred to Genomics England for variant calling, gene-based filtering and variant prioritisation. NHS Scotland genetics laboratories performed interpretation, validation and reporting. New diagnoses were made in 23% cases – 19% in genes implicated in disease at the time of variant prioritisation, and 4% from later review of additional genes. Diagnostic yield varied considerably between phenotype categories and was minimal in cases with prior exome testing. Genome sequencing with gene panel filtering and reporting achieved improved diagnostic yield over previous historic testing but not over now routine trio-exome sequence tests. Re-interpretation of genomic data with updated gene panels modestly improved diagnostic yield at minimal cost. However, to justify the additional costs of genome vs exome sequencing, efficient methods for analysis of structural variation will be required and / or cost of genome analysis and storage will need to decrease.


