2023-09-13 京都大学iPS細胞研究所
ポイント
- 大規模なiPS細胞樹立パイプラインを構築した。
- 指定難病注1)を持つ259人の患者さんから1,532のiPS細胞株の樹立に成功した。
- 樹立されたiPS細胞株は理化学研究所バイオリソース研究センターのiPS細胞バンクに寄託され、これを用いた疾患研究が推進されることが期待される。
1. 要旨
齋藤潤教授(CiRA臨床応用研究部門)らは、希少疾患注2)のiPS細胞研究を推進するため、患者さんの大規模なリクルートシステムとiPS細胞樹立パイプラインを構築し、259人の指定難病の患者さんから1,532個のiPS細胞株を樹立することに成功しました。
希少疾患は、患者数が限定的であるため、治療や研究が難しく、問題となっています。一方、iPS細胞を用いた疾患モデリングは、希少疾患研究の新しいアプローチとして注目されています。日本が医療費助成制度の対象として定める「指定難病」と、疾患モデル作製に有用なiPS細胞という技術を組み合わせることで、価値ある研究リソースが得られると考えられました。
この研究では、指定難病の患者さんからiPS細胞を作製し、細胞バンクへの寄託を目指しました。その結果、259人の患者さんから1,532個のiPS細胞株を確立しました。これらのiPS細胞は、今後、希少疾患の研究のための重要な研究リソースとして、病気の詳細なメカニズムの解明や治療法の開発に貢献することが期待されます。
本成果は、2023年9月8日に日本炎症・再生医学会の学会誌である国際学術誌「Inflammation and Regeneration」にオンライン掲載されました。
2. 研究の背景
希少疾患は、患者数が限られており、適切な治療の提供が困難です。これは、患者数が少なく、研究が十分に進まず、正確な診断法や治療戦略の確立が遅れていることに起因します。希少疾患の定義は国や地域によって異なりますが、その数は7,000以上とも言われます。希少疾患の診断・治療法開発に関する研究は、国際的な協力が必須であるとされ、OrphanetやOMIMなどのデータベースやIRDiRCやIRUDのような国際的、国内的なネットワークやコンソーシアムが構築されています。
希少疾患を対象とした新規の診断法や治療法の開発のため、iPS細胞を利用した疾患モデリングが注目されています。患者さんの細胞から作製されたiPS細胞は、患者さんの遺伝情報をもつため、希少疾患の大部分である遺伝性疾患の研究に適しています。また、複雑な臓器のモデリングや、特定の細胞への分化など、iPS細胞をはじめとした多能性幹細胞の培養技術や分化誘導法の研究が進んでいます。これらのことから、iPS細胞は希少疾患の研究における強力なツールとして活用されています。しかし、希少疾患の数に比べて、樹立されたiPS細胞の種類はまだまだ少ないのが現状です。そのため、さらに多くの希少疾患のiPS細胞を樹立し、細胞バンク等に預けることで、幅広い希少疾患に対してiPS細胞を用いた研究が可能な体制を整備していく必要があります。
日本では特定の希少疾患が医療費助成の対象として「指定難病」に認定されています。患者さんの経済的負担を軽減するために指定難病として定められた各疾患は、明確な診断基準が確立されており、共通の病歴収集フォーマットがあること、有効な特異的治療法が開発されていないことなど、iPS細胞を用いた研究に適した条件が揃っています。指定難病制度のもとで取得された患者さんの情報とiPS細胞を組み合わせることで、希少疾患の解析のための非常に価値のあるリソースとなり得ると考えられます。本研究では、このような背景を踏まえ、希少疾患の研究を推進するために、指定難病の患者さん由来のiPS細胞の樹立に取り組みました。
3. 研究結果
本研究では、指定難病の患者さんを募集し、研究に関する説明を行い、同意を得たあとに血液を採取し、そこからiPS細胞を樹立し、最終的に細胞バンクへiPS細胞を寄託するまでのパイプラインを確立しました(図1)。患者さんの募集は国立病院機構(本部:東京都目黒区)と湘南鎌倉総合病院(神奈川県鎌倉市)の協力のもと行いました。国立病院機構からは30の医療機関の協力を得ました。その結果、139の指定難病について259人の患者さんに本研究にご協力いただきました。
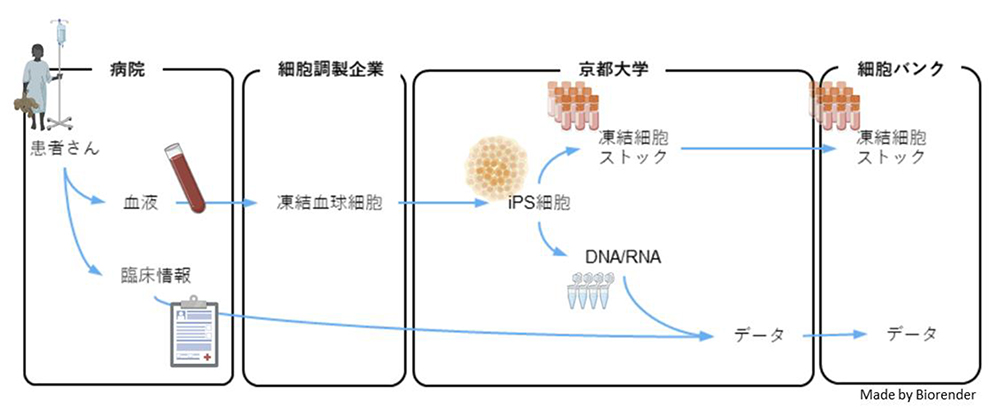
図1:本計画の概略
ドナーの平均年齢は45.53歳でした。内訳は男性125人、女性134人で、男女比は0.93でした。参加された指定難病の患者さんの疾患は、国際疾病分類(ICD)-10注3)の幅広い疾患カテゴリーに分類され、最も症例数が多かったカテゴリーは「先天奇形、奇形、染色体異常」(大分類XVII)でした(表)。
| 分類 | 樹立症例数 |
|---|---|
| I 感染症および寄生虫症 | 3 |
| II 新生物 <腫瘍> | 6 |
| III 血液および造血器の疾患ならびに免疫機構の障害 | 16 |
| IV 内分泌,栄養および代謝疾患 | 44 |
| V 精神および行動の障害 | 1 |
| VI 神経系の疾患 | 54 |
| IX 循環器系の疾患 | 15 |
| X 呼吸器系の疾患 | 5 |
| XI 消化器系の疾患 | 18 |
| XII 皮膚および皮下組織の疾患 | 10 |
| XIII 筋骨格系および結合組織の疾患 | 39 |
| XIV 尿路性器系の疾患 | 8 |
| XVII 先天奇形,変形および染色体異常 | 40 |
| 合計 | 259 |
表:国際疾病分類(ICD-10)に基づいた樹立症例の分類
259人の患者さんの血液から合計1,532個のiPS細胞株を樹立しました。樹立は通常のエピソーマルベクター注4)を用いた方法で行い、樹立ができなかった症例はありませんでした。初期化効率の平均は0.06%で、患者さんの年齢や性別による差は認められませんでした。樹立されたiPS細胞株の倍加時間注5)は、平均29.67±8.38時間で、これも年齢との相関はみられませんでした。一方、男性由来のiPS細胞株は、倍加時間がわずかに長いことがわかりました(女性:29.29±8.11時間 対 男性:30.07±8.64時間)。
次に、樹立したiPS細胞の基本的性質を評価しました。すべてのiPS細胞株は、一般的なヒト多能性幹細胞と同様の形態を示しました(図2)。また、どのような血球細胞にiPS細胞が由来するのかを調べたところ、iPS細胞株の大部分(97.8%)は、T細胞・B細胞以外の血球細胞に由来することがわかりました。樹立に使用したエピソーマルベクターがiPS細胞株に残存しているかを調べたところ、96.3%の細胞株では、1細胞あたりのプラスミド数が1以下であることが確認され、ほとんどのiPS細胞株において、プラスミドの持続性の影響は無視できると考えられました。
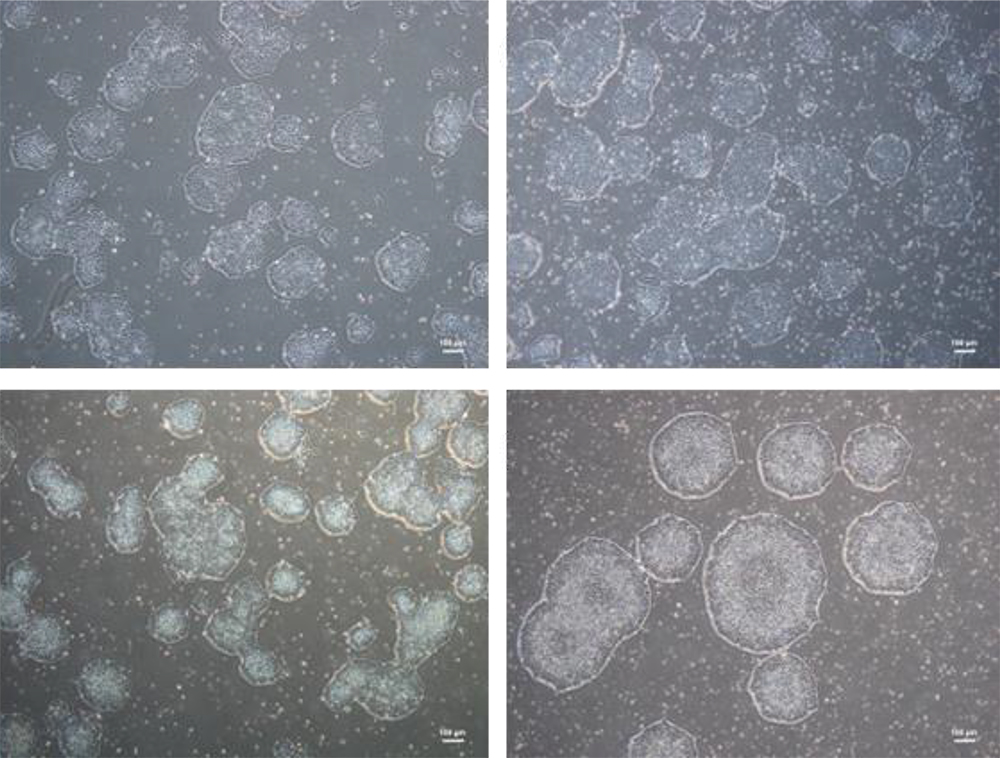
図2:4名の患者さん由来の代表的なiPS細胞株の顕微鏡像
次に、未分化多能性幹細胞で発現する代表的な遺伝子であるOCT3/4とNANOGの発現を評価しましたOCT3/4やNANOGの発現を欠く細胞株はありませんでしたが、その発現レベルには細胞株ごとに大きなばらつきが観察されました。興味深いことに、OCT3/4とNANOGの発現レベルは、どちらも女性由来の細胞株で有意に高いことがわかりました(図3)。年齢とこれらの転写因子の発現レベルとの関連は明らかではありませんでした。
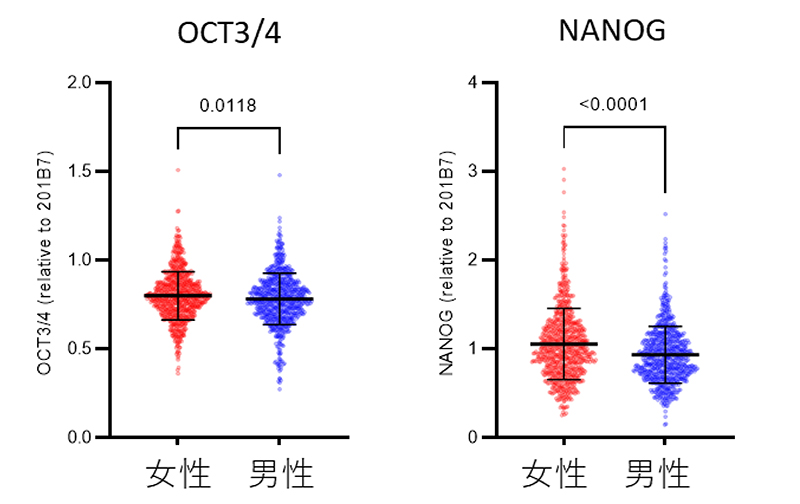
図3:OCT3/4とNANOGの発現レベルの男女比較
これらのiPS細胞株は、さまざまな研究者が希少疾患の研究に用いることができるよう、公的な細胞バンクである「理化学研究所バイオリソース研究センター(理研BRC)」(茨木県つくば市)のiPS細胞バンクに寄託しました。これにより、希少疾患の研究のために、研究者が各iPS細胞株を入手可能になりました。
4. まとめと展望
本研究では、国内の指定難病の患者さんから多数のiPS細胞を樹立し、幅広い疾患領域のiPS細胞リソースの構築に成功しました。樹立したiPS細胞は、理研BRCに寄託し、疾患研究のための研究に役立てられることが期待されます。また、iPS細胞ドナーの臨床情報に基づいた病歴調査システムを活用することで、疾患ごとの統一した病歴情報の取得が可能となるだけでなく、将来的にはドナーの追跡も可能なシステムが考えられます。
これらにより、疾患の表現型と細胞・遺伝子レベルでの表現型との相関研究が実現し、iPS細胞技術は希少疾患の研究や治療法の開発にも大きく寄与する可能性があります。さらに、新たに確認された遺伝子発現における性差の発見は、多能性の維持や細胞機能に与える影響についての理解を深める手がかりとなると考えられます。
今後の方針として、指定難病を含む希少疾患のiPS細胞の樹立、評価、寄託に向けた継続的な取り組みを進めていきます。性差の原因や細胞機能への影響に関する詳細な解析も進めていく予定です。最終的には、iPS細胞の解析結果と臨床知見を直接結びつけることで、治療や予防医療を含む個別化医療の実現を目指します。
5. 論文名と著者
- 論文名
A disease-specific iPS cell resource for studying rare and intractable diseases. - ジャーナル名
Inflammation and Regeneration - 著者
Megumu K. Saito1, Mitsujiro Osawa1, Nao Tsuchida2, Kotaro Shiraishi1, Akira Niwa1, Knut Woltjen1, Isao Asaka1, Katsuhisa Ogata2, Suminobu Ito2, Shuzo Kobayashi3, Shinya Yamanaka1 - 著者の所属機関
- 京都大学iPS細胞研究所(CiRA)
- 国立病院機構
- 徳洲会湘南鎌倉総合病院
6. 本研究への支援
本研究は、下記機関より支援を受けて実施されました。
- 日本医療研究開発機構 再生医療実現拠点ネットワークプログラム
- iPS細胞研究基金
7. 用語説明
注1)指定難病
国が「難病の患者に対する医療等に関する法律」に定められる基準に基づいて、医療費の助成や治療研究の推進を目的として指定している疾患を「指定難病」という。原因や治療法が明確でなく、長期にわたる治療が必要となる。
注2)希少疾患
一定数以下の患者数しか存在しない疾患。
注3)国際疾病分類(ICD)-10
世界保健機関(WHO)が死因や疾病の国際的な統計基準として公表している分類。死因や疾病の国際的な統計や、医療機関における診療記録の管理などに活用される。
注4)エピソーマルベクター
iPS細胞の樹立に必要な遺伝子を組み込んだ非ウイルス性の遺伝子導入分子。通常はiPS細胞樹立後に消失しますが、まれに細胞のゲノムに組み込まれて長期間残存するため、iPS細胞への残存を評価する必要がある。
注5)倍加時間
細胞が増殖して倍の数になるまでの時間。短いほど細胞の増殖力が強いことを示す。