2024-03-28 山梨大学,国立極地研究所
山梨大学総合分析実験センターの瀬川高弘講師、国立極地研究所の高橋晃周教授・國分亙彦助教、ミネソタ大学の石井聡准教授からなる研究チームは、南極昭和基地周辺のアデリーペンギンやナンキョクオオトウゾクカモメ(以下トウゾクカモメ)が様々な抗生物質耐性菌を保有していることを明らかにし、また抗生物質耐性菌が南極へ伝播した経路の調査をおこないました。その結果、南極から赤道付近まで長距離を移動するトウゾクカモメがインド洋で抗生物質耐性菌を取り込み、これらの遺伝子を南極に運び込み、南極での拡散に寄与していることを明らかにしました。本成果を踏まえた南極地域の野生動物における病原体の監視やリスク管理の促進が期待されます。
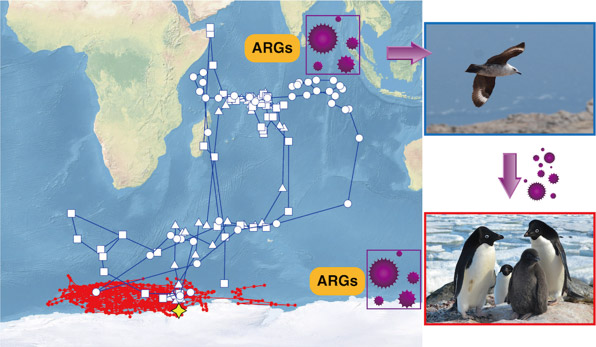
研究成果の概要図
研究の背景
抗生物質耐性遺伝子(*注1)の拡散による社会問題は深刻なものとなると予想されています。抗生物質耐性菌の増加は、従来の抗生物質を用いた感染症の治療を難しくし、公衆衛生に対する脅威を増大させています。また、抗生物質耐性菌は地球規模で広がりつつあり、北極や南極からも検出されています。特に南極では、主に人間活動レベルが大きい南極半島域において、ペンギンや渡り鳥の排泄物をはじめ、土壌などにも抗生物質耐性菌が存在することが確認されています。これらの抗生物質耐性菌は、動物が南極での人間活動に間接的に接触する過程で獲得したと従来考えられてきました。一方、これまでの研究は南極半島域に集中しており、人間の活動が比較的少ない東南極における抗生物質耐性菌の広がりについては、ほとんど知られていませんでした。さらに、自然経路や人為的経路を通じた南極への抗生物質耐性菌の伝播機構も明らかではありませんでした。
そこで本研究では、人間の活動レベルが南極半島に比べて低い東南極域を対象に、南極地域の野生鳥類がどの程度抗生物質耐性菌を保有しているのか、また抗生物質耐性菌がどのようにして南極へと伝播しているのか明らかにすることを試みました。
研究の成果
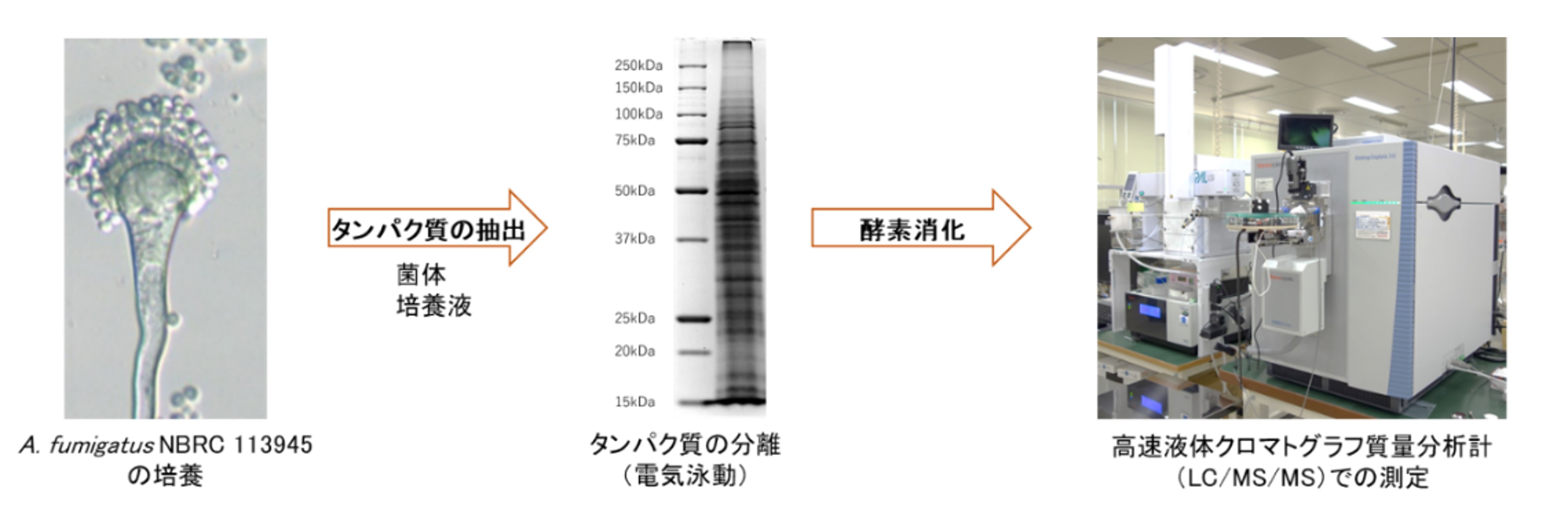
本研究では、昭和基地近くの繁殖コロニーのアデリーペンギンとトウゾクカモメの糞サンプルを分析し(図1)、多種多様な遺伝子を一斉検出可能なハイスループット定量PCR法を用いて抗生物質耐性遺伝子と潜在的病原体を検出しました。その結果、両鳥種の糞から複数の潜在的病原体が確認され、南極生態系においてこれらの病原体が広がっていることが示唆されました(図2)。一方で、繁殖コロニー近くの海水サンプルやすべての糞サンプルから、人間の糞便による汚染を示すマーカーは検出されませんでした。これは、一般に潜在的病原体の拡散に寄与するとされる人間の糞便経由の汚染が、研究地域においてはほとんどなかったことを示しています。
病原体に加えて、アデリーペンギンとトウゾクカモメの糞において抗生物質耐性遺伝子と金属耐性遺伝子を分析した結果、93%のアデリーペンギンのサンプルと100%のトウゾクカモメのサンプルから耐性遺伝子が検出されました。これらの耐性遺伝子には臨床的に重要な抗生物質に対する耐性を示すものも含まれていました。特に、移動性の高いトウゾクカモメではより多くの耐性遺伝子が検出され、これは地域間での遺伝子の移動に関与している可能性が示唆されました(図3)。
次に、これらの鳥がどのようにして抗生物質耐性遺伝子や病原体を獲得し、伝達しているのかをより深く理解するため、ジオロケーター(*注2)を用いてアデリーペンギンとトウゾクカモメの渡りパターンを分析しました。その結果、トウゾクカモメが南半球の冬にインド洋の熱帯および亜熱帯地域に移動することが確認され、これらの地域から耐性遺伝子を取り込み南極に運んでいる可能性が示唆されました。一方でアデリーペンギンは一年を通じて南大洋域に留まることが示されました(図4)。インド洋は抗生物質耐性菌が多い地域の一つであり、トウゾクカモメが渡りの期間中に抗生物質耐性菌を取り込み、これらの遺伝子を南極に運び込み、南極での拡散に寄与していると考えられます。この結果から、長距離を移動する鳥類が地球規模での耐性遺伝子の伝播に重要な役割を果たしていることが示唆されました。
今後の展望
今回の研究結果は、南極地域での野生動物を介した抗生物質耐性菌と潜在的病原体の拡散メカニズムを明らかにしました。特に、トウゾクカモメなどの長距離を移動する鳥類が、抗生物質耐性菌を運ぶ「ベクター(媒介者)」として機能することが確認されました。このことは、これらの鳥類がその他の病原体をも南極に運び込む可能性があることを示唆しています。2024年2月には、高病原性鳥インフルエンザが初めて南極半島に到達し、ペンギンや海棲哺乳類を含む野生動物への感染が懸念される状況にあります。鳥インフルエンザは、人間の健康にも直接的な影響を及ぼす可能性があり、この問題は公衆衛生上も極めて重要です。
また、抗生物質耐性菌や病原体がトウゾクカモメからペンギンへ伝播する正確な経路については、さらなる調査が必要です。ナンキョクオオトウゾクカモメはアデリーペンギンのコロニーでペンギンの卵やヒナを捕食しているのが頻繁に観察され(図5)、これは糞のDNA分析の結果からも確認されました。このことから、トウゾクカモメが捕食のためにコロニーを訪れた際に抗生物質耐性菌や病原体を含む糞を落とし、ペンギンが巣の維持のために石を集めるときなどに、それらの糞や糞便汚染のある土に接触している事が推測されます。
この研究結果を踏まえ、今後は南極地域における抗生物質耐性菌や病原体の監視体制を強化する必要があります。特に、鳥インフルエンザのような病原体の監視には、野生動物の移動パターンを考慮した包括的なアプローチが必要となります。南極地域における野生動物とその生息地の保護をさらに強化するとともに、病原体の監視とリスク管理を促進することが、これからの大きな課題になると考えられます。
注
*注1:抗生物質耐性遺伝子
バクテリアがこの遺伝子が持つと、抗生物質の働きを阻害する物質を生産できるようになります。これらの遺伝子は、同種内や異なる種間のバクテリア集団で移動することがあります。バクテリアがこれらの遺伝子を獲得すると、抗生物質存在下でも生育できるようになります(抗生物質耐性菌の出現)。
*注2:ジオロケータ
動物に装着して移動経路を明らかにする装置の一つ。照度の記録から、動物がいた場所の日の出・日の入り時刻を決定し、その緯度・経度を推定することで動物の移動を追跡できます。
発表論文
論文名:Spread of antibiotic resistance genes to Antarctica by migratory birds.(渡り鳥による抗生物質耐性遺伝子の南極への拡散)
掲載誌:Science of The Total Environment
著者:
瀬川高弘(山梨大学 総合分析実験センター 講師)
高橋晃周(国立極地研究所 生物圏研究グループ 教授)
國分亙彦(国立極地研究所 生物圏研究グループ 助教)
石井聡(ミネソタ大学 准教授)
URL:https://doi.org/10.1016/j.scitotenv.2024.171345
オンライン公開日:2024年3月5日
研究サポート
本研究はJSPS科研費(新学術領域研究(研究領域提案型):17H05983、挑戦的研究(開拓):22K18432, 国際共同研究加速基金(国際先導研究):22K21355)、ミネソタ大学のMnDRIVEプログラムの助成を受けて実施されました。また、現地調査・試料採取は日本南極地域観測隊の一般研究観測課題(AP0922)として、第58, 59, 60次観測隊の支援により行われました。
お問い合わせ先
研究についての問い合わせ先
山梨大学 総合分析実験センター 瀬川 高弘
国立極地研究所 生物圏研究グループ 高橋 晃周
広報についての問い合わせ先
山梨大学総務企画部総務課広報企画室
国立極地研究所 広報室

図1:アデリーペンギンの巣と周辺の糞
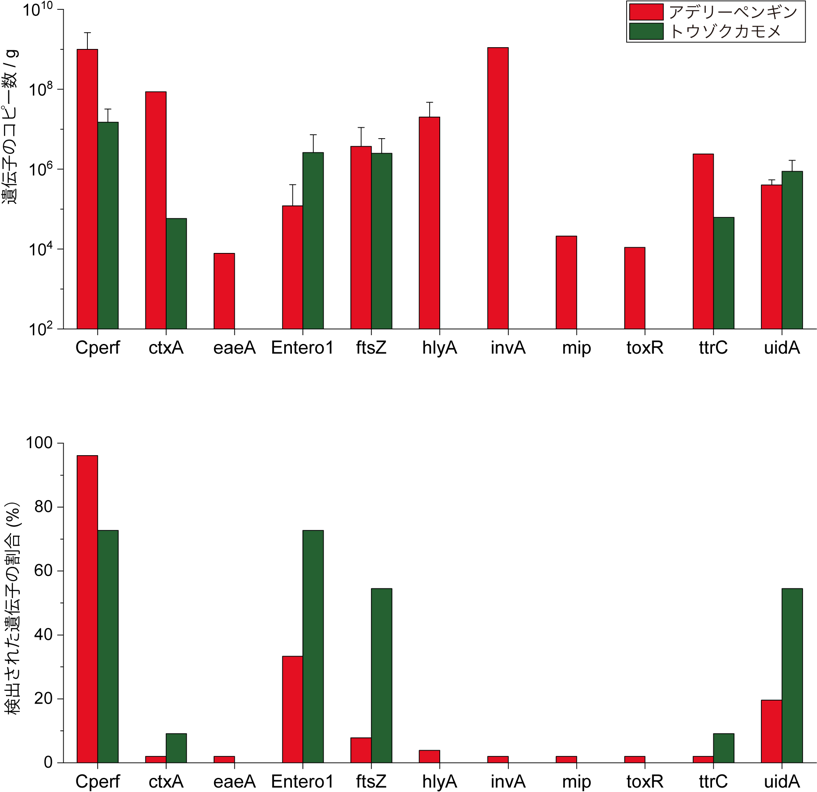
図2:ハイスループット定量PCR法で測定したアデリーペンギンとトウゾクカモメの糞便サンプル中の病原体の量と検出頻度。上図は、本研究で検出された病原体遺伝子の対数10変換量(コピー/g糞;n = 3)の平均を示す。空バーは定量限界以下であることを示す。下図は、糞便サンプル中の病原体の検出頻度(%)を示す。
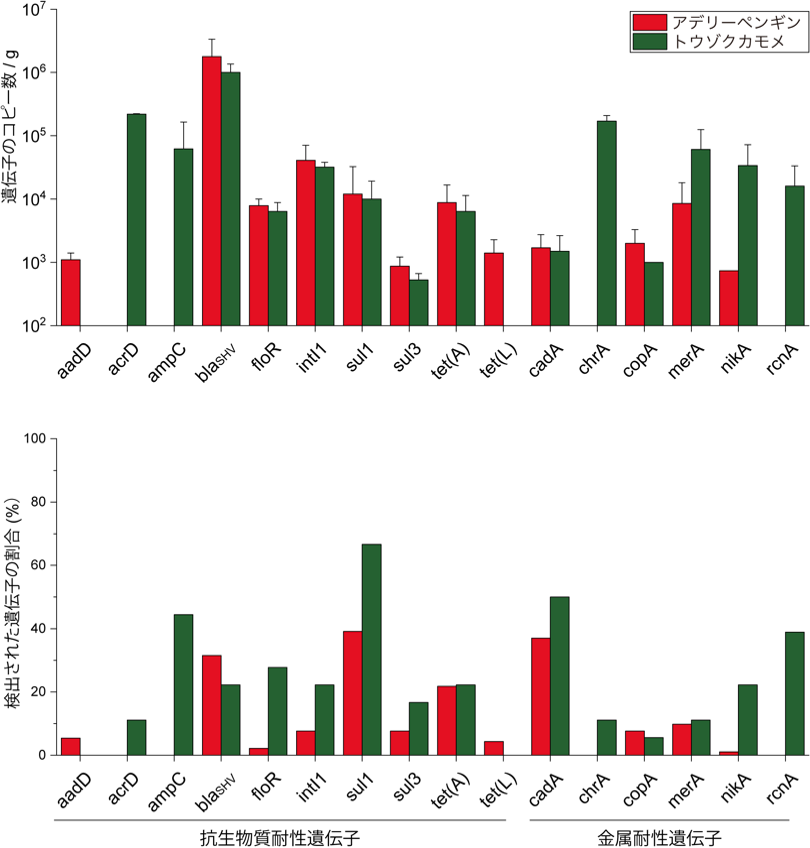
図3:ハイスループット定量PCR法で測定したアデリーペンギンとトウゾクカモメの糞便サンプル中の抗生物質耐性遺伝子と金属耐性遺伝子の量と検出頻度。上図は、本研究で検出された抗生物質耐性遺伝子と金属耐性遺伝子の対数10変換量(コピー/g糞;n = 3)の平均を示す。空バーは定量限界以下であることを示す。下図は、糞便サンプル中の抗生物質耐性遺伝子と金属耐性遺伝子の検出頻度(%)を示す。
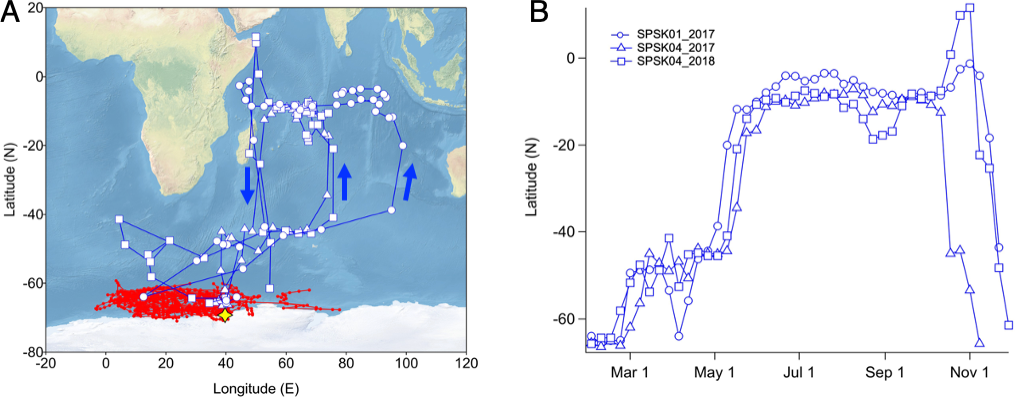
図4:
A) 非繁殖期におけるトウゾクカモメ(青、n = 3トラック)とアデリーペンギン(赤、n = 21トラック)の週ごとの位置。黄色の記号は繁殖地。
B)トウゾクカモメの3つのトラックの緯度方向の位置の季節変化。記号鳥のID(SPSK 01または04)と調査年(2017または2018)を示す。

図5:アデリーペンギンの卵を捕食するため、アデリーペンギンの巣に近づくナンキョクオオトウゾクカモメ。写真は2019年1月6日に南極昭和基地沿岸の袋浦のコロニーで撮影。