2024-07-19 国立がん研究センター
発表のポイント
- 広範な固形がんを対象とした日本初の産学連携全国がんゲノムスクリーニングプロジェクトであるSCRUM-Japan MONSTAR-SCREENプロジェクト(以下、MONSTARプロジェクト)で実施された4つの多施設共同研究の統合解析を行いました。これらの研究に参加された16,144人の患者さんの分子プロファイル及び治療成績や生存期間等に関する解析を行ったものになります。
- MONSTARプロジェクトに参加した患者さんのうち、分子プロファイルから見つけられたバイオマーカーに適合する標的治療を受けた患者さんは、標的治療を受けなかった患者さんと比較して、生存期間が延長することが明らかになり、バイオマーカーに基づく「がん個別化医療」の意義が確認されました。
- 現在、がんの分子プロファイルは、ゲノム解析に加えて、RNA解析(トランスクリプトミクス)、蛋白質解析(プロテオミクス)、代謝物質解析(メタボロミクス)等のマルチオミクス解析を活用する研究が進んでいます。
- MONSTARプロジェクトでは、がん個別化医療のさらなる発展を目指して、分子プロファイル技術を駆使したマルチオミクス解析を導入した新たな大規模研究を開始予定です。
概要
国立研究開発法人国立がん研究センター(理事長:中釜 斉、東京都中央区)東病院(病院長:土井 俊彦)の吉野 孝之副院長、橋本 直佳消化管内科/トランスレーショナルリサーチ支援室医員らの研究グループは、MONSTARプロジェクト注1のうち4つの研究(GI-SCREEN注2、GOZILA注3、MONSTAR-SCREEN注4、MONSTAR-SCREEN-2注5)に参加された16,144人の患者さんの統合解析を行いました。この解析では、患者さんのがんの分子プロファイル注6を詳細に調べ、バイオマーカーに基づく治験薬治療を受けた患者さんの割合や治療成績及びバイオマーカーに基づく標的治療を受けた患者さんの生存期間を調査しました。
解析の結果、治験薬治療を受けた患者さん(n=674人)のうち、奏効注7した患者さんは29.2%(n=197人)で、全生存期間の中央値は14.8ヶ月と延長した結果でした。また、本研究全体の約20%の患者さんがバイオマーカーに適合する標的治療を受けており、適合する標的治療を受けなかった患者さんと比べて、生存期間が長くなることが分かりました。
本研究結果により、バイオマーカーに基づく「がん個別化医療」の重要性が裏付けられたとともに、今後MONSTARプロジェクトがさらなるマルチオミクス解析注8技術を駆使して「がん個別化医療」を発展させることで、より多くのがん患者さんに有効な治療薬をいち早く届けられることが期待されます。
本研究成果は、米国癌学会旗艦誌「Cancer Discovery」に日本時間2024年7月18日付で掲載されました。
背景
近年、がんの遺伝子や分子の特徴を詳細に調べる分子プロファイリング技術が大きく進歩し、それぞれの患者さんに合わせた「がん個別化医療」が発展してきました。
国立がん研究センター東病院では、2015年にSCRUM-Japanという産学連携全国がんゲノムスクリーニングプロジェクトを立ち上げ、全国の医療機関や製薬企業と協力して、がん患者さんの分子プロファイリングを行う取り組みを進めてきました。本プロジェクトの目的は、より有効な治療薬を一刻も早く、より多くのがん患者さんにお届けすることです。中でも、MONSTARプロジェクトは、肺がん以外の固形がん患者さんを対象に様々な大規模な研究を行ってきました。これまでに、24,000人以上の患者さんがMONSTARプロジェクトの研究に参加され、遺伝子や分子の特徴を調べたマルチオミクス解析の結果と詳しい臨床情報を集めたデータベースが作られています。
このような大規模プロジェクトのデータを使って、治験薬の効果やバイオマーカーに基づく治療法の有効性を評価した報告は従来ほとんどありません。そこで、今回MONSTARプロジェクトで実施された4つの研究の結果を統合して、世界でも有数の大規模な解析を行いました。
研究の方法・成果
本研究では、MONSTARプロジェクトで行われたGI-SCREEN、GOZILA、MONSTAR-SCREEN、MONSTAR-SCREEN-2の4つの大規模な臨床研究に参加された16,144人の患者さんのデータを統合的に解析し、治験に参加された患者さんの特徴や治療の標的となったバイオマーカーの種類、治療薬の効果などを詳しく調べました。その結果、治験に参加された患者さんの割合は全体の5.0%で、その中でも大腸がん(51.8%)、胆道がん(9.5%)、胃がん(9.0%)、食道がん(5.3%)、膵臓がん(5.0%)の患者さんが多くを占めていました。また、治験に参加するタイミングは四次治療以降が46.4%と最も多く、一次治療での参加は9.6%と少数でした。治験薬による治療を受けた患者さん(n=674人)のうち、奏効した患者さんは29.2%(n=197人)で、全生存期間の中央値は14.8ヶ月と延長した結果が得られました。最も治療効果が高かった治験薬は、抗HER2治療薬注9でした(図1)。
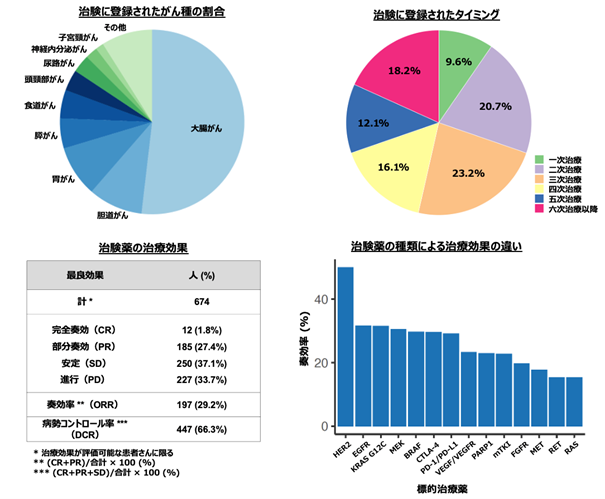
図1 MONSTARプロジェクトから治験に参加された患者さんの治療解析
さらに、バイオマーカーに適合する治療を受けた患者さんの生存期間中央値は19.1ヶ月であったのに対し、適合する治療を受けなかった患者さんの生存期間中央値は15.3ヶ月でした。このことから、バイオマーカーに基づいた標的治療により、患者さんの生存期間が延長する可能性があることが分かりました(ハザード比0.767、P<0.001)(図2)。
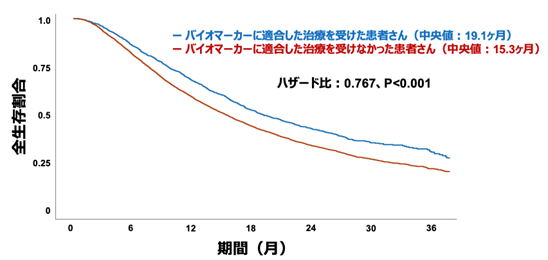
図2 バイオマーカーに適合した治療を受けたかどうかによる生存解析
以上の結果から、MONSTARプロジェクトで行った分子プロファイリングに基づき、多くの患者さんが治験薬による治療を受けて有効な効果が得られており、さらに、バイオマーカーに適合する標的治療が患者さんの予後を改善する可能性が示されました。
MONSTARプロジェクトの遂行にあたり、研究にご協力いただきました患者さんとそのご家族の皆様、全国の医療機関の皆様、またプロジェクトの運営に関わってくださった多くの関係者の皆様にこの場を借りて深く感謝申し上げます。
展望
本研究の成果は、様々な分子プロファイリング検査で見つかったバイオマーカーに基づいて適合する標的治療を届ける「がん個別化医療」の重要性を明確に示すものです。近年の解析技術や創薬技術の目覚ましい発展により、患者さん一人ひとりの腫瘍の特徴をより詳細に調べる精密な分子プロファイリングが可能になってきました。こうした最先端技術を駆使することで、より多くのがん患者さんに、より早く、より有効な治療薬を届けられることが大いに期待されます。
さらに、MONSTARプロジェクトでは、新たな大規模研究「MONSTAR-SCREEN-3」を開始予定ですこの研究では、対象を進行固形がんの患者さんだけでなく、治癒切除が可能な早期の固形がんの患者さんや血液腫瘍の患者さんにも広げ、それぞれの病態に応じた最先端のマルチオミクス解析を行う予定です。今後も世界最先端のマルチオミクス解析を活用し、世界中のがん患者さんとそのご家族に有効な治療法を届けられるよう、「がん個別化医療」の発展に全力で取り組んでまいります。
MONSTARプロジェクトについて
MONSTARプロジェクトは、広範な固形がんを対象とした日本初の産学連携全国がんゲノムスクリーニングプロジェクトとして、参加された患者さんに有効な診断薬・治療薬をいち早く届けることを目指し、様々な専門分野の研究者や医療従事者からなる複数の委員会活動によって支えられて数多くの研究を行っています。また、MONSTARプロジェクトでは、がんの遺伝子や分子の特徴だけではなく、治療内容や治療効果などの詳しい臨床情報を長期間にわたって収集しており、それらの膨大なデータは国立がん研究センター東病院に設置されたスーパーコンピュータ「KASHIWARP」に安全に保管されています。「KASHIWARP」は、人工知能を駆使した解析を含む様々な最先端のソフトウェアを備えており、収集された膨大なデータを高速かつ効率的に解析することができます(図3)。
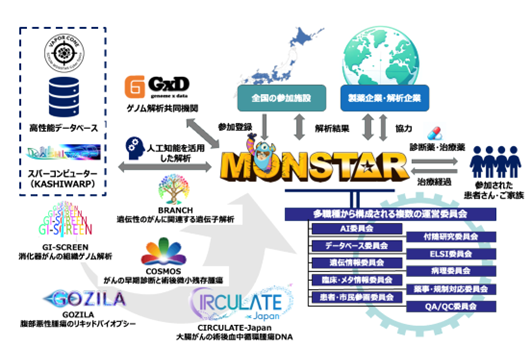
図3 SCRUM-Japan MONSTARプロジェクトの概要
論文情報
雑誌名
Cancer Discovery
タイトル
The SCRUM-MONSTAR Cancer-Omics Ecosystem: Striving for a Quantum Leap in Precision Medicine
著者
Tadayoshi Hashimoto, Yoshiaki Nakamura, Takao Fujisawa, Mitsuho Imai, Taro Shibuki, Naoko Iida, Hiroshi Ozaki, Norio Nonomura, Chigusa Morizane, Hiroji Iwata, Susumu Okano, Wataru Yamagami, Naoya Yamazaki, Shigenori Kadowaki, Hiroya Taniguchi, Makoto Ueno, Shogen Boku, Eiji Oki, Yoshito Komatsu, Satoshi Yuki, Akitaka Makiyama, Tomoyuki Otsuka, Hiroki Hara, Naohiro Okano, Tomohiro Nishina, Yasutoshi Sakamoto, Izumi Miki, Shin Kobayashi, Junichiro Yuda, Shun-Ichiro Kageyama, Michiko Nagamine, Shingo Sakashita, Naoya Sakamoto, Riu Yamashita, Yoshikatsu Koga, Hideaki Bando, Genichiro Ishii, Takeshi Kuwata, Woong-Yang Park, Atsushi Ohtsu, Takayuki Yoshino*
*Corresponding author
DOI
10.1158/2159-8290.CD-24-0206
掲載日
2024年7月18日(日本時間)
URL
https://aacrjournals.org/cancerdiscovery/article/doi/10.1158/2159-8290.CD-24-0206/746433/The-SCRUM-MONSTAR-Cancer-Omics-Ecosystem-Striving(外部サイトにリンクします)
用語解説
注1 SCRUM-Japan MONSTAR-SCREEN
SCRUM-Japanは、2013年に開始した肺がん患者さんを対象としたLC-SCRUM-Japan(現:LC-SCRUM-Asia)と、2014年に開始した消化器がん患者さんを対象としたGI-SCREEN-Japan(現:MONSTAR-SCREEN)が統合した産学連携がんゲノムスクリーニングプロジェクトです。
注2 GI-SCREEN(2015年~2019年)
消化器がん患者さんを対象とした多施設共同のがん遺伝子スクリーニング研究で、進行消化器がんの患者さんの腫瘍組織を遺伝子パネル検査(Oncomine Comprehensive Assay)で解析し、治療薬を届ける全国がんゲノムスクリーニングプロジェクトで、5,743人の患者さんが登録されました。
注3 GOZILA(2018年~2024年)
進行消化器がんの患者さんを対象として、血液を用いた遺伝子解析(リキッドバイオプシー)でスクリーニングを行うプロジェクトです。米国Guardant Health社が開発した高感度な遺伝子解析技術Guardant360(R)アッセイが用いられ、現在約5,500人の患者さんが登録されております。(現在一部の関連試験を残して登録を完了しております。)
注4 MONSTAR-SCREEN(2019年~2021年)
広範な固形がん患者さんを対象として、患者さんのがん組織だけでなく、リキッドバイオプシー、糞便を用いた腸内細菌叢(マイクロバイオーム)の検査・解析などを行うスクリーニングプロジェクトです。組織の解析にはFoundationOne CDx、リキッドバイオプシーにはFoundationOne Liquid CDxという技術が用いられ、2,224人の患者さんが登録されました。
注5 MONSTAR-SCREEN-2(2021年~2024年)
肺がん以外の進行固形がん患者さんを対象として、患者さんのがん組織だけでなく、リキッドバイオプシーを用いて、がんのDNA・RNA・タンパク質などの異常を網羅的に解析するスクリーニングプロジェクトで、2,768人の患者さんが登録されました。これらの検査から得られるデータは膨大であることから、多量な情報をすばやく処理するための手法として人工知能を用いた解析も導入しました。
注6 分子プロファイル
分子プロファイルとは、がんの詳しい特徴のことで、遺伝子や蛋白質発現の変化を詳しく調べることで明らかになります。この分子プロファイルを詳しく調べることを分子プロファイリングと呼び、それぞれの患者さんのがんの特徴を知ることで、患者さん一人一人に合わせた治療法を選ぶ際の重要な情報となります。
注7 奏効
奏効は、完全奏効(完全に腫瘍が消失)と部分奏効(腫瘍病変の径和が30%以上減少)に分類されますが、本研究においては完全奏効と部分奏効を合わせて「奏効」と言います。
注8 マルチオミクス解析
遺伝子解析(ゲノミクス: Genomics)、RNA解析(トランスクリプトミクス: Transcriptomics)、蛋白質解析(プロテオミクス: Proteomics)、代謝物質解析(メタボロミクス:Metabolomics)等をすべて一括して分析する手法で、“ミクス (-omics)”は総合的解析を意味します。
注9 抗HER2治療薬
HER2(human epithelial growth factor receptor type 2)とは、HER familyに属する細胞膜に存在するタンパクです。HER2タンパクは正常細胞において細胞の増殖に関与していますが、何らかの理由で、HER2タンパクの過剰発現やHER2遺伝子の増幅が起こると細胞の増殖が制御できなくなり、がん化に結びつくと考えられています。複数のがんでHER2タンパクの過剰発現が確認され、日本でもHER2タンパクを標的とした薬剤が既に承認されており、がん治療の有力な標的分子と考えられています。
お問い合わせ先
研究に関するお問い合わせ
国立研究開発法人国立がん研究センター
東病院 SCRUM-Japan事務局
広報窓口
企画戦略局 広報企画室(柏キャンパス)