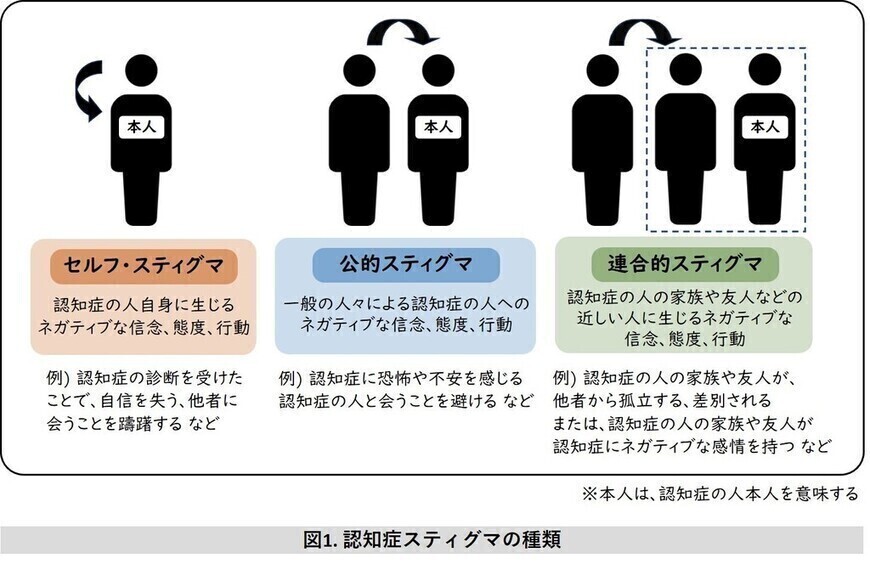
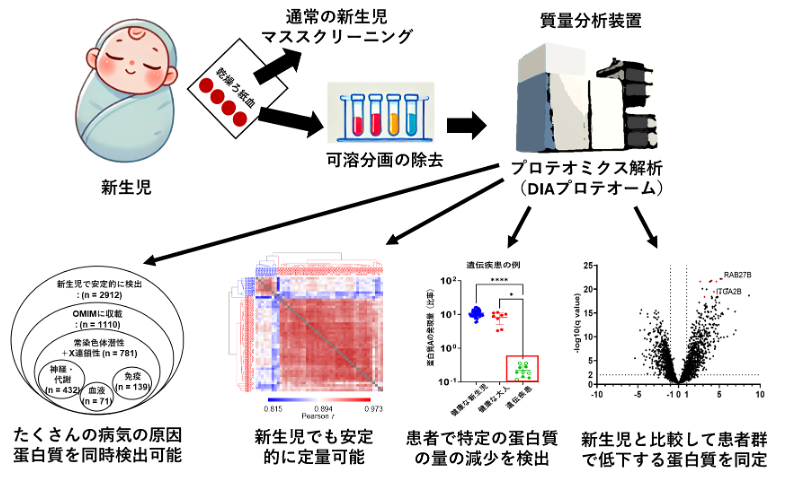
2024-11-01 東京大学
- 2024年3月に米国の乳牛で確認された高病原性鳥インフルエンザウイルス(H5N1亜型)は、牛から牛への感染伝播のみならず、ヒトなどの哺乳類にも感染伝播している。
- ニワトリ由来高病原性H5N1鳥インフルエンザウイルスのHAを基に作製したLNP-mRNAワクチン候補製剤の、牛由来高病原性H5N1鳥インフルエンザウイルスに対する防御効果をマウスモデルで評価したところ、同製剤がウイルスの増殖および病原性を強力に抑制することが明らかになった。
- LNP-mRNAワクチンモダリティは、主に呼吸器において増殖する新型コロナウイルスに対する有効性が既に示されているが、高病原性鳥インフルエンザのように全身感染を引き起こすウイルスに対しても高い防御効果を持つことが、新たに明らかになった。
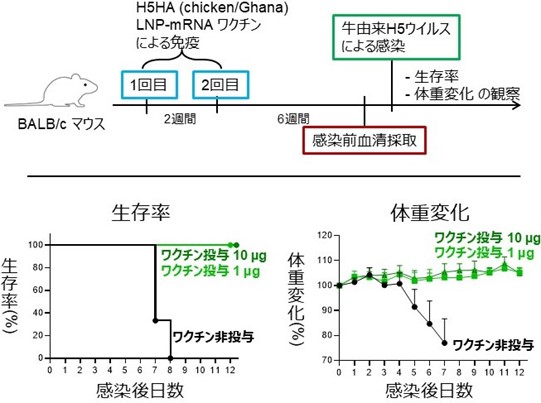
LNP-mRNAワクチンによる免疫スケジュールと生存率・体重変化への影響
発表内容
東京大学国際高等研究所 新世代感染症センター 河岡義裕 機構長らの研究グループおよび第一三共株式会社は、鳥インフルエンザH5HAの lipid nanoparticle (LNP)-mRNA ワクチン (注1) 候補製剤が、2024年に米国の乳牛で流行中の高病原性H5N1鳥インフルエンザウイルス(注2)に対する高い防御効果を示すことを、マウスモデルで明らかにしました。
H5N1亜型高病原性鳥インフルエンザウイルスは、1996年の出現以来、ヒトにおいて重篤な症状をひきおこし、高い致死率 (>50%) を示します。高病原性H5ウイルスは、初めは主にアジアにおいて感染例が報告されてきましたが、clade 2.3.4.4b (注3) のウイルスが2016年にヨーロッパで検出され、さらに2020年以降北米・南米も含めた世界中で、野鳥・家禽だけでなく様々な種の哺乳類の感染例が見られるようになりました。2024年、米国の乳牛からH5N1亜型の高病原性ウイルスが検出され、ウシ間の感染伝播のみならず、ネコやヒトの感染例も報告されています。高病原性鳥インフルエンザの種の壁を越えた感染伝播と拡大の危険性を念頭に置いた事前の準備の重要性が高まっています。
本研究では、2021年にニワトリから分離された高病原性鳥インフルエンザH5N1ウイルス (A/chicken/Ghana/AVL-76321VIR7050-39/2021) のHAのLNP-mRNAワクチン候補製剤の牛由来高病原性ウイルスに対する防御効果を、マウスモデルにおいて検証しました。
マウスをLNP-mRNAワクチン候補製剤を用いて2週間間隔で2回免疫し、2回目の免疫の6週間後の血清中のHA結合抗体価を調べたところ、ワクチンのニワトリH5ウイルスのHAに対してのみならず、牛由来H5ウイルスのHAに対しても有意に高いHA結合抗体が誘導されていることが明らかになりました(図1)。
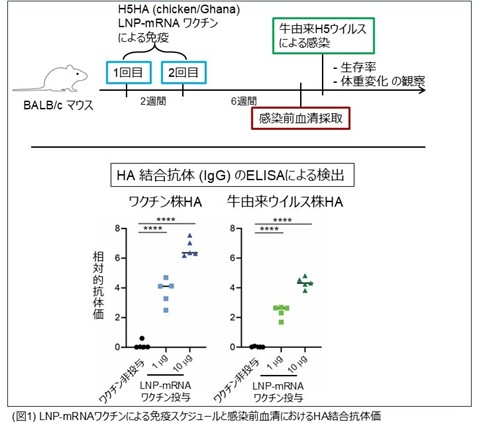
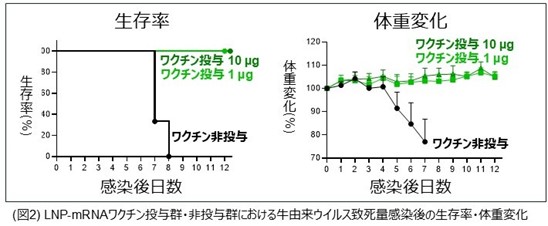
また、免疫したマウスに致死量の牛由来ウイルスを経鼻感染させたところ、非ワクチン群の個体が感染7日で死滅したが、ワクチン投与群は低用量・高用量投与のいずれの群でも全個体が生存し、ウイルスの病原性の指標である体重減少もまったく見られませんでした(図2)。
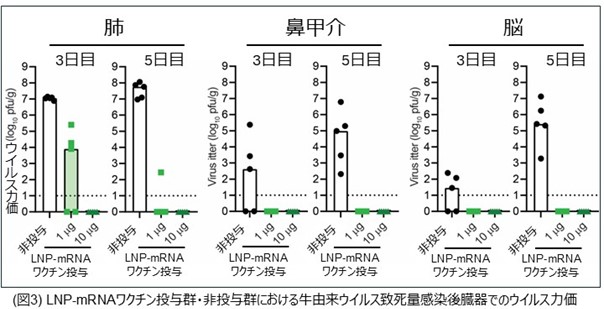
同様にLNP-mRNAワクチン候補製剤で2回免疫したマウスに致死量の牛由来ウイルスを感染させ、感染後3・5日目の臓器におけるウイルス力価を定量したところ、ワクチン非投与群では、肺、鼻甲介、脳において105 – 108 plaque forming unit (pfu) という高いウイルス力価が検出されましたが、ワクチン投与群ではウイルス増殖が強く抑制され、特に高用量投与群では、いずれの臓器でも感染性ウイルスが検出されませんでした (図3)。
すなわち、H5HA LNP-mRNAワクチンの投与が、強力な免疫応答を賦与し、牛由来ウイルスに対して高い防御効果を示すことが明らかになりました。
これらの結果から、LNP-mRNAワクチンは、牛由来H5ウイルスのように種の壁を越えたウイルスの感染やパンデミックに備える意味で、非常に有望なモダリティであると考えられます。本研究は10月30日、英国科学誌「eBioMedicine」(オンライン版)に公表されました。
発表者
東京大学国際高等研究所 新世代感染症センター
河岡 義裕 特任教授/機構長
兼:国立国際医療研究センター研究所 国際ウイルス感染症研究センター長
東京大学医科学研究所 ウイルス感染部門 特任教授
研究助成
本研究は、東京大学国際高等研究所 新世代感染症センターが東京大学医科学研究所、国立国際医療研究センターの協力のもと、第一三共株式会社と共同で実施し、日本医療研究開発機構(AMED)新興・再興感染症研究基盤創生事業 (中国拠点を基軸とした新興・再興および輸入感染症制御に向けた基盤研究)、AMED SCARDAワクチン開発のための世界トップレベル研究開発拠点の形成事業 (ワクチン開発のための世界トップレベル研究開発拠点群 東京フラッグシップキャンパス(東京大学新世代感染症センター))、ならびにAMED SCARDA ワクチン・新規モダリティ研究開発事業(インフルエンザワクチンに関する研究開発)の一環として行われました。
用語解説
(注1)Lipid nanoparticle (LNP)-mRNA ワクチン
ウイルス抗原の遺伝子をコードするmRNAを脂質ナノ粒子(lipid nanoparticle; LNP)に封入した形状のワクチン。LNPは、生体内にワクチンを投与した際に細胞内に効率よくmRNAが送達する役割、および免疫応答を賦活化する役割を兼ね備える。生体内で、mRNAを鋳型として抗原たんぱく質が発現し、抗原特異的な免疫応答を惹起する。
(注2)鳥インフルエンザウイルス
A、B、C、D型の4種類に分類されるインフルエンザウイルスの中で、A型インフルエンザウイルスは、ウイルス表面にある2つの糖たんぱく質、ヘマグルチニン(HA)とノイラミニダーゼ(NA)の抗原性の違いにより、細かく亜型が分類されている。現在までに、HAでは18種類(H1からH18)、NAでは11種類(N1からN11)の亜型が報告されており、本研究で対象としたH5N1はH5亜型、N1亜型に分類されるA型インフルエンザウイルスのことをいう。抗原性の異なるHAとNAの組合せのウイルスが新たに出現した場合、パンデミックの危険性がある。
鳥インフルエンザはA型インフルエンザウイルスが原因となり生じる鳥の病気である。鳥インフルエンザウイルスは家禽に対する病原性を指標に、低病原性と高病原性に分類される。低病原性鳥インフルエンザウイルスに感染した家禽は無症状か軽い呼吸器症状、下痢、産卵率の低下を示す程度であるが、高病原性鳥インフルエンザウイルスでは重篤な急性の全身症状を呈して、ほぼ100%の家禽が死亡する。近年、野鳥・家禽のみならず、様々な種の哺乳類の高病原性鳥インフルエンザウイルスへの感染例が報告されている。
(注3)Clade 2.3.4.4b
H5HA は抗原性の違いでさらに細かいclade に分類される。Clade 2.3.4.4bに属するH5 ウイルスは、2016年に欧州で検出されたのを皮切りに、N6, N8 といったN1以外のNAとの組合せのウイルスも生じ、世界的に感染拡大した。2024年に北米の乳牛で検出されたウイルスは、clade 2.3.4.4bに属するHAを有するH5N1ウイルスである。一方で、インド、カンボジアといったアジア地域ではその間、clade 2.3.2.1a や2.3.2.1cといったH5ウイルスが主に検出されている。
論文情報
Shiho Chiba*, Maki Kiso, Shinya Yamada, Kazuhiko Someya, Yoshikuni Onodera, Aya Yamaguchi, Satoko Matsunaga, Nao Jounai, Seiya Yamayoshi, Fumihiko Takeshita, and Yoshihiro Kawaoka¶, “Protective effects of an mRNA vaccine candidate encoding H5HA clade 2.3.4.4b against the newly emerged dairy cattle H5N1 virus,” eBioMedicine, doi:10.1016/j.ebiom.2024.105408.
論文へのリンク (掲載誌)
お問い合わせ先
〈研究に関する問合せ〉
東京大学国際高等研究所 新世代感染症センター
河岡 義裕(かわおか よしひろ)特任教授/機構長
兼:
国立国際医療研究センター研究所 国際ウイルス感染症研究センター長
東京大学医科学研究所 ウイルス感染部門 特任教授