2024-12-25 東京大学医科学研究所
発表のポイント
- デングウイルス(略称DENV)は、デング熱を引き起こすウイルスです。蚊を介して人から人へ感染する蚊媒介性ウイルスとして知られ、有効な予防薬、治療薬は未だありません。重症化するとデング出血熱やデングショック症候群などを引き起こし死に至る危険性があります。
- DENVの予防及び治療を目的として、核酸医薬として知られ機能が異なる2種の分子、small interfering RNA (siRNA)とRNAアプタマーとを1つの複合体とすることでDENVに結合する機能とDENV由来遺伝子を分解する機能を持つDENV増殖抑制核酸分子「キメラ核酸」を開発しました。
- キメラ核酸は今後、様々なウイルス感染症に対し幅広く応用できる分子形態であると期待されます。
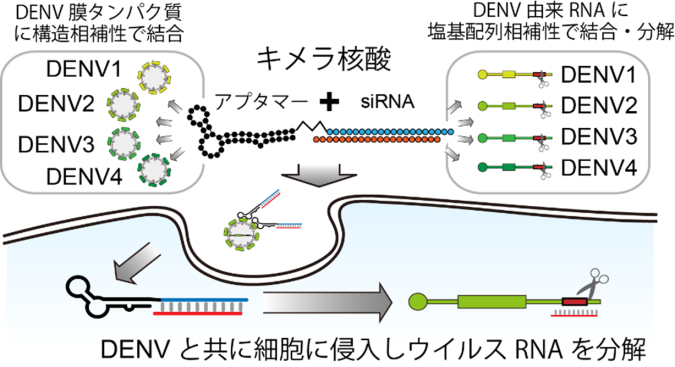
キメラ核酸がDENVに作用する概念図
概要
東京大学医科学研究所RNA医科学社会連携研究部門の高橋理貴特任准教授(開発当時)、株式会社リボミックの中村義一代表取締役社長(東京大学名誉教授)、東京大学大学院医学系研究科国際保健学専攻国際生物医科学講座のMOI MENG LING教授、東京大学医科学研究所附属アジア感染症研究拠点の山本瑞生特任講師、早稲田大学理工学術院の浜田道昭教授らによる研究グループは、DENVの増殖を抑制する新たな核酸分子を開発しました。
DENVは大きく分けて4つの種類(DENV1~4の血清型、注1)が存在します。それに対応するワクチン開発も進んでいる一方で、未だ有効な予防薬、治療薬が無いウイルス感染症として知られています。その課題克服のため、本研究グループでは、全血清型のDENVに対して、DENV膜タンパク質に構造相補性で結合するRNAアプタマー(注2)と、DENV由来のRNAに塩基配列相補性で分解に導くsiRNA(注3)とを個別に開発しました。加えて、それら核酸分子を1分子として結合させることで、DENVに結合し、DENV感染と共に細胞内に侵入することでウイルス由来のRNAを感染した細胞内で分解する多機能核酸分子「キメラ核酸(siRNA-aptamer複合体)」を開発し、その有効性を疑似的な感染評価系および実際のウイルス感染評価系を用いて評価しました。その結果、我々が開発したキメラ核酸はDENVの増殖を強く抑制できることが分かりました。また、複数存在する血清型に対しても有効であることを示唆する結果も得られています。本分子の開発戦略は、DENV以外のウイルスにも適応できるものであり、幅広いウイルス感染症の予防及び治療分子の迅速な開発に新たな選択肢を提供することが期待できます。
本成果は12月25日、国際学術専門誌「Nucleic Acids Research Molecular Medicine」に掲載されました。
研究内容
RNAアプタマーは、一本鎖核酸が形成する様々な立体構造を基盤として、タンパク質など多様な標的に対して構造相補性で結合する分子です。標的に対する高い特異性と親和性を有し、化学的に改変・加工が容易であり、免疫反応を引き起こしにくいなどの特徴があることから、抗体医薬に代わる次世代医薬として期待されています。これまで血液中の液性因子を標的として機能阻害する医薬品として社会実装されてきたことに加え、近年では細胞膜タンパク質に結合するアプタマーを利用することで任意の細胞に種々の薬剤を送達する分子としての活用法も注目を集めています。一方、同じく核酸医薬として知られるsiRNAは、塩基配列相補性で標的とする細胞内の任意のRNAに結合し分解に導く分子として知られています。標的RNAに対する特異性・選択性が高く、分子設計が比較的容易であることから汎用的研究ツールとしても活用されています。しかし、医薬品としての活用を促進するためには細胞内に導入するための送達技術が必須であり、安全で効率的な送達技術の確立が課題とされています。アプタマー及びsiRNAの両者において、ウイルスの治療や予防を目的とした研究開発が行われていますが、それぞれ単剤としては中和活性や薬剤送達が課題となり社会実装が困難であるのが現状です。
本研究では、4つの種類・血清型が存在することで未だ有効な予防薬や治療薬が存在せず世界的に感染者の多いDENVを対象として、全ての血清型のDENV膜タンパク質に結合するアプタマーと、全血清型のDENV由来RNAを分解するsiRNAを開発することで、血清型を問わずDENVを増殖抑制するキメラ核酸の開発を行いました。アプタマー創製については、ウイルス様粒子(VLP)を用いた独自のアプタマー創製法(VLP-SELEX法)(Takahashi M et al., PNAS 2020)とアプタマー創製に特化した高度なバイオインフォマティクス(Ishida R et al., NAR 2020)を利用することで開発しました。その開発アプタマーの特徴を理解するために、ウイルス膜タンパク質と感染細胞の膜融合過程を評価する特殊な感染解析手法(Yamamoto M et al., Viruses 2020)で評価した結果、開発したアプタマーはDENVに対して強い結合力を持つ一方で、重要な感染過程の一つである膜融合は阻害しないことが分かりました。また、全血清型DENVに共通するRNA配列を標的としてsiRNAを設計し活性評価することで全血清型に対応するsiRNAの同定にも成功しました。その後、両者を結合させた複合体「キメラ核酸」による実際のDENVに対する抑制効果を確認した結果、複数の血清型に対しウイルス増殖を抑制できることを、古典的なPCR法に加え独自のウイルス中和活性解析手法 (Haga K et al., Pathogens 2023)によって実証することができました(図)。
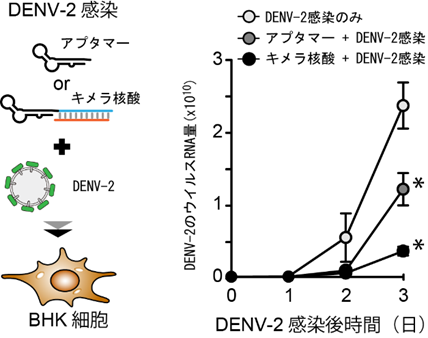 図.キメラ核酸のDENVに対する感染防御効果
図.キメラ核酸のDENVに対する感染防御効果
左)DENVの血清型の一つであるDENV-2とアプタマーもしくはキメラ核酸とを混合しBHK細胞(ハムスター腎由来細胞株)に添加した。右)添加0日、1日、2日、3日後にウイルスRNA量をPCR法にて測定した結果、キメラ核酸の添加によりウイルスRNAの増加を約10分の1程度に抑制できることが分かりました。
本研究では、開発したキメラ核酸が全血清型のDENVに対応する新たな増殖抑制分子としての実用が期待できることに加え、アプタマーとsiRNAから成るキメラ核酸がウイルス感染症の予防及び治療薬を開発する有効な一つの選択肢であることを示唆する成果になります。
発表者・研究者等情報
東京大学医科学研究所 RNA医科学社会連携研究部門
高橋 理貴 研究当時:特任准教授
株式会社リボミック
中村 義一 代表取締役社長 兼:東京大学名誉教授
東京大学大学院医学系研究科 国際保健学専攻 国際生物医科学講座 発達医科学
MOI MENG LING(モイ メン リン) 教授
東京大学医科学研究所附属アジア感染症研究拠点
山本 瑞生 特任講師
早稲田大学理工学術院
浜田 道昭 教授
論文情報
雑誌名:Nucleic Acids Research Molecular Medicine
題 名:A chimeric RNA consisting of siRNA and aptamer for inhibiting dengue virus replication
著者名:Ryo Amano, Masaki Takahashi*, Kazumi Haga, Mizuki Yamamoto, Kaku Goto, Akiko Ichinose, Michiaki Hamada, Jin Gohda, Jun-ichiro Inoue, Yasushi Kawaguchi, Meng Ling Moi, Yoshikazu Nakamura(*責任著者)
DOI: 10.1093/narmme/ugae025
URL: https://academic.oup.com/narmolmed/advance-article/doi/10.1093/narmme/ugae025/7918429
研究助成
本研究は、国立研究開発法人科学技術振興機構(JST) 戦略的創造研究推進事業(CREST)「AIアプタマー創薬プロジェクト」(JPMJCR21F1)、日本学術振興会 科学研究費助成事業 挑戦的研究(萌芽)(17K20087)、国立研究開発法人日本医療研究開発機構(AMED)橋渡し研究戦略的推進プログラム・シーズA(A159)、AMED ワクチン開発のための世界トップレベル研究開発拠点の形成事業(JP243fa627001)、AMED 新興・再興感染症に対する革新的医薬品等開発推進研究事業(24fk0108656h1302)、AMED 新興・再興感染症研究基盤創生事業・海外拠点研究領域事業(JP20wm0125002)の支援により実施されました。
用語解説
(注1)デングウイルス(DENV):デングウイルスは、主に熱帯および亜熱帯地域で流行するウイルスです。このウイルスは、4つの種類・血清型が存在し、感染すると、軽度から中等度の症状が現れることが多く、これらの症状は「デング熱」と呼ばれます。重症化すると死に至る危険性があります。
(注2)RNAアプタマー:配列依存的に様々な立体構造をとることで、様々な標的に対して結合することができる一本鎖核酸。核酸医薬としても利用されています。
(注3)siRNA:siRNA(small interfering RNA)は、遺伝子の発現を特異的に抑制する短い二本鎖RNA分子です。RNA干渉(RNA interference、RNAi)と呼ばれるプロセスを通じて、標的遺伝子のRNAを分解し、発現を阻害します。
問合せ先
〈研究に関する問合せ〉
東京大学医科学研究所RNA医科学社会連携研究部門
特任准教授 高橋 理貴(たかはし まさき)※開発当時
※現、株式会社リボミック 開発研究部・探索研究部
担当部長 高橋 理貴(たかはし まさき)
東京大学大学院医学系研究科 国際保健学専攻 国際生物医科学講座 発達医科学
教授 MOI MENG LING(モイ メン リン)
東京大学医科学研究所附属アジア感染症研究拠点
特任講師 山本 瑞生(やまもと みずき)
早稲田大学 理工学術院
教授 浜田 道昭(はまだ みちあき)
〈報道に関する問合せ〉
東京大学医科学研究所 プロジェクトコーディネーター室(広報)
早稲田大学広報室広報課