2022-08-11 ジョージア工科大学
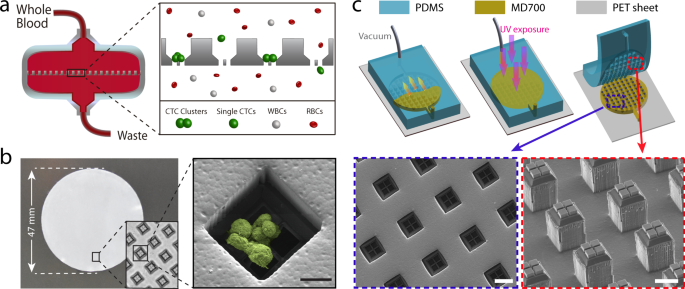
マイクロ流体チップの精度と膜ろ過の効率を組み合わせて、CTC(循環腫瘍細胞)クラスターを見つけるためのCluster-Wellと呼ばれる新しいタイプのチップを発明した。マイクロ流体チップは、ミクロンサイズの特徴を利用して、血液サンプル中の各細胞の位置を正確に特定し、それが癌であるかどうかを判断することができます。
<関連情報>
- https://research.gatech.edu/new-chip-could-make-treating-metastatic-cancer-easier-and-faster
- https://www.nature.com/articles/s41467-022-31009-9
メッシュ状マイクロウェルにおける循環腫瘍細胞クラスターのハイスループット、ラベルフリー分離 High throughput, label-free isolation of circulating tumor cell clusters in meshed microwells
Mert Boya,Tevhide Ozkaya-Ahmadov,Brandi E. Swain,Chia-Heng Chu,Norh Asmare,Ozgun Civelekoglu,Ruxiu Liu,Dohwan Lee,Sherry Tobia,Shweta Biliya,L. DeEtte McDonald,Bassel Nazha,Omer Kucuk,Martin G. Sanda,Benedict B. Benigno,Carlos S. Moreno,Mehmet A. Bilen,John F. McDonald & A. Fatih Sarioglu
Nature Communications Published:13 June 2022
DOI:https://doi.org/10.1038/s41467-022-31009-9
Abstract
Extremely rare circulating tumor cell (CTC) clusters are both increasingly appreciated as highly metastatic precursors and virtually unexplored. Technologies are primarily designed to detect single CTCs and often fail to account for the fragility of clusters or to leverage cluster-specific markers for higher sensitivity. Meanwhile, the few technologies targeting CTC clusters lack scalability. Here, we introduce the Cluster-Wells, which combines the speed and practicality of membrane filtration with the sensitive and deterministic screening afforded by microfluidic chips. The >100,000 microwells in the Cluster-Wells physically arrest CTC clusters in unprocessed whole blood, gently isolating virtually all clusters at a throughput of >25 mL/h, and allow viable clusters to be retrieved from the device. Using the Cluster-Wells, we isolated CTC clusters ranging from 2 to 100+ cells from prostate and ovarian cancer patients and analyzed a subset using RNA sequencing. Routine isolation of CTC clusters will democratize research on their utility in managing cancer.

